Clear Sky Science · de
Einzelzell-Analyse zeigt vielschichtige Merkmale der B‑Zell‑Entwicklung sowie altersassoziierte B‑Zell‑Subpopulationen
Wie sich unsere Antikörperfabriken mit dem Alter verändern
B‑Zellen sind die Antikörperfabriken des Körpers: Sie wehren Infektionen ab und machen Impfungen wirksam. B‑Zellen sind jedoch nicht alle gleich: Sie durchlaufen viele Entwicklungsstadien, leben in verschiedenen Geweben und verändern sich mit dem Alter. In dieser Studie wurden leistungsfähige Einzelzell‑Methoden eingesetzt, um B‑Zellen einzeln im menschlichen Knochenmark, Blut und in den Mandeln zu kartieren. Die Arbeit zeigt, wie sie heranreifen, mit Nachbarzellen kommunizieren und wie spezielle altersgebundene B‑Zellen bei älteren Erwachsenen stille Entzündungsprozesse fördern könnten.
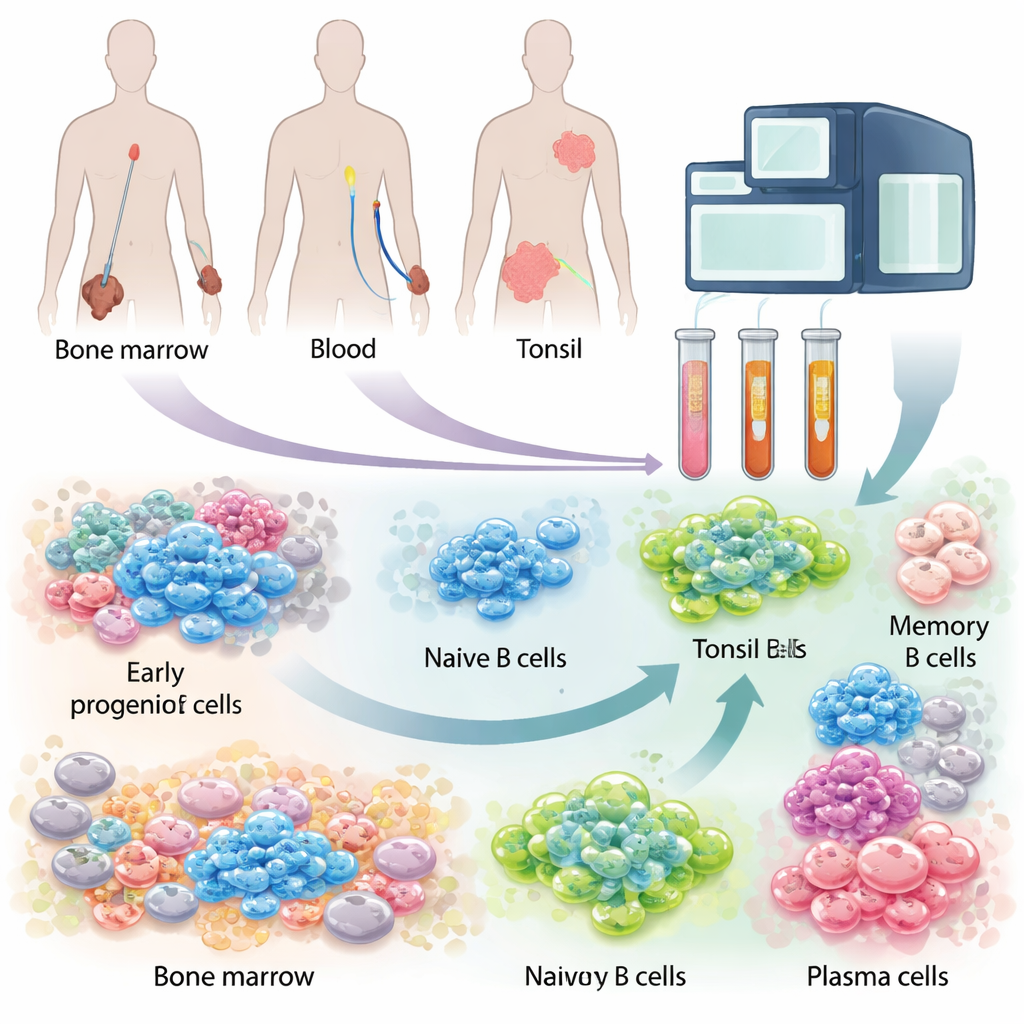
B‑Zellen von der Entstehung bis zur Abwehr verfolgen
Die Forschenden kombinierten mehrere große Datensätze und neue Experimente, um fast 200.000 einzelne Zellen zu analysieren. Sie fokussierten sich auf 18 unterschiedliche B‑Zell‑Typen, von den frühesten Vorläufern im Knochenmark bis zu voll ausgerüsteten, Antikörper freisetzenden Plasmazellen. Indem sie für jede Einzelzelle lasen, welche Gene aktiv waren und welche Antikörper die jeweilige B‑Zelle produzieren konnte, verfolgten sie die Entwicklungspfade der Zellen. Außerdem untersuchten sie die „Nachbarn“ der B‑Zellen — etwa myeloide Zellen und stromale Zellen des Knochenmarks — um das Unterstützungsnetzwerk zu verstehen, das die Schicksale der B‑Zellen formt.
Ruhige Phase in der mittleren Kindheit der B‑Zellen
Eine Überraschung war, dass unreife und naive B‑Zellen — Zellen, die ihren Zielpathogen noch nicht getroffen haben — ungewöhnlich ruhig sind. Mithilfe einer Methode, die darstellt, wie schnell Gene zeitlich an‑ und abgeschaltet werden, fand das Team heraus, dass frühe Vorläuferzellen und spätere Plasmazellen sehr aktive Genprogramme zeigen, während unreife und naive B‑Zellen geringe Aktivität und wenige sich verändernde Gene aufweisen. Das deutet darauf hin, dass B‑Zellen nach abgeschlossenen DNA‑Umordnungen eine ruhige, stoffwechselarmere „Wartephase“ durchlaufen, bevor sie das Knochenmark verlassen und in den zirkulierenden Pool eintreten, der auf künftige Infektionen reagieren kann.
Verborgene Vielfalt in vermeintlich „einfachen“ B‑Zellen
Obwohl naive B‑Zellen häufig als eine einheitliche Gruppe betrachtet werden, identifizierte die Studie spezialisierte Untergruppen. Einige naive Zellen zeigten Hinweise auf niedriggradige, homeostatische Proliferation — sanfte, selbst erneuernde Teilung, die die Zahl der Zellen ohne offensichtliche Infektion aufrechterhält. Andere wiesen Stress‑Antwort‑Signaturen und frühe Anzeichen eines Klassenwechsels der Antikörper auf, besonders in der Mandelumgebung. Bei Gedächtnis‑B‑Zellen, die frühere Begegnungen speichern, fanden die Autoren Hinweise auf zwei wichtige Entwicklungswege: einen, der auf Hilfe von T‑Zellen in klassischen Keimzentren angewiesen ist, und einen anderen, eher unabhängigen Pfad. Diese beiden Modelle, lange diskutiert, scheinen koexistieren zu können und erklären möglicherweise, warum Gedächtnis‑B‑Zellen so unterschiedlich auf neue Herausforderungen reagieren.
Wechselwirkungen mit Helferzellen in der Umgebung
B‑Zellen agieren nicht allein. Durch systematisches Durchsuchen nach passenden Paaren von Signalstoffen und Rezeptoren erstellten die Autoren Interaktionskarten zwischen B‑Zellen und umgebenden Zelltypen. Im Knochenmark bildeten stromale Zellen ein dichtes Netz von Kontakten, das frühe B‑Zellen nährt, während myeloide Zellen — wie dendritische Zellen und Monozyten — als wichtige Partner im Knochenmark, in Keimzentren der Mandeln und im Blut hervorgingen. Signale aus der TNF‑Familie und verschiedene Adhäsionsmoleküle dominierten diesen Austausch und veränderten sich je nach Reifestadium der B‑Zellen. Dieses Muster unterstreicht, wie physischer Kontakt und entzündliche Signale zusammen steuern, ob B‑Zellen überleben, sich teilen oder sterben.
Altersassoziierte B‑Zellen, die „Inflammaging“ antreiben könnten
Das Team entdeckte außerdem zwei ungewöhnliche B‑Zell‑Subsets, die hauptsächlich bei älteren Erwachsenen auftreten. Eine Gruppe unreif‑ähnlicher B‑Zellen produzierte S100A8 und S100A9 — Proteine, die normalerweise von myeloiden Zellen gebildet werden und mit chronischer Entzündung und Alterung assoziiert sind. Eine andere Gruppe exprimierte C1q, einen Bestandteil des Komplementsystems, dessen Spiegel mit dem Alter ansteigen. Nachfolgende Experimente zeigten, dass menschliche B‑Zellen S100A8/A9 in ihre Umgebung ausschütten können, und Studien an Mäusen verbanden höhere Mengen dieser Moleküle in B‑Zellen mit höherem Alter, insbesondere bei weiblichen Tieren. Diese Befunde legen nahe, dass bestimmte B‑Zellen selbst Quellen entzündungsfördernder Faktoren werden können und so zur niedriggradigen, langfristigen Entzündung beitragen, die im Alter häufig beobachtet wird.
Was das für Gesundheit und Alterung bedeutet
Indem B‑Zellen über Gewebe und Lebensphasen hinweg mit Einzelzellauflösung kartiert wurden, liefert diese Arbeit einen detaillierten Atlas darüber, wie unser Antikörpersystem aufgebaut, erhalten und altersbedingt verändert wird. Für Nichtfachleute ist die wichtigste Erkenntnis, dass B‑Zellen weit vielfältiger und dynamischer sind als früher angenommen und dass bestimmte B‑Zell‑Subsets bei älteren Personen zur altersbedingten Entzündung beitragen können. Das Verständnis dieser Wege und der zellulären Kommunikation könnte helfen, bessere Impfstoffe für Ältere zu entwickeln, die Immunalterung früher zu diagnostizieren und Therapien zu schaffen, die schädliche entzündliche B‑Zell‑Zustände dämpfen, ohne den wichtigen Schutz vor Infektionen zu beeinträchtigen.
Zitation: Yang, X., Tang, H., Lan, C. et al. Single-cell analysis reveals multi-faceted features of B cell development, together with age-associated B cell subpopulations. Commun Biol 9, 240 (2026). https://doi.org/10.1038/s42003-026-09515-z
Schlüsselwörter: B‑Zell‑Entwicklung, Einzelzellsequenzierung, Immunalterung, Gedächtnis‑B‑Zellen, Knochenmark‑Mikroumgebung