Clear Sky Science · de
Verknüpfung molekularer Spannung und zellulärer Zugkräfte: ein multiskaliger Ansatz zur Mechanik fokaler Adhäsionen
Wie Zellen ihre Umgebung fühlen und daran ziehen
Jedes Mal, wenn eine Zelle sich bewegt, teilt oder ein Gewebe umgestaltet, zieht sie unauffällig an ihrer Umgebung. Diese winzigen mechanischen Züge sind entscheidend bei Wundheilung, Krebs‑Ausbreitung und der Organentwicklung, sind aber schwer zu sehen und noch schwerer zu messen. Diese Studie stellt eine neue Methode vor, diese Kräfte aus zwei Perspektiven zugleich zu betrachten: wie stark eine ganze Zelle an einem weichen Material zieht und wie viel Kraft einzelne „molekulare Federn“ innerhalb der Zellverankerungen tragen. Durch die Verknüpfung dieser Sichtweisen hilft die Arbeit zu erklären, wie Zellen Steifigkeit wahrnehmen und ihren Halt an der Umgebung regulieren.
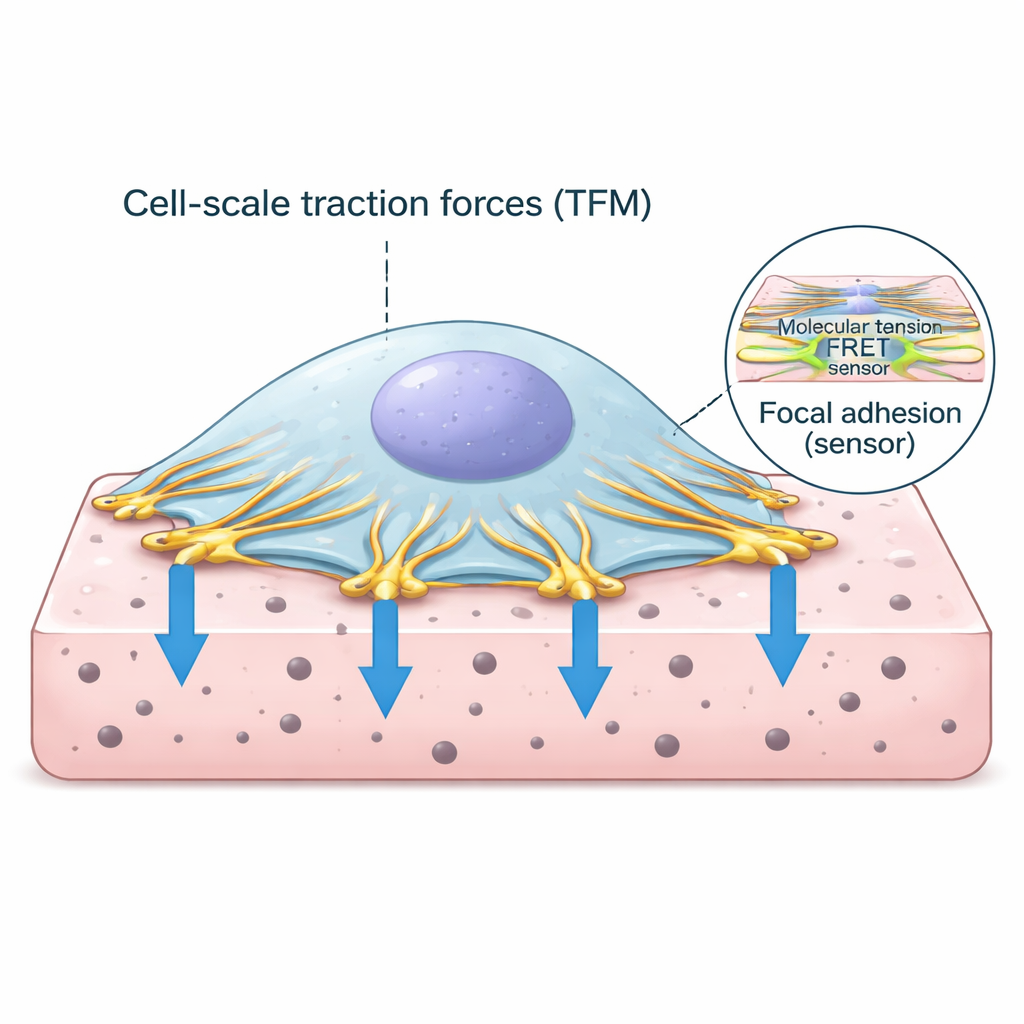
Die Griffpunkte der Zelle zur Außenwelt
Zellen treiben nicht einfach im Gewebe; sie verankern sich über spezialisierte Kontaktpunkte, die als fokale Adhäsionen bezeichnet werden. An diesen Stellen verbindet das interne Gerüst der Actinfasern Proteine, die die Zellmembran durchspannen und an der umgebenden Matrix haften. Eines der Schlüsselproteine in diesem Ankerkomplex ist Vinculin, das wie eine kraftempfindliche Verbindung wirkt. Wenn die kontraktile Maschinerie der Zelle an Actin zieht, spürt Vinculin die Belastung und hilft, die Verbindung zu verstärken. Zu verstehen, wie viel Kraft durch diese Verbindungen fließt und wie das mit dem gesamten Zugverhalten der Zelle zusammenhängt, ist zentral, um zu entschlüsseln, wie Gewebe gesund bleiben oder erkranken.
Zwei Fenster in zelluläre Kräfte
Die Forschenden kombinierten zwei leistungsfähige Techniken in einem einzigen Arbeitsablauf. Erstens misst die Tractionskraft‑Mikroskopie, wie stark eine Zelle ein weiches, gelartiges Substrat verformt, indem sie die Bewegung winziger fluoreszierender Kügelchen im Gel verfolgt. Aus diesen Kügelchenbewegungen lässt sich die Verteilung von Druck‑ und Zugkräften unter der Zelle berechnen. Zweitens trägt ein speziell konstruierter Vinculin‑Protein einen fluoreszenten Spannungssensor, dessen Lichtsignal sich ändert, wenn er gedehnt wird. Mithilfe fortgeschrittener Lebensdauermessungen (lifetime imaging) wandelte das Team dieses Lichtsignal in eine Ablesung molekularer Spannung an Vinculin um. Sie entwarfen dünne, flache Hydrogele, die mit hoher Auflösung abbildbar sind, und schrieben maßgeschneiderte Software, um beide Datensätze bis hin zu einzelnen Adhäsionsstellen auszurichten, zu segmentieren und zu analysieren.
Wie Steifigkeit den Aufwand der Zelle verändert
Als Zellen auf weichen im Vergleich zu steiferen Gelen kultiviert wurden, änderte sich ihr Verhalten auf deutliche Weise. Auf steiferen Substraten breiteten sich die Zellen stärker aus und übten stärkere Zugkräfte auf die Geloberfläche aus. Gleichzeitig zeigte die fluoreszente Ablesung des Vinculin‑Sensors eine erhöhte molekulare Spannung in fokalen Adhäsionen. Interessanterweise veränderten sich die grundlegenden strukturellen Merkmale dieser Adhäsionen — etwa ihre Anzahl oder die durchschnittliche Größe — zwischen weichen und steifen Gelen kaum. Stattdessen änderte sich die Organisation der Kräfte. Große, radial ausgerichtete Adhäsionen mit mehr Vinculin trugen tendenziell höhere Zugarbeiten, was darauf hindeutet, dass sowohl Geometrie als auch molekulare Zusammensetzung dieser Stellen beeinflussen, wie stark die Zelle zieht.
Eine komplexe Beziehung zwischen lokalen und molekularen Kräften
Bei genauerer Betrachtung einzelner Adhäsionen zeigte sich, dass die Verbindung zwischen lokalem Zug und Vinculin‑Spannung nicht universell ist. In manchen Zellen zeigten Adhäsionen mit höheren Zugarbeiten auch höhere Vinculin‑Spannung, was darauf hindeutet, dass engagierte, lasttragende Kontakte die Kraft direkter über ihre molekularen Verbindungen teilen. In anderen Zellen trat das entgegengesetzte Muster auf: Bereiche starker Zugkräfte waren mit geringerer Vinculin‑Spannung assoziiert, während andere Adhäsionen mehr molekulare Last trugen, ohne große äußere Zugkräfte zu erzeugen. Viele Zellen zeigten überhaupt kein klares Muster. Diese unterschiedlichen Verhaltensweisen spiegeln wahrscheinlich verschiedene Zellzustände wider — etwa aktive Ausbreitung, stabile Adhäsion oder Retraktion — und deuten darauf hin, dass Zellen Kräfte auf mehrere Arten über ihr Adhäsionsnetzwerk umverteilen können.
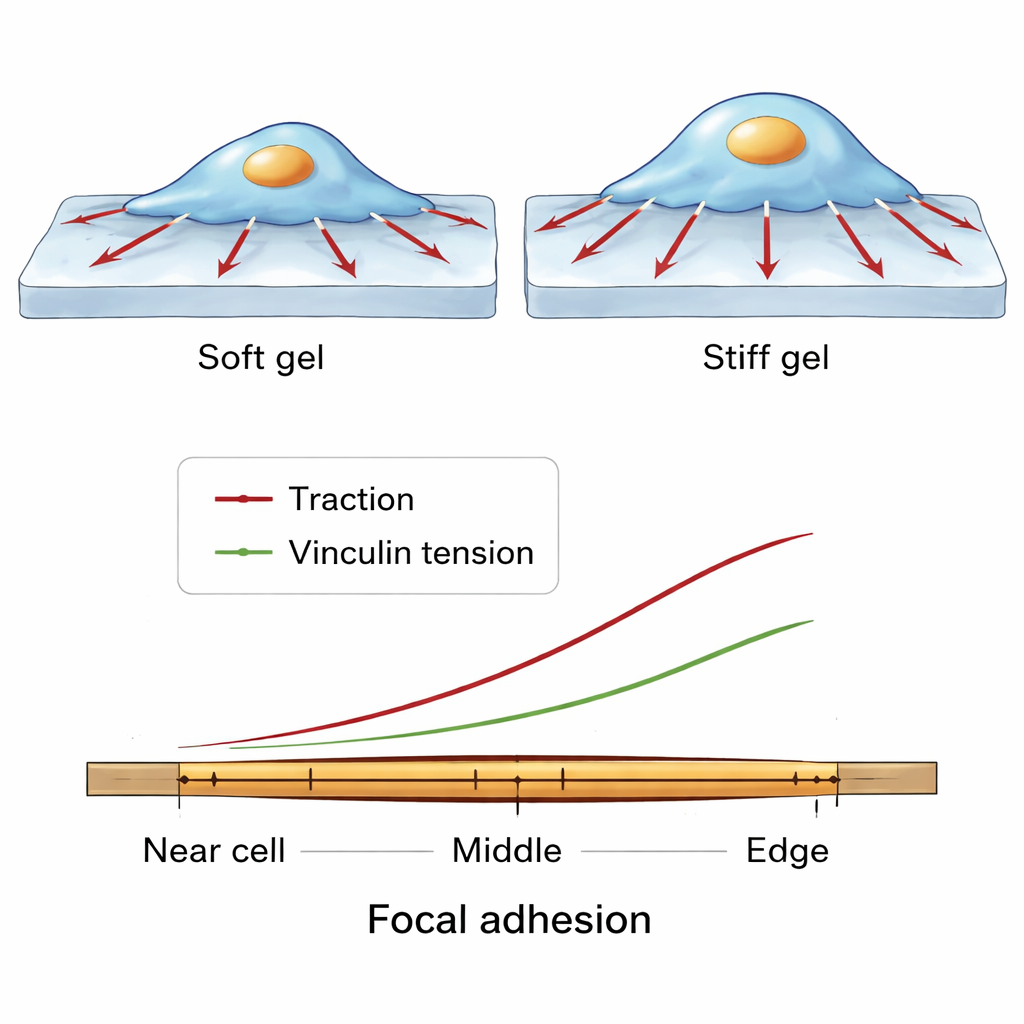
Feinräumige Kraftmuster entlang eines einzelnen Griffpunkts
Das Team zoomte dann noch weiter hinein und untersuchte, wie sich Kräfte entlang der Länge einer einzelnen fokalen Adhäsion ändern, von der dem Zellzentrum zugewandten Seite bis zur Kante nahe dem Zellrand. Über viele Zellen und Bedingungen ergab sich ein konsistentes Muster. Vinculinmoleküle waren in Richtung Mitte der Adhäsion am dichtesten gepackt. Sowohl die auf das Substrat ausgeübte Zugkraft als auch die molekulare Spannung an Vinculin stiegen jedoch zum äußeren, periphereren Ende hin an. Das deutet auf ein Ausgleichsspiel hin: In zentralen Regionen können viele Vinculinmoleküle die Last teilen, sodass jedes einzelne weniger Spannung spürt, während am äußeren Rand weniger Moleküle relativ mehr Kraft tragen und so starke lokale Zugkräfte unterstützen, ohne die Adhäsion zu zerstören.
Was das für Gesundheit und Krankheit bedeutet
Durch die Verschmelzung ganzer Zell‑Zugkarten mit proteinbasierten Spannungsmessungen bietet diese Studie ein multiskaliges Bild davon, wie Zellen ihren mechanischen Griff steuern. Die Arbeit zeigt, dass Zellen bei zunehmender Umgebungssteifigkeit sowohl stärker ziehen als auch ihre Vinculin‑Verbindungen stärker belasten, wobei die detaillierte Beziehung zwischen äußeren Kräften und molekularer Spannung jedoch von Adhäsion zu Adhäsion und von Zelle zu Zelle variiert. Gleichzeitig scheint ein robustes räumliches Muster der Kraftverteilung innerhalb einzelner Adhäsionen erhalten zu bleiben. Für Nicht‑Spezialisten lautet die Kernbotschaft: Zellen stimmen sehr genau ab, wo und wie sie ziehen, und verteilen Kräfte über viele kleine molekulare „Federn“, um sich an unterschiedliche mechanische Umgebungen anzupassen — ein Prinzip, das Prozessen von der Gewebeentwicklung über Fibrose bis hin zur Krebsinvasion zugrunde liegen könnte.
Zitation: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Schlüsselwörter: Zellmechanik, fokale Adhäsionen, Vinculin, Tractionskraft-Mikroskopie, Mechanotransduktion