Clear Sky Science · de
Zeitliche Dynamik der kollateralen RNA-Spaltung durch LbuCas13a in menschlichen Zellen
Aus einer bakteriellen Abwehr wird ein präziser Zell-Killer
Forscher haben eine Methode entdeckt, ein bakterielles Immunprotein in einen hochselektiven "Selbstzerstörungs"-Schalter für menschliche Zellen zu verwandeln. Durch Nutzung eines CRISPR-Enzyms namens LbuCas13a können sie eine gewählte RNA-Nachricht in einer Zelle erkennen und dann nahezu die gesamte übrige RNA dieser Zelle zerschreddern. Für Laien ist das interessant, weil RNA-Nachrichten steuern, welche Proteine eine Zelle herstellt; zu lernen, sie auf Abruf zu löschen, eröffnet Möglichkeiten für neue Krebstherapien, antivirale Strategien und leistungsfähige Forschungstools.
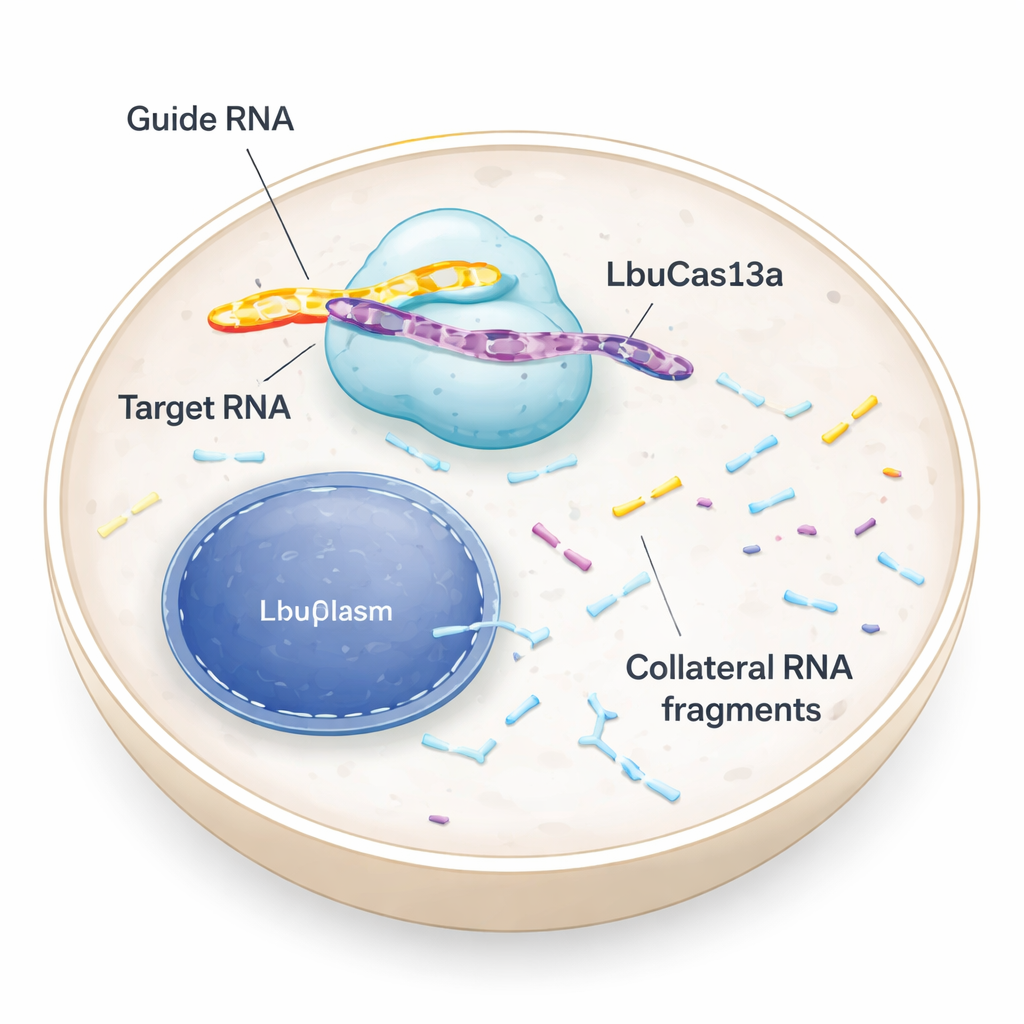
Eine molekulare Schere, die RNA statt DNA anvisiert
Die meisten haben von CRISPR-Werkzeugen gehört, die DNA schneiden und den genetischen Code umschreiben. LbuCas13a ist anders: es erkennt und schneidet RNA, die temporären Nachrichten, die Anweisungen von der DNA zu den Proteinfabriken der Zelle tragen. In Bakterien sind Cas13-Enzyme Teil einer antiviralen Abwehr. Sobald sie eine virale RNA entdecken, zerschneiden sie nicht nur den Eindringling, sondern beginnen auch, viele andere RNAs in der Nähe zu schneiden. Diese sogenannte "kollaterale" Aktivität kann infizierte Zellen in Dormanz oder Tod treiben und so die bakterielle Gemeinschaft schützen. Frühe Tests in Tier- und menschlichen Zellen deuteten darauf hin, dass Cas13s kollaterales Schneiden schwach oder nicht vorhanden sei, sodass das Enzym hauptsächlich als präziser RNA-"Ausschalter" verwendet wurde. Die neue Studie überprüft diese Annahme und zeigt, dass unter den richtigen Bedingungen die kollaterale Aktivität in menschlichen Zellen sowohl stark als auch nützlich sein kann.
Freisetzung kollateralem Schneidens in menschlichen Zellen
Das Team verglich mehrere Cas13-Varianten und stellte fest, dass LbuCas13a besonders wirksam war. Sie brachten gereinigtes LbuCas13a-Protein, das mit einer kurzen Leit-RNA vorgeladen war, direkt in menschliche Zellen ein — eine Form der molekularen "Protein-Injektion", genannt Ribonukleoprotein-(RNP-)Lieferung. Wenn die Leit-RNA auf eine Ziel-RNA passte — beispielsweise ein fluoreszierendes Markergen oder häufige natürliche Nachrichten wie GAPDH und 18S-rRNA — schnitt das Enzym zunächst dieses Ziel und begann dann, viele andere RNAs zu zerkauen. Innerhalb von etwa 50 Minuten veränderte sich das gesamte RNA-Profil der Zelle dramatisch, mit charakteristischen Spaltfragmenten. Dieser kollaterale Effekt wurde bei verschiedenen Liefermethoden und in einer Reihe von Zelltypen beobachtet, was zeigt, dass es kein Zufall einer einzelnen Zelllinie oder eines künstlichen Ziels war.
Von RNA-Zerstückelung zu Zellsterben und Selektion
Was geschieht mit einer Zelle, deren RNA-Nachrichten plötzlich verschwinden? Mit Live-Zell-Mikroskopie beobachteten die Forschenden, dass Zellen, die die Ziel-RNA exprimierten, allmählich in die Apoptose eintraten — eine ordentliche Form des programmierten Zelltods, gekennzeichnet durch charakteristische "Frühwarn"-Signale, bevor die Zelle auseinanderfällt. Wichtig ist, dass benachbarte Zellen, die die Ziel-RNA nicht exprimierten, weitgehend unbeeinflusst blieben, was zeigt, dass die Selbstzerstörung spezifisch ist. Die Gruppe nutzte diese Eigenschaft dann als Selektionswerkzeug. Als sie Ziel-tragende Zellen mit normalen Zellen mischten und LbuCas13a aktivierten, wurden die Ziel-tragenden Zellen über mehrere Tage selektiv dezimiert. Wiederholte Behandlungen senkten ihren Anteil noch weiter. Sie zeigten, dass sich dies zur Anreicherung erfolgreich geneditierter Zellen einsetzen lässt und auch feinabgestimmt Tumorzellen angreifen kann, die ein Onkogen wie CDK4 überproduzieren, während verwandte Zellen, die deutlich weniger von dieser RNA herstellen, verschont bleiben.
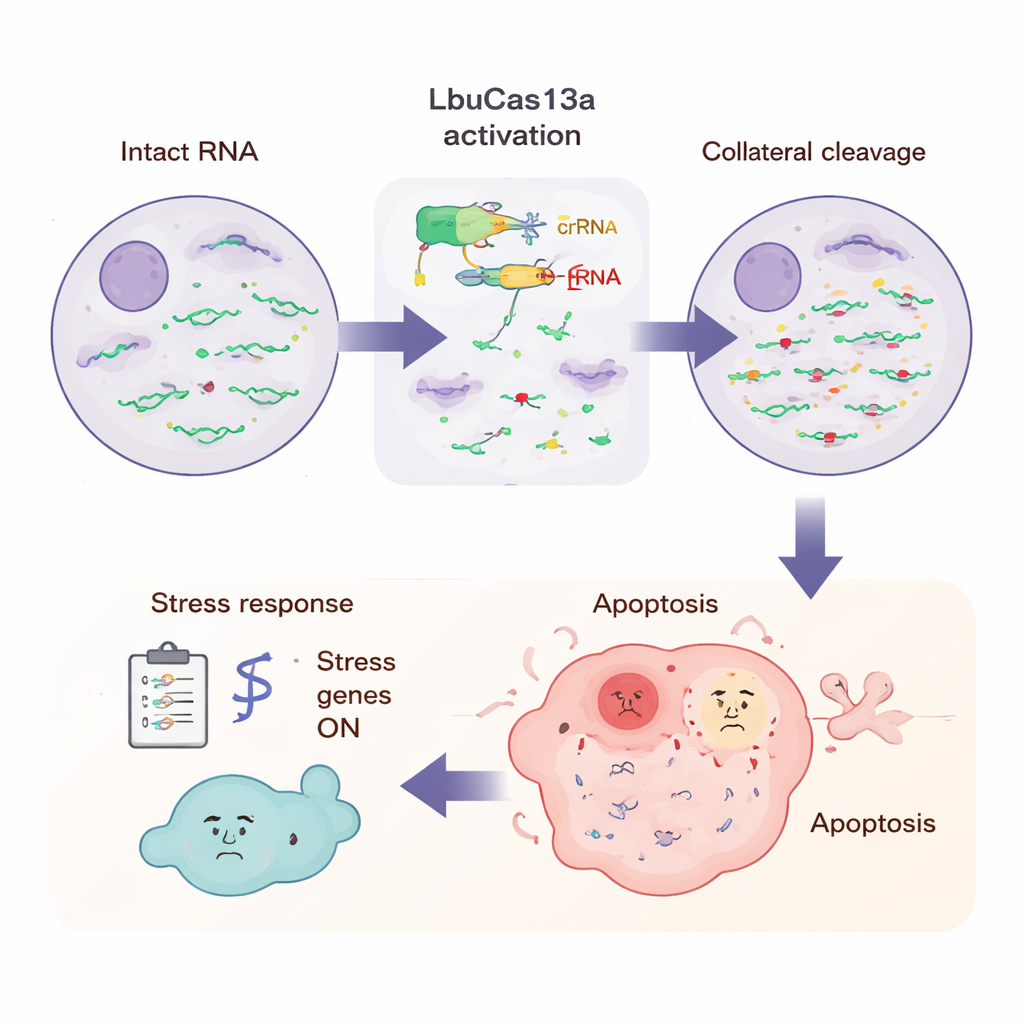
Was die Zelle während des Angriffs erlebt
Um das Gesamtbild zu sehen, maßen die Wissenschaftler alle RNAs in der Zelle zu mehreren Zeitpunkten nach LbuCas13a-Aktivierung. Durch das Zufügen bekannter RNA-Standards konnten sie feststellen, dass die meisten protein-codierenden RNAs im Zytoplasma innerhalb weniger Stunden um mehr als die Hälfte abnahmen, während bestimmte RNAs — wie mitochondriale Botschaften und einige nukleäre nichtkodierende RNAs — weitgehend verschont blieben. Langlese-Sequenzierung zeigte, dass Schnitte an wiederkehrenden, spezifischen Nukleotidpositionen auftraten, häufig in flexiblen Schleifenregionen der RNA, die reich an der Base Uracil sind, was Mustern entspricht, die in Reagenzglas-Experimenten gesehen wurden. Zu späteren Zeitpunkten wurden viele Stress- und angeborene Immungene hochreguliert, einschließlich solcher, die an Entzündungs-Signalen und antiviralen Abwehrreaktionen beteiligt sind. Dieses Muster legt nahe, dass die Zelle die plötzliche Flut gebrochener RNA-Enden ähnlich wahrnimmt wie eine Virusinfektion und ein Alarmprogramm auslöst, das in der Apoptose gipfelt.
Warum das wichtig ist und wohin es führen kann
Kurz gesagt zeigt die Studie, dass LbuCas13a in einen RNA-geführten "Tötungsschalter" für Zellen verwandelt werden kann: Wenn eine Zelle zu viel einer bestimmten RNA herstellt, führt die Aktivierung von LbuCas13a gegen diese RNA zu einem nahezu globalen RNA-Verlust, einem immunähnlichen Alarm und anschließend kontrolliertem Zellsterben. Da der Prozess stark von der Menge der Ziel-RNA abhängt, könnte er genutzt werden, um Zellen zu eliminieren, die schädliche Gene überexprimieren — etwa bestimmte Krebszellen — oder um unerwünschte Zellen in gemischten Kulturen bei Forschung oder Herstellung von Zelltherapien zu entfernen. Zugleich ist die Arbeit eine Mahnung: Auf RNA abzielende CRISPR-Werkzeuge können starke Nebeneffekte haben, die sorgfältig gesteuert werden müssen. Das Verständnis, wann und wie kollaterale RNA-Spaltung auftritt, ist entscheidend für den sicheren Einsatz von Cas13-Technologien in Medizin und Biotechnologie.
Zitation: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Schlüsselwörter: CRISPR-Cas13, RNA-Spaltung, Zellsterben, Krebsziel, Genbearbeitungswerkzeuge