Clear Sky Science · de
Modulation humaner Klasse-B1-GPCRs durch Plasma-Membranlipide
Fette, die die Empfänger unserer Zellen feinabstimmen
Unsere Zellen verlassen sich auf winzige Proteinantennen, sogenannte Rezeptoren, um Hormone und Neurotransmitter wahrzunehmen. Viele Blockbuster-Medikamente wirken, indem sie diese Rezeptoren ansteuern. Diese Studie zeigt, dass gewöhnliche Fette in der äußeren Schicht unserer Zellen weit mehr tun als nur als passiver Hintergrund zu dienen: Sie greifen direkt an und formen eine ganze Familie wichtiger Rezeptoren und steuern so subtil, wie Signale ein- oder ausgeschaltet werden. Das Verständnis dieser verborgenen Kontrollebene könnte helfen, klügere Medikamente mit weniger Nebenwirkungen zu entwickeln.
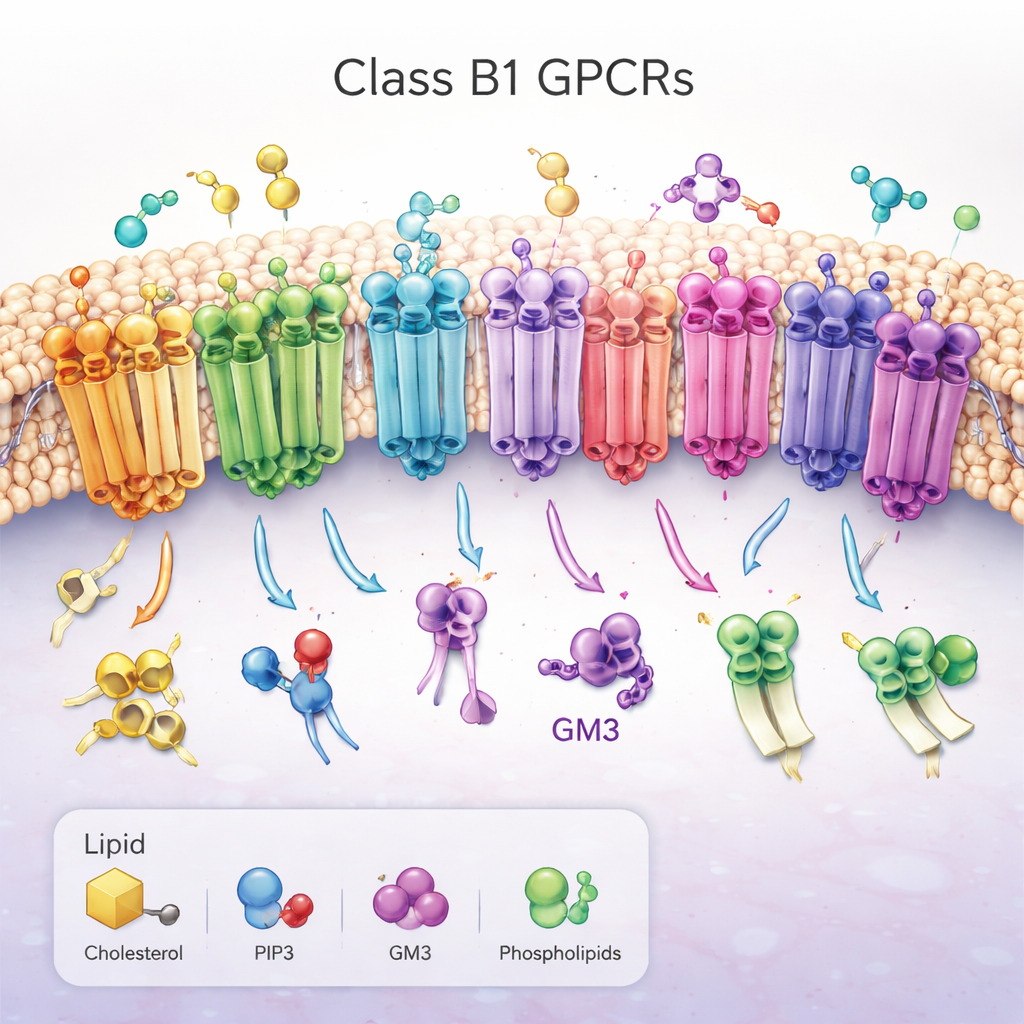
Eine Familie wichtiger molekularer Antennen
Die Arbeit konzentriert sich auf Klasse-B1-G-Protein-gekoppelte Rezeptoren (GPCRs), eine Gruppe von 15 eng verwandten Rezeptoren, die bei der Kontrolle von Blutzucker, Stoffwechsel, Wachstum und Stressreaktionen helfen. Sie sitzen in der äußeren Zellmembran, mit einem großen „Kopf“ außerhalb der Zelle, der hormonähnliche Moleküle bindet, und einem Bündel aus sieben Helices, das durch die fettige Membran reicht. Bei Aktivierung ändern diese Rezeptoren ihre Form auf der Innenseite der Zelle und öffnen eine Rinne, die Partnerproteine rekrutiert und Signalkaskaden auslöst. Wegen ihrer zentralen Rolle bei Krankheiten wie Diabetes und Adipositas sind Klasse-B1-GPCRs wichtige Arzneizielstrukturen; wie die umgebenden Membranlipide sie regulieren, war jedoch weitgehend rätselhaft.
Rezeptoren in ihrer natürlichen Nachbarschaft simulieren
Anstatt Rezeptoren in künstlichen Detergenzblasen zu untersuchen, setzten die Forschenden alle 15 humanen Klasse-B1-GPCRs in computergestützte Membranen ein, die das komplexe Gemisch von Fetten in echten Zellen nachbilden. Mithilfe einer Technik namens grobkörnige Molekulardynamik führten sie mehrere lange Simulationen jedes Rezeptors in sowohl aktivem als auch inaktivem Zustand durch, insgesamt etwa eine Millisekunde simulierter Zeit. Sie verfolgten, wie drei „regulierende“ Lipide — Cholesterin, das Signallipid PIP2 und das zuckerverzierte Fett GM3 — sich Regionen der einzelnen Rezeptoren näherten, anbanden und wieder losließen. Damit andere diese umfangreichen Daten reproduzieren und weiter darauf aufbauen können, dokumentierten sie jeden Schritt der Einrichtung und Analyse mit einem offenen Workflow-Tool namens aiida-gromacs und verglichen ihre physikbasierten Ergebnisse mit Vorhersagen eines neuen KI-Modells (Chai‑1), das abschätzt, wie Proteine kleine Moleküle binden.
Verborgene Taschen und ein konservierter Lipidgriff
Die Simulationen legten wiederkehrende Bindungsmuster über die gesamte Rezeptorfamilie offen. Cholesterin, bekannt aus Ernährungsdiskussionen, wurde nicht nur in einer zuvor bekannten Stelle einer Helix gesehen, sondern auch in „tiefen Membran“-Taschen zwischen Helices, wobei sein polarer Kopf ungewöhnlich weit in die Membran eingesenkt war. Ein Rezeptor, der Secretin-Rezeptor, zeigte besonders langlebige Cholesterinbindung in unterschiedlichen Taschen in seiner aktiven und inaktiven Form, was darauf hindeutet, dass Cholesterin dessen Signalgebung stark beeinflussen könnte. PIP2 zeigte ein auffallend konserviertes Verhalten: Es gruppierte sich an der inneren Fläche der Rezeptoren an der Kreuzung von zwei Helices und einem kurzen Schwanzsegment (TM6, TM7 und H8), insbesondere wenn die Rezeptoren im aktiven Zustand waren. An dieser Stelle griffen Netzwerke positiv geladener Aminosäuren das negativ geladene PIP2-Kopfgruppen, was nahelegt, dass dieses Lipid die aktive Form stabilisieren oder bei der Rekrutierung von Signalkomponenten auf der Innenseite der Zelle helfen könnte.
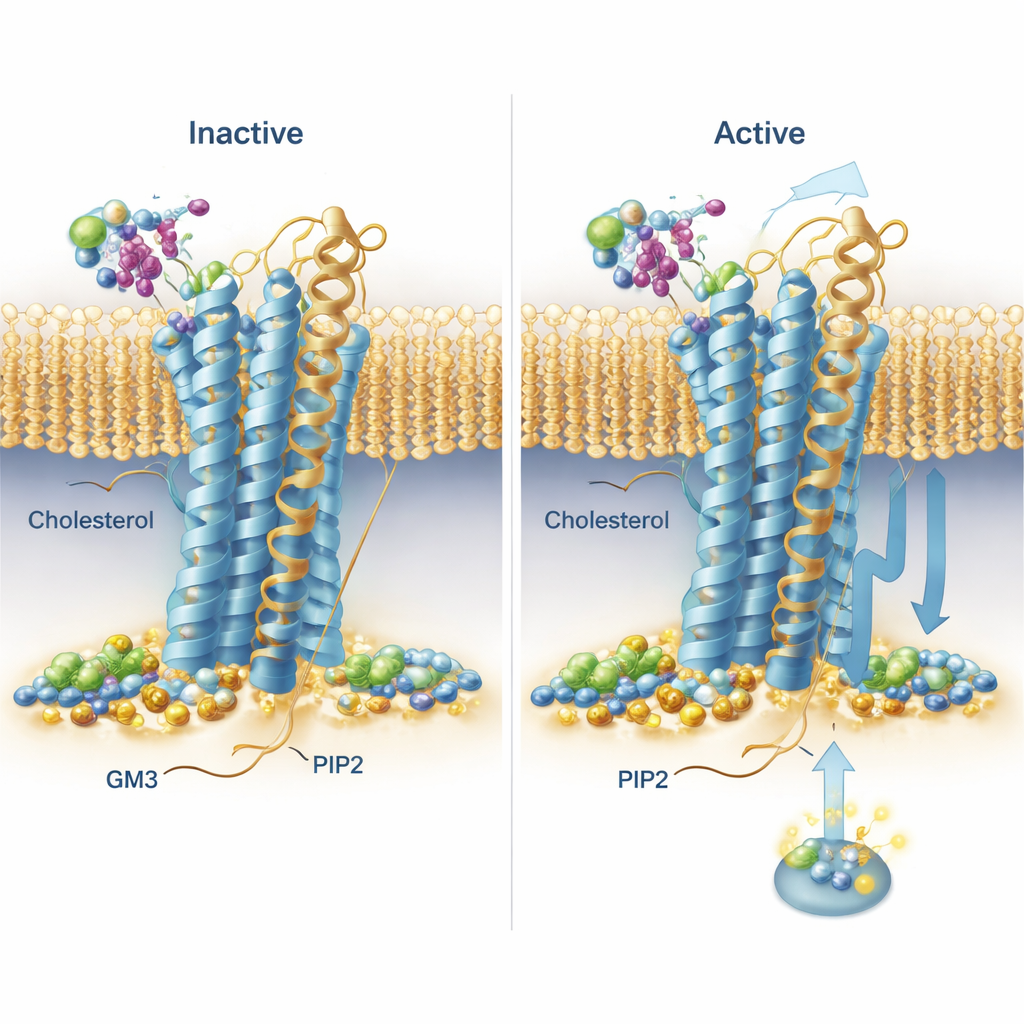
Ein zuckerbeschichtetes Lipid, das Rezeptorbewegung beeinflusst
GM3, ein komplexes Lipid mit einem Zucker-Kopf, wechselwirkte überwiegend mit den großen äußeren Köpfen der Rezeptoren. Das Team beobachtete, dass sich die äußeren Domänen mancher Rezeptoren gegenüber der Membran stark schwenkten und bogen, während andere stärker eingeschränkt waren. Für zwei medizinalrelevante Rezeptoren — GLP‑1R und GIPR — untersuchten sie GM3s Rolle im Detail. In Simulationen mit GM3 lag das Lipid entweder am Ansatz der äußeren Domäne und der Ligandenbindetasche (GLP‑1R) an oder heftete sich an die entfernte Spitze der äußeren Domäne (GIPR) und beeinflusste in beiden Fällen, wie frei diese Domänen sich bewegen konnten. Um diese Vorhersagen in lebenden Zellen zu testen, nutzten die Forschenden eine lichtbasierte Technik (TR‑FRET), die anzeigt, wie nah ein markierter Rezeptorkopf an der Membran ist. Als sie die GM3-Spiegel mit einem kleinen molekularen Inhibitor reduzierten, sahen sie messbare Veränderungen darin, wie sich die Rezeptorköpfe bei Stimulation verschoben — im Großen und Ganzen konsistent mit der Idee, dass GM3 die Rezeptorflexibilität rezeptor- und zustandsspezifisch abstimmt.
Warum diese Lipid–Rezeptor-Partnerschaften wichtig sind
Insgesamt zeichnet die Studie das Bild von Klasse-B1-GPCRs nicht nur als Hormonschalter, sondern als Teil eines eng choreografierten Zusammenspiels mit umgebenden Lipiden. Cholesterin kann verborgene Taschen besetzen und bestimmte Signalausgänge subtil bevorzugen, PIP2 bildet einen konservierten inneren „Henkel“, der Rezeptoren in ihre aktive Form verriegeln und Partnerproteine führen könnte, und GM3 beeinflusst, wie die äußeren Bereiche der Rezeptoren sich bewegen und ihre Liganden treffen. Für Laien ist die Kernaussage: Die Membran ist eine aktive Regulierungsebene — kleine Unterschiede in der Lipidzusammensetzung können verändern, wie derselbe Rezeptor in verschiedenen Geweben oder Krankheitszuständen reagiert. Indem diese Wechselwirkungen detailliert kartiert und die zugrunde liegenden Simulationsdaten geteilt werden, legt diese Arbeit eine Grundlage dafür, künftig Medikamente zu entwerfen, die bestimmte Lipidkontakte ausnutzen oder vermeiden, und so Behandlungen selektiver und wirksamer machen könnten.
Zitation: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
Schlüsselwörter: G-Protein-gekoppelte Rezeptoren, Membranlipide, Cholesterin, PIP2, GM3