Clear Sky Science · de
Strukturelle Einblicke in den Transport von Metallclustern im Assemblierungsgerüst NifEN der Nitrogenase
Wie die Natur ein mächtiges chemisches Werkzeug baut
Stickstoff umgibt uns in der Luft, aber die meisten Lebewesen können ihn in dieser Form nicht nutzen. Ein spezielles Enzym, die Nitrogenase, löst dieses Problem, indem es atmosphärischen Stickstoff in Ammoniak umwandelt — eine zentrale Verbindung für Leben und Dünger. Im Zentrum der Nitrogenase sitzt ein dichter Metall‑„Cluster“, der die eigentliche Chemie ausführt, doch wie Zellen dieses komplexe Gebilde zusammenbauen, blieb lange unklar. Diese Arbeit gewährt Einblick in diesen Konstruktionsprozess und zeigt, wie ein Protein‑Gerüst namens NifEN als flexible Verladestation und Förderweg für die Metallfracht des Clusters dient.
Eine molekulare Fabrik hinter Dünger und Treibstoffen
Die Nitrogenase ist die natürliche Entsprechung industrieller Prozesse zur Herstellung von Ammoniak und flüssigen Brennstoffen. Anstatt riesiger Reaktoren verwenden Mikroben eine kompakte Proteinfabrik, angetrieben durch zelluläre Energie. Ihre Leistungsfähigkeit hängt von einem außergewöhnlich komplexen Metallzentrum ab, aufgebaut aus Eisen, Schwefel, Molybdän, Kohlenstoff und einer organischen Seitenkette. Der Zusammenbau dieses Kerns ist zu empfindlich, um dem Zufall überlassen zu werden, daher setzen Zellen ein Staffelspiel von Hilfsproteinen ein. Eines der wichtigsten ist NifEN: Es empfängt ein nahezu fertiges All‑Eisen‑Vorläufercluster (L‑Cluster), hilft dessen Umwandlung in die reife Form (M‑Cluster) und übergibt es anschließend an die arbeitende Nitrogenase. Zu verstehen, wie NifEN diesen Verkehr steuert, könnte helfen, Mikroben für sauberere Düngerproduktion oder neue kohlenstoffbasierte Brennstoffe zu entwickeln.
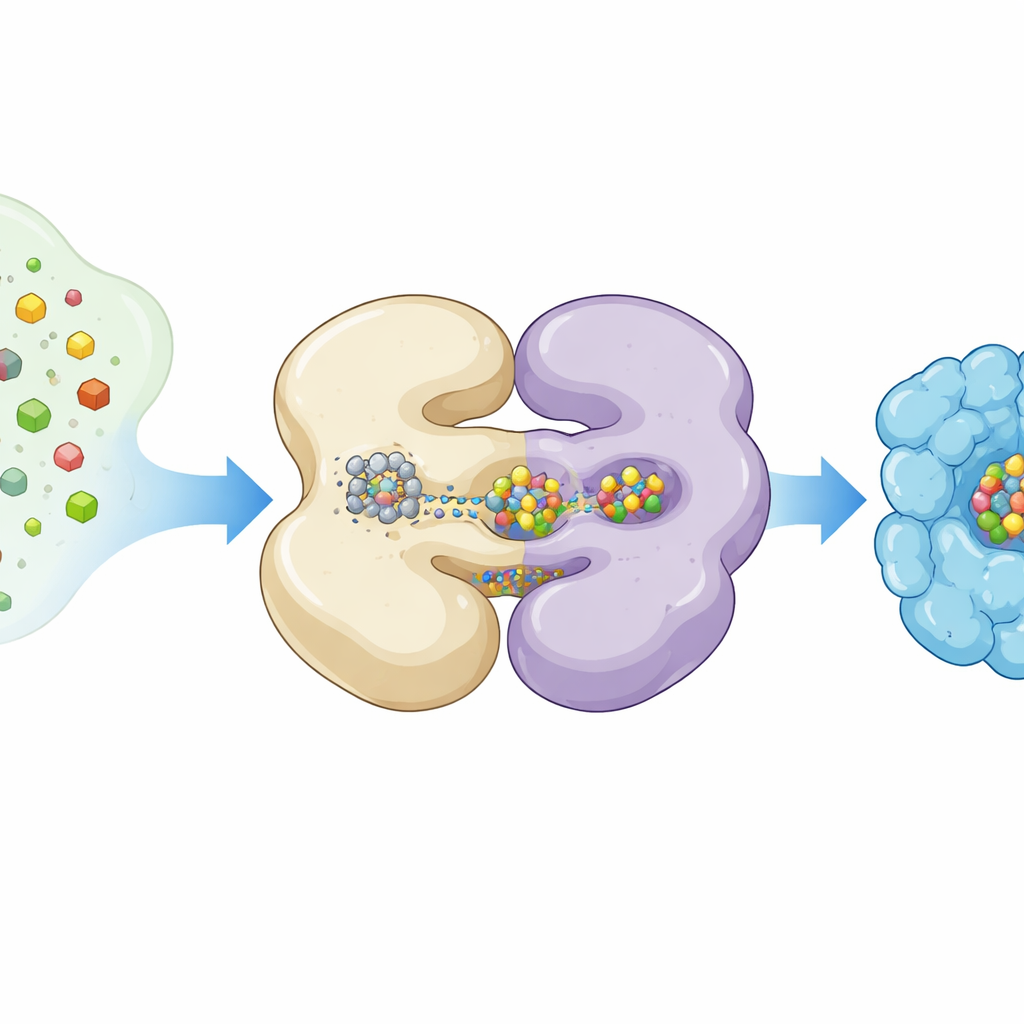
Eine bewegte Maschine mit eingefrorenen Momentaufnahmen sehen
Die Autoren nutzten kryogene Elektronenmikroskopie, eine Technik, die Proteine bei extrem niedrigen Temperaturen abbildet, um NifEN in verschiedenen Arbeitsstellungen einzufangen. Sie exprimierten NifEN in Laborbakterien so, dass einige Proteinkopien ein L‑Cluster trugen, andere leer waren. Durch Sortieren von Millionen Einzelpartikelbildern rekonstruierten sie zwei Hauptformen: eine „apo“‑Form ohne das bewegliche Cluster und eine „holo“‑Form mit dem Cluster an einer internen Bindestelle. Beide Formen teilen einen Kern aus vier Untereinheiten, angeordnet als zwei Paare, doch wenn das L‑Cluster vorhanden ist, wird eine Hälfte von NifEN deutlich geordneter und mehrere Helices schwenken nach innen und schließen sich um die Metallladung.
Ein verborgener Tunnel für Metallfracht
Der Vergleich der leeren und beladenen Strukturen offenbarte ein auffälliges Merkmal: ein langer Tunnel, der durch das NifEN‑Dimer führt. Im leeren Zustand ist diese Passage breit und offen; nach der Clusterbindung verengt sie sich, während das Protein seine Ladung umklammert. Frühere Kristallstrukturen hatten eine alternative „äußere“ Position des L‑Clusters nahe der Proteinoberfläche gezeigt. Zusammengenommen deuteten die Forscher darauf hin, dass das Cluster mindestens zwei Stationen auf NifEN einnehmen kann — eine im Inneren verborgen und eine exponierte — und sich entlang eines gekrümmten Pfads bewegt, der von Verschiebungen einer flexiblen Domäne gated wird. Diese Bewegung scheint entspannter zu sein als in der finalen Nitrogenase, deren aktiver Cluster starr an Ort und Stelle gehalten wird; das legt nahe, dass NifEN eher für die Übergabe als für langfristige Katalyse ausgelegt ist.
Andockpartner und eine durchgehende Route
Um zu verstehen, wie NifEN mit seinen vorgelagerten und nachgelagerten Partnern verbunden ist, kombinierten die Forscher ihre experimentellen Strukturen mit AlphaFold‑3‑Modellen und niedrigauflösender Elektronenmikroskopie von Proteinkomplexen. Die Modelle legen nahe, dass das Enzym NifB, das das L‑Cluster aus kleineren Eisen‑Schwefel‑Bausteinen herstellt, in einem Tal auf einer Fläche von NifEN andockt. Von dort lässt sich ein durchgehender Tunnel vom Metallzentrum von NifB direkt in den NifEN‑Tunnel und weiter zur internen L‑Cluster‑Station verfolgen. Auf der gegenüberliegenden Fläche von NifEN bietet eine andere Andockstelle Platz für NifH, das Protein, das Molybdän und eine organische Seitenkette einbaut, um den Kofaktor zu vervollständigen. In dieser Konfiguration sitzt das L‑Cluster an der Oberflächenstelle, ideal positioniert für die Modifikation. Mutationen wichtiger Aminosäuren, die die vorgeschlagene Route auskleiden, stören das Laden, die Bewegung oder die Reifung des Clusters und liefern experimentelle Unterstützung für dieses Förderband‑Modell.
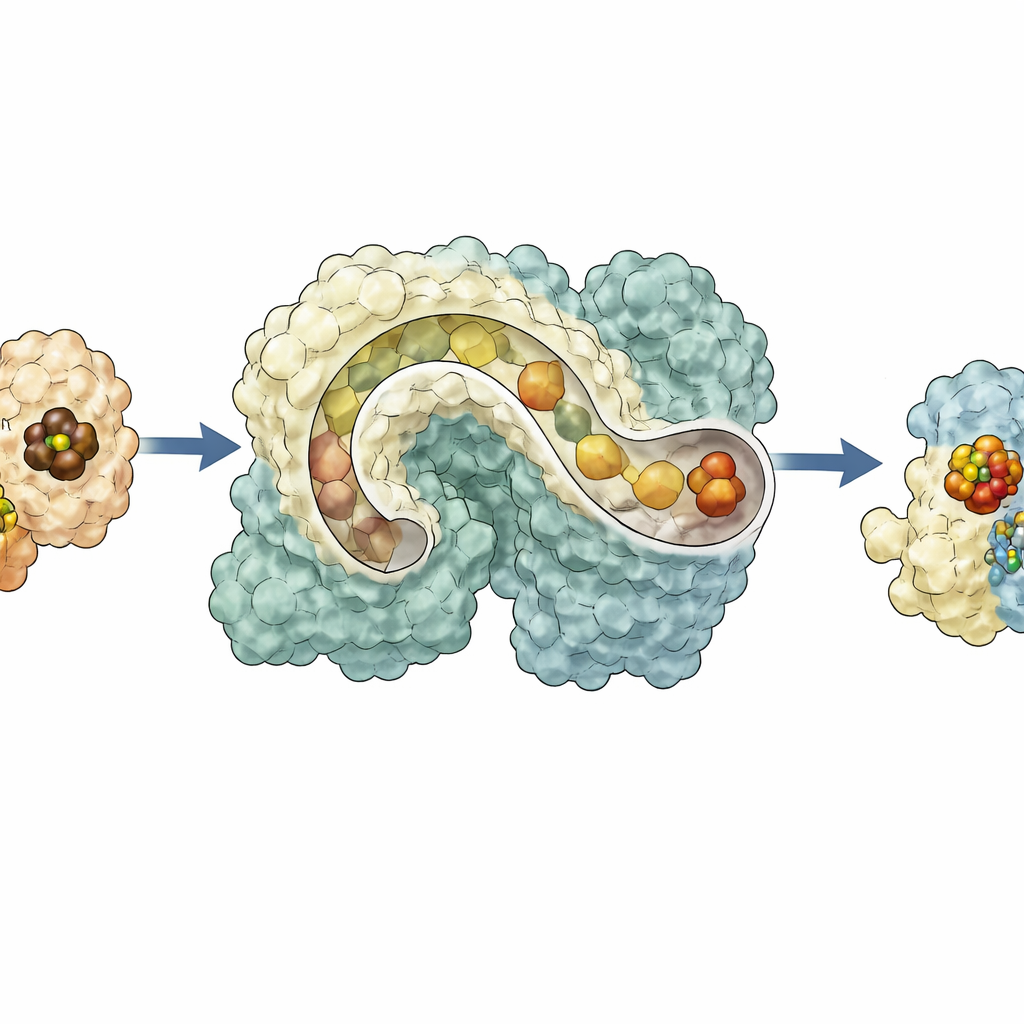
Warum ein flexibles Gerüst wichtig ist
In der Summe zeichnen die Ergebnisse NifEN als ein dynamisches Zentrum, das einen Metallkern von NifB auf der einen Seite empfängt, ihn in eine innere Haltebucht verschiebt, ihn dann auf der gegenüberliegenden Oberfläche zur Fertigstellung durch NifH präsentiert und den reifen Cluster anschließend wieder nach innen führt, um ihn an die Nitrogenase zu übergeben. Dieses durch Konformationsänderungen gesteuerte Transportschema erklärt, wie mehrere empfindliche Schritte innerhalb eines einzigen Proteinrahmens koordiniert werden können, und deutet darauf hin, wie frühe Enzyme sich von flexibleren Gerüsten zu den heute hochspezialisierten Katalysatoren entwickelt haben könnten. Für Nicht‑Spezialisten zeigt die Arbeit, dass die Natur selbst auf der Nanoskala auf Fließbänder, Tunnel und bewegliche Teile setzt, um die molekularen Werkzeuge zu bauen, die die globalen Stickstoffkreisläufe, die Lebensmittelproduktion und womöglich künftige grüne Technologien antreiben.
Zitation: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Schlüsselwörter: Nitrogenase, Assemblierung von Metallclustern, NifEN-Gerüst, kryo‑Elektronenmikroskopie, biologische Stickstofffixierung