Clear Sky Science · de
Aufdeckung aktiver Stellen und die kooperative Rolle von Nicht-Gleichgewichtsplasma und Kupfer‑Zink‑Katalysatoren bei der Hydrierung von CO2 zu Methanol
Klimagefährdendes Gas in eine nützliche Flüssigkeit verwandeln
Das Verbrennen von Kohle, Öl und Gas setzt Kohlendioxid (CO2) frei, das wichtigste Treibhausgas, das den Klimawandel antreibt. Was wäre, wenn wir dieses CO2 nicht nur erfassen, sondern auch in etwas Nützliches verwandeln könnten — etwa in Methanol, eine Flüssigkeit, die als Brennstoff, als Baustein für Kunststoffe und zur Speicherung erneuerbarer Energie dienen kann? In dieser Studie wird ein vielversprechender Ansatz untersucht, der elektrische Entladungen, sogenannte nicht-thermische Plasmen, zusammen mit Kupfer‑Zink‑Katalysatoren nutzt, um CO2 effizienter und unter milderen Bedingungen als in heutigen Chemieanlagen in Methanol umzuwandeln.
Eine neue Art, chemische Reaktionen zu treiben
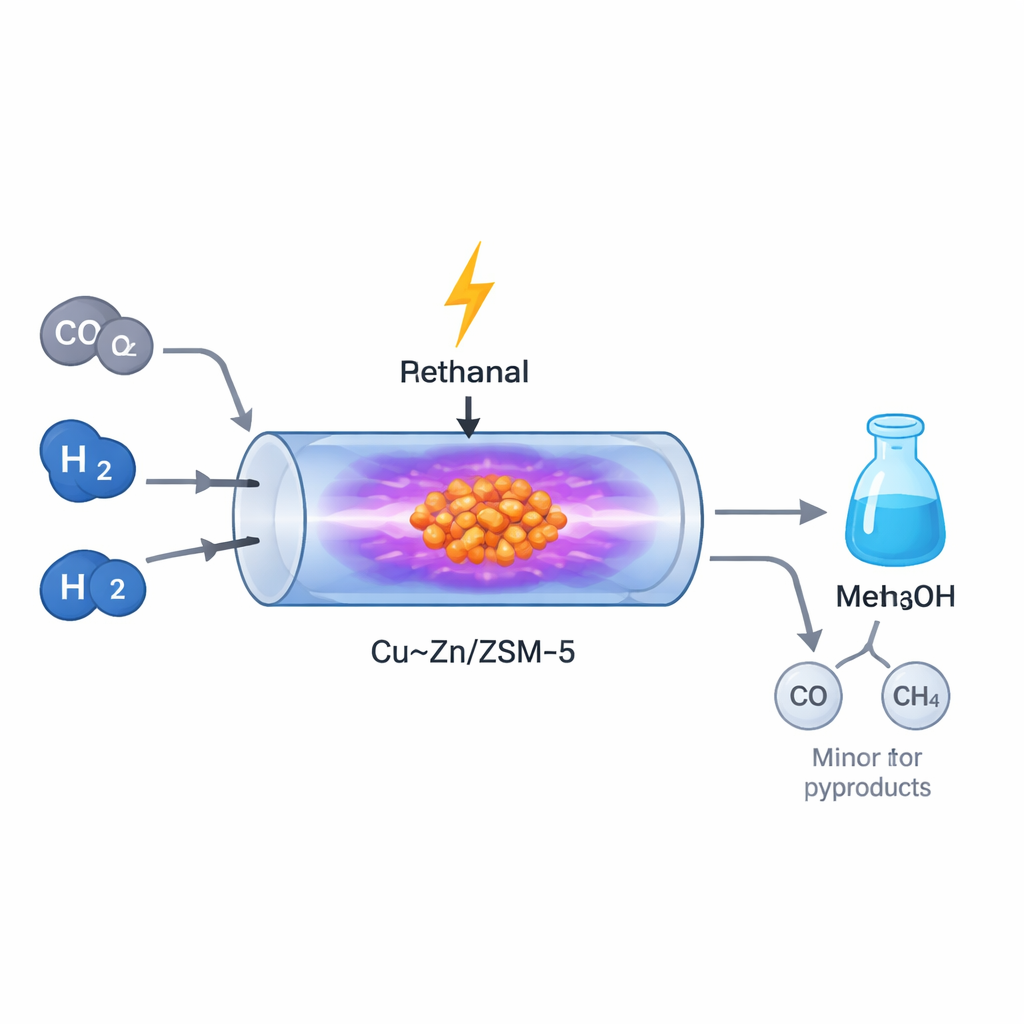
Konventionelle Methanolanlagen arbeiten bei hohen Temperaturen und Drücken, was viel Energie erfordert und große, zentralisierte Anlagen nötig macht. Im Gegensatz dazu nutzt das nicht-thermische Plasma starke elektrische Felder, um Gasmoleküle zu energisieren, ohne alles aufzuheizen. In dieser Arbeit führten die Forschenden ein Gemisch aus CO2 und Wasserstoff in einen kleinen Plasmareaktor, der mit einem speziell gestalteten Kupfer‑Zink‑Katalysator auf dem porösen Mineral ZSM‑5 gefüllt war. Das Plasma erzeugte eine Vielzahl angeregter und fragmentierter Gasarten, die mit der Katalysatoroberfläche wechselwirkten und so die Bildung von Methanol bei etwa Atmosphärendruck und vergleichsweise niedrigen Bulk‑Temperaturen ermöglichten. Dadurch eignet sich das Verfahren potenziell gut für flexible, mit erneuerbarer Energie betriebene „Mikro‑Anlagen“, die nahe an CO2‑Quellen platziert werden können.
Warum Kupfer und Zink ein starkes Team bilden
Kupferbasierte Katalysatoren werden bereits kommerziell genutzt, um Synthesegas (ein Gemisch aus Kohlenmonoxid, CO, und Wasserstoff) in Methanol umzuwandeln. Unter Plasmabedingungen mit CO2 als Ausgangsstoff schnitt jedoch ein standardmäßiger industrieller Kupfer‑Zink‑Alumina‑Katalysator schlecht ab und wandelte nur einen kleinen Bruchteil des CO2 um. Die Forschenden gestalteten das Material daher neu: Sie hielten die Kupferladung auf einem niedrigen Niveau konstant und variierten systematisch die Menge an Zink auf der ZSM‑5‑Trägersubstanz. Sie fanden, dass eine bestimmte Zusammensetzung, bezeichnet als 2Cu2Zn, das richtige Gleichgewicht traf. Unter nicht-thermischem Plasma erreichte dieser Katalysator CO2‑Umwandlungen von etwa 14–15 %, eine Methanolselektivität nahe 37 % und eine Methanolproduktionsrate, die mehrere Male höher lag als bei reinem Kupfer oder reinem Zink. Wichtig ist, dass diese Verbesserungen bei deutlich milderen Bedingungen als in konventionellen thermischen Prozessen erzielt wurden.
Den Katalysator während des Betriebs beobachten
Um zu verstehen, warum das Kupfer‑Zink‑Paar so gut funktionierte, nutzte das Team eine Reihe fortschrittlicher Methoden, während die Reaktion tatsächlich lief. Röntgenabsorptionsmethoden zeigten, dass Zugabe von Zink half, Kupfer in kleinere, gleichmäßiger verteilte Partikel aufzubrechen und das Kupfer leichter in seiner metallischen, aktiven Form zu erhalten. Gleichzeitig blieb Zink in oxidierter Form und bildete eine enge Grenzfläche mit Kupfer, anstatt sich zu einer echten Legierung zu vermischen. Infrarotspektroskopie mit adsorbiertem Kohlenmonoxid zeigte, dass diese Kupfer‑Zink‑Oxid‑Schnittstellen spezielle Stellen erzeugen, die CO anders binden als reines Kupfer. Unter Plasmabestrahlung konnten diese interfacialen Stellen Reaktionszwischenprodukte stabilisieren, die wichtige Zwischenschritte auf dem Weg zu Methanol sind, während die Gesamtstruktur über viele Stunden hinweg dem Verklumpen und der Reoxidation widerstandsfähig blieb.
Zwei Pfade, die Hand in Hand wirken
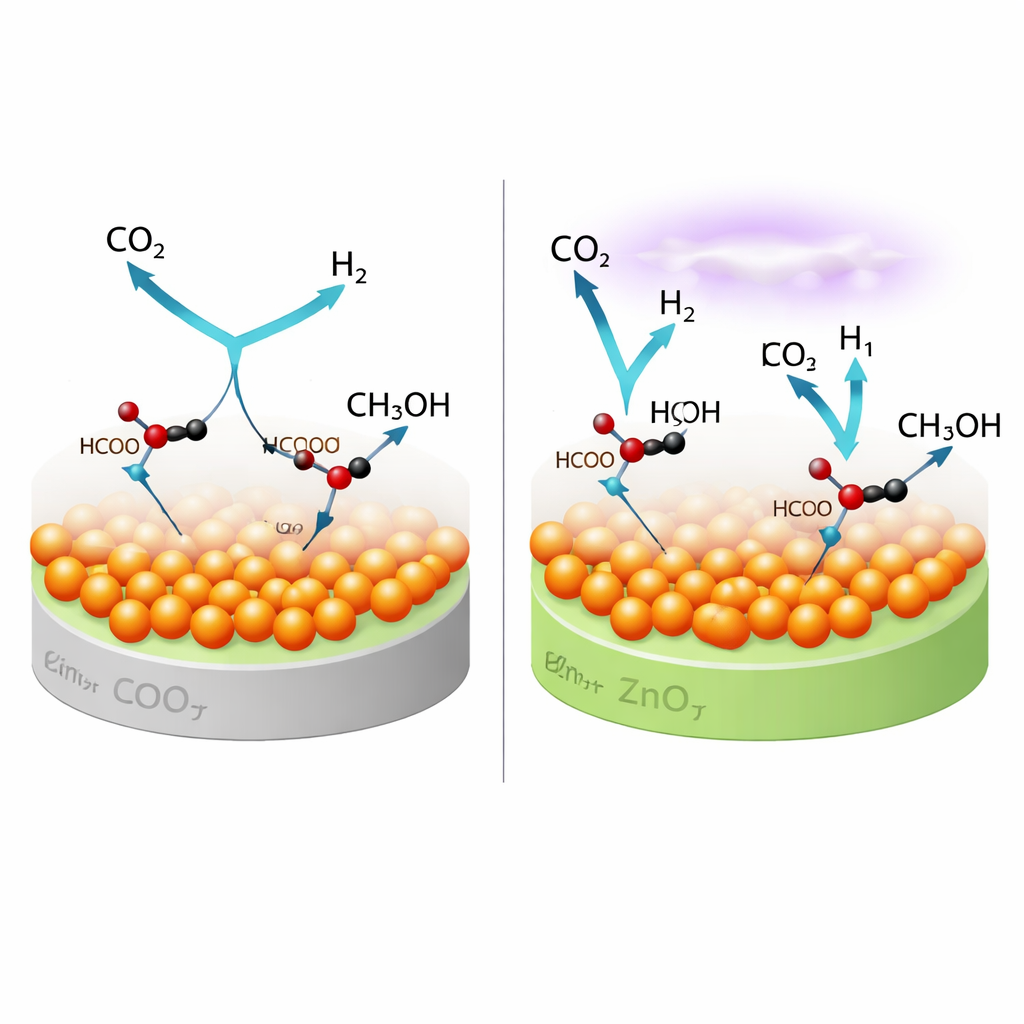
Die Studie ging auch einer zentralen Frage nach: Welche molekularen Routen führen unter Plasmabedingungen tatsächlich von CO2 zu Methanol? Operando‑Infrarotmessungen in Kombination mit Massenspektrometrie zeigten, dass die Reaktion auf reinem Kupfer hauptsächlich über einen „Formiat“-Pfad verläuft, bei dem sich CO2 zuerst an die Oberfläche anlagert und schrittweise hydriert wird. Auf dem optimierten Kupfer‑Zink‑Katalysator öffnet sich ein zweiter Pfad. Hier spaltet das Plasma teilweise CO2 in der Gasphase zu CO, das dann an der Kupfer‑Zink‑Oxid‑Grenzfläche landet und weiter über ein „Formyl“‑Zwischenprodukt hydriert wird, bevor es zu Methanol wird. Weil das Plasma kontinuierlich sowohl CO als auch reaktive, wasserstoffhaltige Spezies erzeugt, können diese beiden Wege nebeneinander ablaufen und die Gesamtmethanolausbeute steigern.
Was das für zukünftige Kraftstoffe bedeutet
Vereinfacht sagt diese Arbeit: Sorgfältig konstruierte Kupfer‑Zink‑Katalysatoren können in Kombination mit elektrisch betriebenen Plasmen Abfall‑CO2 effizienter und schonender in nützliches Methanol verwandeln als traditionelle, wärmebasierte Verfahren. Das Plasma liefert hochreaktive CO2‑ und Wasserstofffragmentspezies, während die Kupfer‑Zink‑Grenzfläche des Katalysators die passenden „Landeplätze“ bietet, um diese Fragmente entlang effizienter Reaktionspfade zu führen. Da der Prozess bei niedrigem Druck und vergleichsweise niedriger Temperatur läuft, ließe er sich mit intermittierender erneuerbarer Energie und modularen Reaktoren in der Nähe von CO2‑Quellen koppeln. Zwar ist noch viel Engineering nötig, bevor solche Systeme in großem Maßstab einsetzbar sind, doch die Studie liefert eine klare mechanistische Blaupause für die Gestaltung der nächsten Generation elektrifizierter Reaktoren, die dabei helfen, den Kohlenstoffkreislauf zu schließen.
Zitation: Xu, S., Potter, M.E., Simancas, R. et al. Unveiling active sites and the cooperative role of non-thermal plasma and copper–zinc catalysts in the hydrogenation of CO2 to methanol. Nat Catal 9, 134–147 (2026). https://doi.org/10.1038/s41929-025-01477-5
Schlüsselwörter: CO2-zu-Methanol, Nicht‑thermische Plasmakatalyse, Kupfer‑Zink‑Katalysatoren, Kohlenstoffrecycling, elektrifizierte chemische Prozesse