Clear Sky Science · de
Kombination aus föderiertem Lernen und reisendem Modell steigert Leistung und eröffnet Chancen für digitale Gesundheitgerechtigkeit
Warum es wichtig ist, medizinische Erkenntnisse zu teilen, ohne Daten weiterzugeben
Die moderne Medizin verlässt sich zunehmend auf künstliche Intelligenz, um Muster in Scans und Gesundheitsakten zu erkennen. Patientendaten sind jedoch sensibel und dürfen oft das Krankenhaus, in dem sie erhoben wurden, nicht verlassen. Daraus entsteht ein Dilemma: Wie können Krankenhäuser weltweit zusammenarbeiten, um leistungsfähige KI-Werkzeuge zu trainieren, ohne rohe Patientendaten über Grenzen hinweg oder in große zentrale Server zu schicken? Diese Studie stellt einen neuen Ansatz vor, der genau das ermöglicht und dabei nicht nur auf Genauigkeit abzielt, sondern auch auf Fairness zwischen gut ausgestatteten Krankenhäusern und kleineren, ressourcenärmeren Kliniken.
Zwei Wege, eine KI zu trainieren, ohne Daten zu verschieben
Heute erlauben zwei Hauptstrategien Krankenhäusern, gemeinsam KI zu trainieren und gleichzeitig Daten vor Ort zu belassen. Beim föderierten Lernen trainiert jedes Krankenhaus parallel eine lokale Kopie eines Modells; diese lokalen Modelle werden anschließend auf einem zentralen Server zu einem gemeinsamen "Globalmodell" zusammengeführt. Beim reisenden Modell hingegen gibt es nur ein Modell, das von Krankenhaus zu Krankenhaus wandert und nacheinander an jedem Standort trainiert wird. Beide Methoden schützen die Privatsphäre, haben aber jeweils Nachteile. Föderiertes Lernen kann Probleme bekommen, wenn einige Krankenhäuser sehr wenige Daten haben oder nicht alle Patientengruppen vertreten sind; das Zusammenführen schwacher oder unausgewogener lokaler Modelle kann zu einem schlechten Globalmodell führen, das vor allem große, wohlhabende Standorte widerspiegelt. Das reisende Modell ist robuster gegenüber solchen Ungleichgewichten, kann aber langsamer und schwieriger zu verwalten sein.
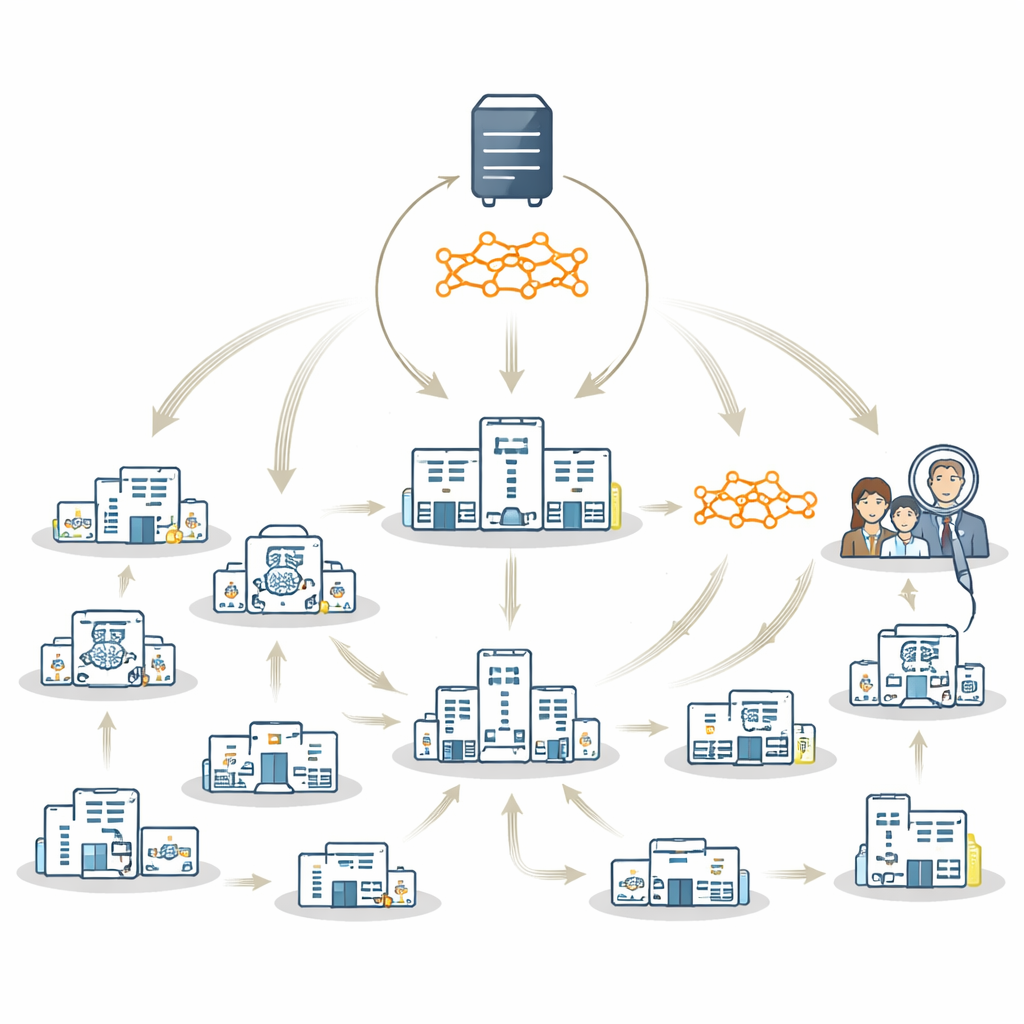
Eine Hybridstrategie, die das Beste aus beiden Welten nutzt
Die Autorinnen und Autoren schlagen FedTM vor, ein hybrides Trainingsschema, das die Stärken von föderiertem Lernen und dem reisenden Modell vereint. Das Training läuft in zwei Phasen ab. Zuerst gibt es eine "Aufwärmphase", in der nur die größten Krankenhäuser mit vollständigeren und ausgewogeneren Datensätzen parallel nach den üblichen föderierten Lernverfahren das Modell trainieren. Das erzeugt ein leistungsfähiges Ausgangsmodell. Danach folgt eine "Feinabstimmungsphase", in der dieses aufgeheizte Modell nacheinander jeden Standort besucht, einschließlich sehr kleiner Kliniken, die möglicherweise nur wenige Hirnscans oder sogar nur einen Patienten haben. In dieser zweiten Phase wird das Modell schrittweise aktualisiert, während es reist, und nimmt dabei Wissen aus jedem Standort auf, ohne dass deren Daten jemals den lokalen Kontrollbereich verlassen müssen.
Test des Verfahrens an Hirnscans von Parkinson-Patienten
Um FedTM zu prüfen, nutzten die Forschenden 1.817 Hirn-MRT-Scans von 83 Bildgebungsstandorten weltweit, um ein KI-System zu trainieren, das Menschen mit Parkinson-Krankheit von gesunden Personen unterscheidet. Das ist ein besonders anspruchsvolles Szenario: Mehr als die Hälfte der Standorte lieferte weniger als zehn Scans, nur etwa ein Drittel hatte sowohl Patientendaten als auch Kontrolldaten, und die Scanning-Protokolle variierten stark. Unter diesen realen Bedingungen konnte reines föderiertes Lernen die Aufgabe nicht gut erlernen, während ein reines reisendes Modell besser abschnitt, aber noch Verbesserungsspielraum ließ. FedTM, besonders wenn das Aufwärmen die sieben größten und ausgeglichensten Standorte einbezog, übertraf beide Ansätze deutlich: Die Fläche unter der ROC-Kurve, ein Standardmaß für Klassifikationsqualität, stieg von 77 % beim rein reisenden Modell auf etwa 82 % mit FedTM, mit ähnlichen Verbesserungen bei anderen klinisch wichtigen Metriken wie Sensitivität, Spezifität und F1-Score.
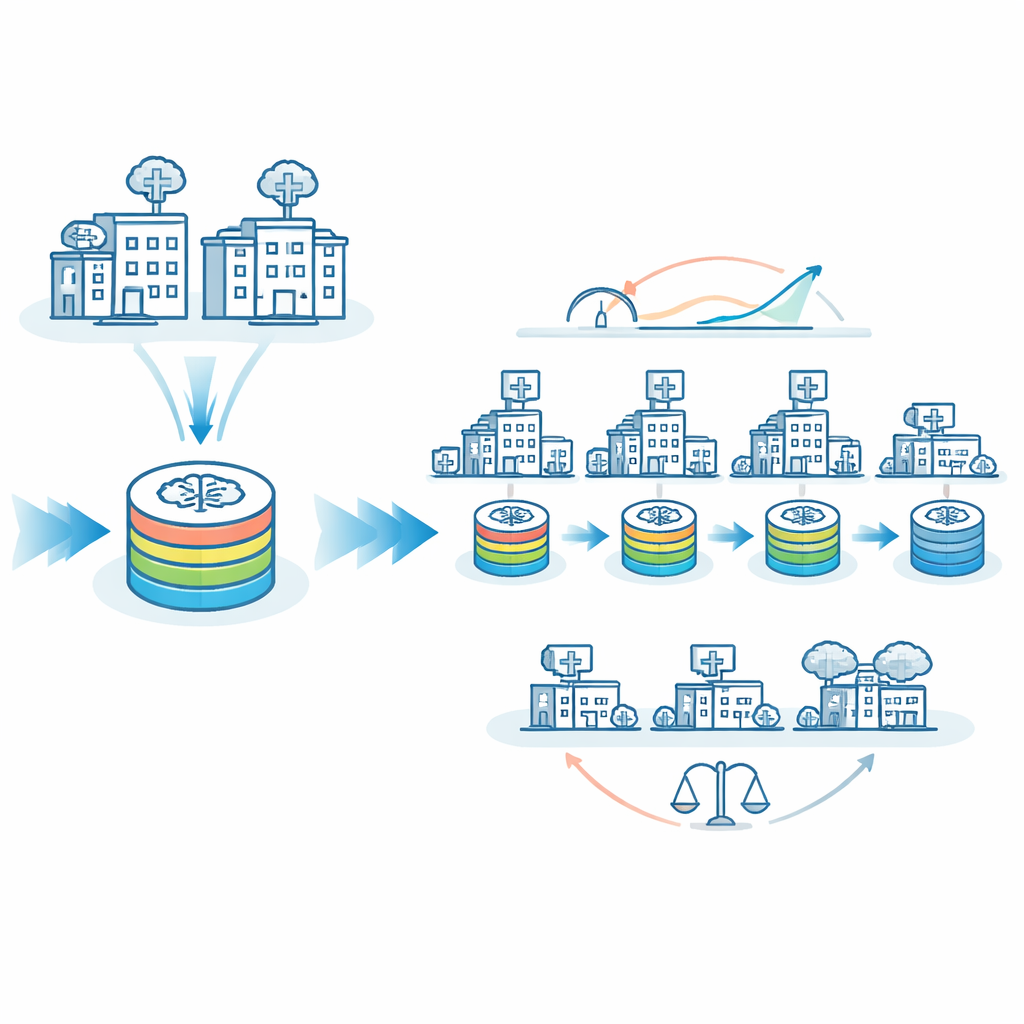
KI fairer zwischen großen und kleinen Krankenhäusern machen
Ein großes Anliegen bei medizinischer KI ist die Gerechtigkeit: Funktioniert ein Modell für Patienten in kleinen, ländlichen oder ressourcenarmen Krankenhäusern genauso gut wie für solche in großen akademischen Zentren? Das Team untersuchte, wie oft die KI an "größeren" im Vergleich zu "kleineren" Standorten falsche Vorhersagen traf. Beim reinen reisenden Modell unterschieden sich die Fehlklassifikationsraten zwischen diesen Gruppen um etwa 8 Prozentpunkte. Mit FedTM, richtig abgestimmt, wurden die Fehlklassifikationsraten für größere und kleinere Standorte nahezu identisch, bei etwa 26 %. Mit anderen Worten: Das Modell wurde nicht nur insgesamt genauer, sondern auch gleichmäßiger in seiner Leistung. FedTM verlagerte außerdem den Großteil der rechenintensiven Arbeit in die Aufwärmphase an besser ausgestatteten Standorten und halbierte damit nahezu die Anzahl der Trainingszyklen, die kleine Standorte durchführen mussten, während die gesamte Trainingszeit ähnlich blieb.
Was das für die globale digitale Gesundheit bedeutet
FedTM bietet einen praktischen Weg zu KI-Werkzeugen, die Privatsphäre respektieren, die Leistung verbessern und die Vorteile gerechter über die Welt verteilen. Indem auch Standorte mit sehr wenig Daten Einfluss auf das Endmodell nehmen können, kann dieses Rahmenwerk dazu beitragen, dass Menschen in ressourcenarmen oder abgelegenen Regionen beim Fortschritt neuer Diagnosewerkzeuge nicht zurückbleiben. Obwohl die Studie sich auf eine Scan-Art und eine Erkrankung konzentrierte, lässt sich der Ansatz prinzipiell auf viele andere medizinische Fragestellungen übertragen. Mit der zunehmenden Verbreitung mobiler Geräte und Wearables und strengeren Regularien zur Datensouveränität könnten hybride Strategien wie FedTM entscheidend werden, um vertrauenswürdige, inklusive und verantwortungsvolle medizinische KI aufzubauen.
Zitation: Souza, R., Stanley, E.A.M., Ohara, E.Y. et al. Combining federated learning and travelling model boosts performance and opens opportunities for digital health equity. npj Digit. Med. 9, 294 (2026). https://doi.org/10.1038/s41746-026-02483-y
Schlüsselwörter: föderiertes Lernen, reisendes Modell, Parkinson-Krankheit, medizinische Bildgebung KI, Gesundheitsgerechtigkeit