Clear Sky Science · de
Unterscheidung zwischen primärem und metastasiertem muzinösem Ovarialkarzinom anhand histopathologischer Bilder mittels Deep Learning
Warum das für Patienten und Ärzte wichtig ist
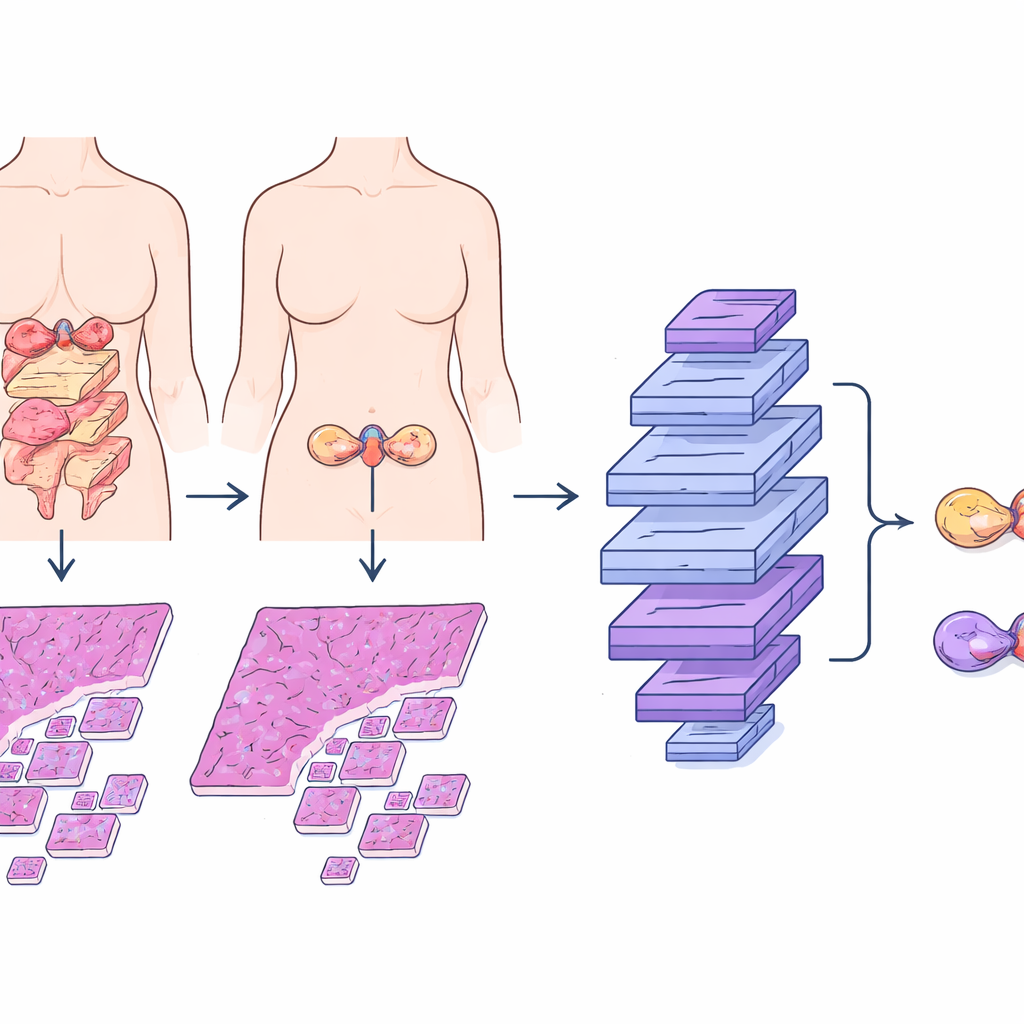
Wenn jemand die Diagnose Eierstockkrebs erhält, steht als nächstes die entscheidende Frage an: Wo hat der Krebs begonnen? Beim häufigen Subtyp des muzinösen Ovarialkarzinoms können Tumoren im Eierstock entweder echte primäre Eierstocktumoren sein oder Befunde, die von Magen oder Darm gestreut haben. Diese beiden Situationen erfordern sehr unterschiedliche Behandlungen und haben unterschiedliche Prognosen, doch selbst erfahrene Pathologen haben mitunter Schwierigkeiten, sie mikroskopisch zu unterscheiden. Diese Studie stellt ein spezialisiertes künstliches Intelligenz‑(KI‑)System vor, das digitale Mikroskopbilder auswertet und Ärzten hilft, diese beiden Möglichkeiten genauer und effizienter zu unterscheiden.
Zwei sich ähnelnde Krebserkrankungen mit sehr unterschiedlichen Verläufen
Das muzinöse Ovarialkarzinom bildet oft große, von Schleim gefüllte Tumoren, die bemerkenswert ähnlich aussehen können, egal ob sie im Eierstock entstanden sind oder vom Gastrointestinaltrakt eingewandert sind. Klassischerweise stützen sich Pathologen auf eine Kombination aus visuellen Hinweisen in eingefärbten Gewebeschnitten, zusätzlichen Laborfärbungen, bildgebenden Verfahren und der klinischen Vorgeschichte. Selbst mit dieser umfassenden Abklärung kann die Diagnose unsicher bleiben, besonders wenn kleine oder verborgene Tumoren an anderer Stelle im Körper vorliegen. Frühere Arbeiten schlugen Checklisten vor, die Tumorgröße, Ein‑ oder beidseitige Ovarbefall und bestimmte Zelltypen berücksichtigen, doch diese Regeln versagen, wenn metastatische Tumoren primären Ovarialtumoren nachahmen. Eine Fehleinordnung — metastatisch als primär oder umgekehrt — kann zu falscher Operation, falscher Chemotherapie und irreführender Beratung zur Prognose führen.
Computern beibringen, Gewebebilder zu lesen
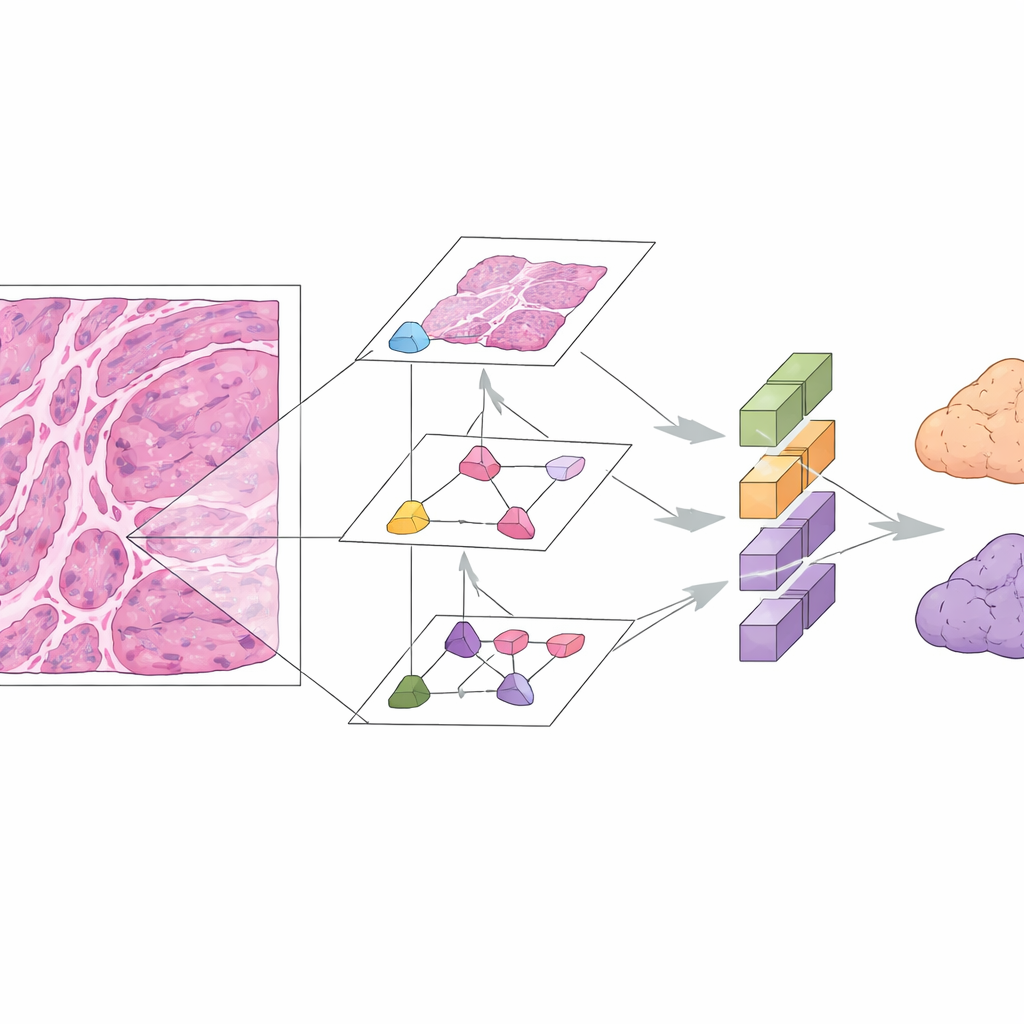
Digitale Pathologie und Deep Learning bieten einen alternativen Weg. In dieser Studie sammelten die Forschenden Mikroskopbilder von 167 Patientinnen mit gut dokumentierten muzinösen Ovarialtumoren aus drei Krankenhäusern. Sie konzentrierten sich auf die standardmäßigen Hämatoxylin‑und‑Eosin (H&E)‑gefärbten Schnitte, wie sie ohnehin routinemäßig verwendet werden. Das Team entwickelte das Mucinous Ovarian Carcinoma Origin Prediction Model, kurz MOCOPM, das jede ganze Objektträgeraufnahme automatisch in viele kleine Patches unterteilt und diese ohne zusätzliche klinische Informationen analysiert. Sie testeten mehrere neuronale Netzwerkarchitekturen und fanden heraus, dass ein neuer graphbasierter Ansatz, der davon inspiriert ist, wie Pathologen bei verschiedenen Vergrößerungen hinein‑ und herauszoomen, am besten funktioniert. Dieses Modell verbindet Patches über drei Zoom‑Ebenen hinweg und kann so sowohl feine zelluläre Details als auch breitere Wachstumsmuster erfassen.
Wie gut die KI in der Praxis performt
MOCOPM wurde zunächst anhand von Fällen aus einem großen Überweisungszentrum trainiert und validiert, in dem schwierige und ungewöhnliche Tumoren häufig sind. In dieser internen Kohorte trennte es primäre von gastrointestinalen Metastasen mit hoher Genauigkeit, was durch eine Fläche unter der Receiver‑Operating‑Characteristic‑Kurve (AUC) von 0,91 gezeigt wurde. Die Forschenden forderten das System dann mit Bildern aus zwei weiteren Krankenhäusern heraus, in denen die Präparation der Schnitte unabhängig erfolgte und die Fälle insgesamt unkomplizierter waren. Dort erzielte das Modell eine noch bessere Performance mit einer AUC von 0,96 sowie guten Werten für Präzision und Sensitivität. Es hielt auch bei Tests auf einem separaten öffentlichen Datensatz primärer muzinöser Ovarialkarzinome einer anderen Forschungsgruppe stand, was darauf hindeutet, dass der Ansatz über verschiedene Quellen hinweg relativ robust ist.
Ein Blick in die Black Box
Da KI‑Werkzeuge oft als undurchsichtig wahrgenommen werden, nutzten die Forschenden eine Erklärtechnik namens GNNExplainer, um hervorzuheben, welche Bereiche eines Schnitts die Entscheidungen des Modells am stärksten beeinflussten. In der Mehrzahl der korrekt klassifizierten Fälle, die sie untersuchten, überlappten die hervorgehobenen Regionen mit Merkmalen, die auch menschliche Expertinnen und Experten verwenden, etwa Gruppen spezieller "Signet‑Ring"‑Zellen, Muster des invasiven Verhaltens der Tumorzellen und Gemische aus benignen, grenzwertigen und eindeutig malignen Komponenten. Diese Übereinstimmung legt nahe, dass das System nicht nur irrelevante visuelle Besonderheiten nutzt, sondern medizinisch sinnvolle Muster erkennt. Wichtig ist auch, dass MOCOPM nur routinemäßige H&E‑Schnitte benötigt, was Zeit und Kosten sparen kann, weil umfangreiche Zusatzfärbungen seltener nötig wären.
Was das für die künftige Versorgung bedeuten könnte
Die Autorinnen und Autoren betonen, dass MOCOPM nicht dazu gedacht ist, Pathologinnen und Pathologen zu ersetzen, sondern als Entscheidungsunterstützung zu dienen. In hektischen oder ressourcenarmen Umgebungen könnte es schwierige Fälle markieren, Expertinnen und Experten auf verdächtige Regionen eines Schnitts hinweisen und eine zusätzliche Kontrolle liefern, bevor eine endgültige Diagnose gestellt wird. Die Studie hat Einschränkungen: Die Krebsform ist selten, die Stichprobengröße beschränkt und metastatische Tumoren aus nicht‑intestinalen Primärherden wurden nicht eingeschlossen. Größere, prospektive Studien sind erforderlich, bevor ein solches System in den klinischen Alltag integriert werden kann. Dennoch zeigt die Arbeit, dass sorgfältig gestaltete KI dabei helfen kann, eine der schwierigsten Unterscheidungen beim Eierstockkrebs zu treffen und so sicherzustellen, dass Patientinnen die Behandlung erhalten, die dem tatsächlichen Ursprungsort ihres Tumors entspricht.
Zitation: Zhang, MY., Liu, B., Qin, ZJ. et al. Distinction between primary and metastatic mucinous ovarian carcinoma from histopathology images using deep learning. npj Digit. Med. 9, 276 (2026). https://doi.org/10.1038/s41746-026-02459-y
Schlüsselwörter: mucinöses Ovarialkarzinom, digitale Pathologie, Deep Learning, graphneuronales Netzwerk, Krebsdiagnose