Clear Sky Science · de
Robuste und interpretierbare kausale Inferenz auf Einheitsebene in neuronalen Netzen bei pädiatrischer Myopie
Warum das für Familien und Ärztinnen wichtig ist
Kindliche Kurzsichtigkeit, oder Myopie, nimmt weltweit in alarmierendem Tempo zu, besonders in Ostasien. Eltern möchten wissen, welche Gewohnheiten, Körpermerkmale und familiären Faktoren tatsächlich dazu führen, dass die Sehschärfe ihrer Kinder schlechter wird – und nicht nur, welche Merkmale zufällig mit schlechtem Sehen einhergehen. Gleichzeitig können moderne Künstliche-Intelligenz-(KI)-Werkzeuge vorhersagen, wer myop wird, agieren aber häufig als undurchsichtige Blackboxen. Diese Studie verbindet beide Welten: Sie zeigt, wie ein neuronales Netz so umgestaltet werden kann, dass es für jedes Kind aufzeigt, welche spezifischen Faktoren wahrscheinlich die Entwicklung einer Myopie verursachen – auf eine Weise, die Ärztinnen und Ärzten verständlich und vertrauenswürdig erscheint.

Mehrere tausend Kinder über die Zeit beobachtet
Die Forschenden analysierten Daten der Anyang Childhood Eye Study, einer großen schulbasierten Studie in Zentralchina, die mehr als 3000 Erstklässler über sechs Jahre begleitete. Jedes Jahr unterzogen sich die Kinder ausführlichen Augenuntersuchungen und beantworteten Fragebögen zu ihrem Alltag. Aus diesem reichhaltigen Datensatz extrahierte das Team 16 zentrale Merkmale, die Verhalten (wie Naharbeit und Zeit im Freien), Körpermaße (etwa Größe und Puls), Ernährung, Augenstruktur (einschließlich Achsenlänge und Hornhautform) und familiäre Brillen-Vorgeschichte abbilden. Sie trainierten ein standardmäßiges Feedforward‑Neuronales Netz, um vorherzusagen, ob ein Kind während der sechsjährigen Nachbeobachtung Myopie entwickeln würde, und erreichten eine Genauigkeit, die mit starken traditionellen Modellen wie logistischer Regression und Random Forest vergleichbar war oder diese übertraf.
Aus einer Blackbox wird eine Ursache‑Wirkungs‑Karte
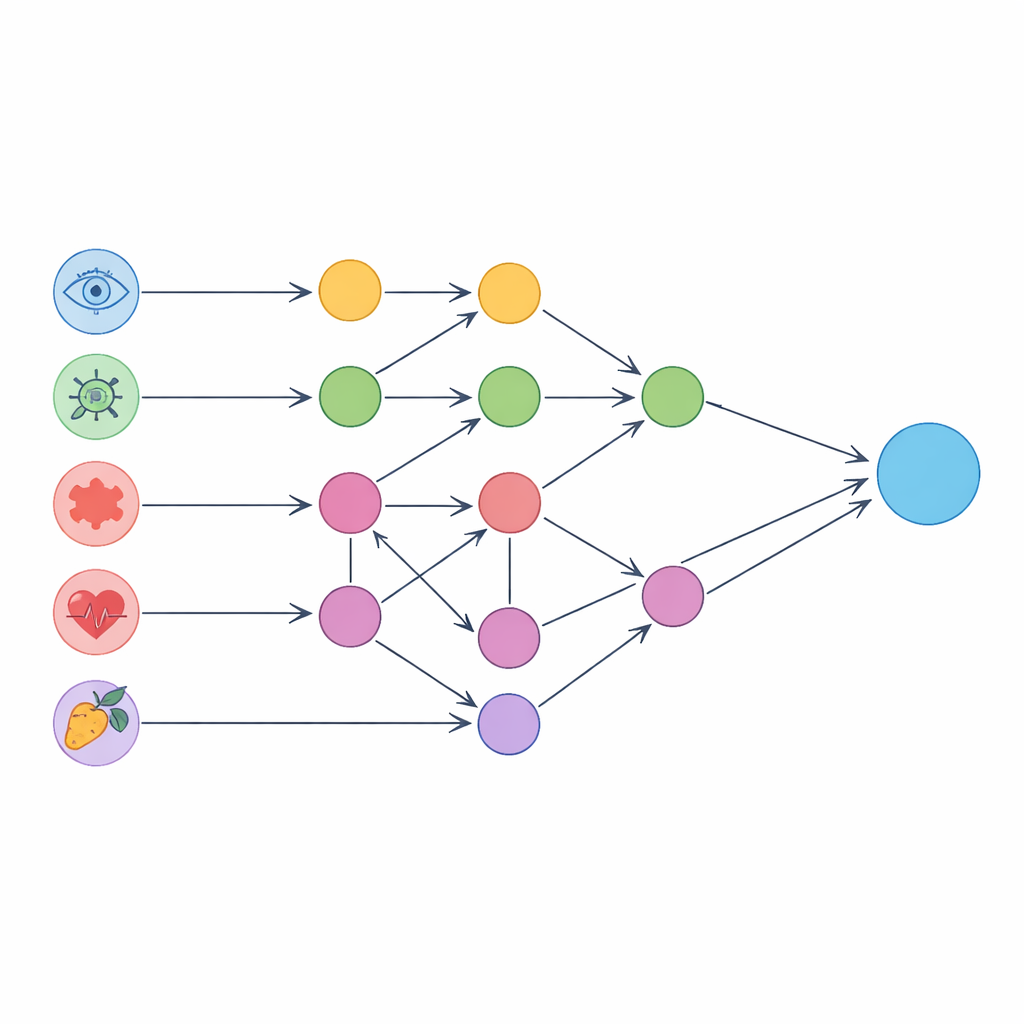
Statt bei der Prognose stehen zu bleiben, stellten die Autorinnen und Autoren eine tiefere Frage: Welche Eingaben treiben diese Vorhersagen wahrscheinlich über Ursache‑Wirkungs‑Pfade an? Zunächst wendeten sie einen Algorithmus zur kausalen Entdeckung an, um aus rein beobachtungsbasierten Daten ein gerichtetes Netzwerk von Beziehungen zwischen den 16 Merkmalen abzuleiten. Dieser Graph stimmte mit vielen bekannten klinischen Zusammenhängen überein – etwa beeinflussten elterliche Myopie, Geschlecht, Fokussierfähigkeit und Hornhautkrümmung die Augenachse und Refraktion, und die Augenlänge wiederum bestimmte, wie Licht im Auge fokussiert wird. Das Team legte diesen Graphen über die Eingabeschicht des neuronalen Netzes und gruppierte jeden Eingangsneuron in eine von drei Kategorien: isolierte Einheiten, die weder andere Eingaben verursachen noch von ihnen abhängen; reine Einheiten, die über klare Vermittlungsketten wirken; und konfunderte Einheiten, deren Effekte mit anderen Variablen verknäuelt sind.
Einblicke in unterschiedliche Eingabetypen
Bei isolierten Einheiten, etwa Pulsrate oder bestimmten Ernährungsmaßen, schätzten die Forschenden, wie eine alleinige Änderung dieses einen Merkmals die Netzwerkvorhersage in Richtung „myop“ oder „nicht myop“ verschieben würde. Ein höherer Puls, der auf eine bessere Durchblutung hindeuten kann, erwies sich als schützend gegen Myopie, was mit früheren medizinischen Studien übereinstimmt. Einige andere isolierte Faktoren, wie kohlensäurehaltige Getränke und Eierkonsum, zeigten Muster, die früheren Berichten widersprachen—wahrscheinlich wegen unausgewogener Ernährungsgewohnheiten in bestimmten Untergruppen der Kohorte. Für reine Einheiten, darunter Größe, Geschlecht, elterliche Myopie, Fokussierfähigkeit und Hornhautkrümmung, verfolgte das Team sowohl direkte als auch indirekte Pfade im kausalen Graphen. Sie bestätigten zum Beispiel, dass größere Kinder tendenziell längere Augen und ein höheres Myopie‑Risiko haben — nicht weil Größe an sich schädlich ist, sondern weil Augenwachstum mit dem Körperwachstum einhergeht.
Verschlungene Einflüsse mit klügerer Statistik handhaben
Die herausforderndsten Faktoren — Achsenlänge und cycloplegische Refraktion — sind sowohl zentral für Myopie als auch stark mit anderen Augenmerkmalen verknüpft. Um diese konfunderten Einheiten zu behandeln, bauten die Forschenden ein domänen‑adaptives Meta‑Learning‑System, das die Daten mittels Techniken neu ausbalanciert, wie sie in moderner kausaler Inferenz verwendet werden. Indem sie schätzten, wie wahrscheinlich es für jedes Kind ist, in verschiedene „Behandlungs“-Level der Augenachse oder Refraktion zu fallen, und ein Ensemble aus baumbasierten Modellen nutzten, konnten sie abschätzen, wie Änderungen dieser Messgrößen kausal das vorhergesagte Myopie‑Risiko beeinflussen würden. Die resultierenden Muster — etwa dass längere Augen das Risiko erhöhen und schwächere Fokussierleistung mit mehr Myopie einhergeht — stimmten gut mit langjährigem klinischem Wissen überein. Eine Reihe von „Widerlegungs“-Tests — Hinzufügen falscher Confounder, Resampling der Daten und Verwendung von Placebo‑Variablen — zeigte, dass diese kausalen Schätzungen stabil sind und keine Artefakte von Overfitting darstellen.
Was das für klarere, gerechtere medizinische KI bedeutet
Am Ende zeigt die Studie, dass sich ein tiefes neuronales Netz für pädiatrische Myopie in sinnvolle Bausteine zerlegen lässt, die reale Biologie widerspiegeln und nicht bloß numerische Tricks. Durch die Klassifikation von Eingaben in isolierte, reine und konfunderte Rollen und das anschließende Anwenden maßgeschneiderter kausaler Methoden für jede Gruppe offenbart das Framework, welche Lebensstilfaktoren wirklich schützend wirken, welche Körpermaße als Frühwarnzeichen dienen und wo die interne Logik des Modells mit dem medizinischen Konsens in Konflikt steht. Die Arbeit ersetzt zwar keine klinischen Studien, bietet aber eine leistungsfähige Linse zur Überprüfung und Verbesserung von KI‑Werkzeugen, bevor sie die Versorgung beeinflussen. Allgemeiner ist der Ansatz modellagnostisch und könnte auf andere Gesundheitsfragen angewandt werden, um medizinische KI dahin zu treiben, nicht nur genau, sondern auch transparent, prüfbar und mit den Zielen von Präzisionsmedizin und gerechter Gesundheitsversorgung in Einklang stehend zu sein.
Zitation: Jin, Z., Kang, M., Zhao, W. et al. Robust and interpretable unit level causal inference in neural networks for pediatric myopia. npj Digit. Med. 9, 263 (2026). https://doi.org/10.1038/s41746-026-02442-7
Schlüsselwörter: pädiatrische Myopie, kausale Inferenz, erklärbare KI, neuronale Netze, digitale Medizin