Clear Sky Science · de
Ein Deep‑Learning‑Modell, das strukturierte Daten und klinische Texte integriert, um Rezidive von Vorhofflimmern vorherzusagen
Warum das für Menschen mit unregelmäßigem Herzschlag wichtig ist
Vorhofflimmern, eine häufige Störung des Herzrhythmus, kehrt oft zurück, selbst nachdem Patientinnen und Patienten eine Katheterablation durchlaufen haben — ein invasiver Eingriff, der einen normalen Herzrhythmus wiederherstellen soll. Viele Betroffene und ihre Ärztinnen und Ärzte fragen sich: Wer hat das höchste Rückfallrisiko, und wer kann sich eher beruhigt zurücklehnen? Diese Studie zeigt, wie moderne künstliche Intelligenz sowohl Zahlen als auch Arztberichte in der Patientenakte auswerten kann, um die Wahrscheinlichkeit eines Rezidivs von Vorhofflimmern genauer vorherzusagen — mit potenziellen Folgen für die Nachsorge und zur Vermeidung wiederholter Eingriffe.
Ein hartnäckiges Rhythmusproblem, das oft wieder auftritt
Bei der Katheterablation werden kleine Bereiche im Herzen verödet oder vereist, die den abnormalen Rhythmus auslösen oder aufrechterhalten. Dennoch erleben 30–50 % der Patienten innerhalb eines Jahres ein Wiederauftreten des unregelmäßigen Herzschlags und benötigen manchmal einen weiteren Eingriff. Bestehende Risikoscores, die meist auf einer Handvoll Messgrößen wie Kammergröße und Typ des Vorhofflimmerns basieren, liefern nur ein unvollständiges Bild. Häufig werden dabei detaillierte Informationen zur Durchführung des Eingriffs, Befunde aus Ultraschalluntersuchungen und Feinheiten des Gesamtzustands, die in Textberichten verborgen sind, nicht berücksichtigt. Folglich fällt es Ärztinnen und Ärzten weiterhin schwer, diejenigen zu identifizieren, die besonders engmaschig überwacht oder zusätzlich vorbehandelt werden sollten.
Routine‑Krankenhausdaten in ein intelligenteres Vorhersagewerkzeug verwandeln
Forschende in China sammelten Daten von 2.508 Patienten, die zwischen 2015 und 2024 in fünf Krankenhäusern einer Vorhofflimmer‑Ablation unterzogen wurden. Der typische Patient war 65 Jahre alt; etwa jeder Fünfte erlitt während einer medianen Nachbeobachtungszeit von annähernd drei Jahren ein Rezidiv. Für jede Person erfasste das Team strukturierte Daten — etwa Alter, Blutdruck, Blutwerte, Größe der Herzkammer und vorhandene Risikoscores — sowie unstrukturierte Texte wie 24‑Stunden‑Herzmonitor‑Zusammenfassungen, Ultraschallberichte und detaillierte Protokolle der Eingriffe von Elektrophysiologen. Anschließend entwickelten sie ein zweigleisiges Deep‑Learning‑Modell: ein Zweig verarbeitete numerische und kategoriale Daten, der andere nutzte große Sprachmodelle, um freie Textberichte in quantitative Merkmale zu überführen, die mit den Zahlen kombiniert werden konnten.
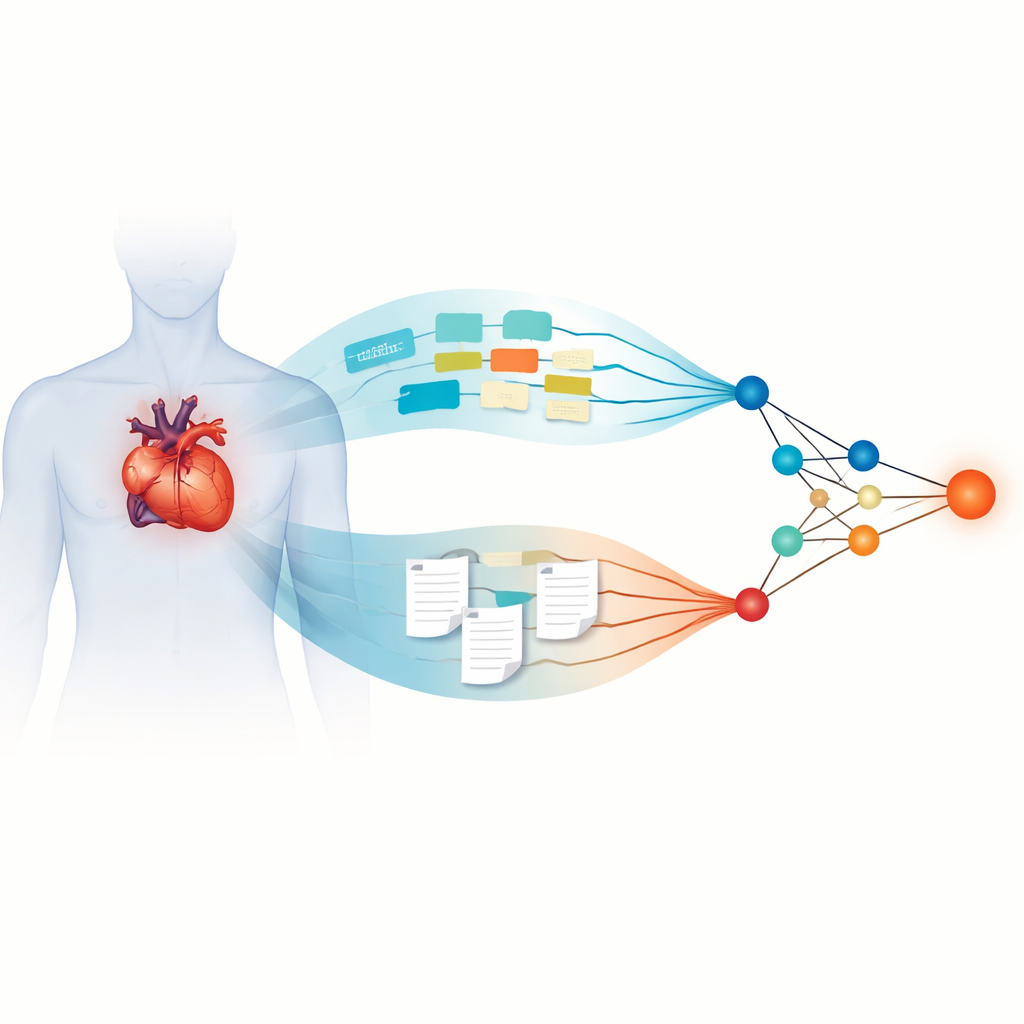
Wie fortgeschrittene Sprachmodelle Ärzte‑Notizen lesen
Der Textzweig des Systems stützte sich auf vier moderne große Sprachmodelle, die ursprünglich mit riesigen Textkorpora trainiert und dann an die medizinische Fachsprache angepasst wurden. Diese Modelle wurden an de‑identifizierten Krankenhausberichten feinabgestimmt, damit sie spezielle Fachbegriffe und Muster besser erfassen können. Die Studie verglich verschiedene Sprachmodelle, um zu ermitteln, welche Textmerkmale Rezidive am besten vorhersagten. Der Spitzenreiter war MedGemma, ein speziell für medizinische Inhalte optimiertes Modell. Wenn seine Textmerkmale mit dem Zweig für strukturierte Daten fusioniert wurden, zeigte das resultierende „MedGemma‑Fusion“‑Modell beeindruckende Genauigkeit, mit Flächen unter der ROC‑Kurve von über 0,90 in Trainings-, Validierungs‑ und unabhängigen Testkliniken. Das bedeutete, dass das Modell zuverlässig zwischen Patienten unterscheiden konnte, die frei von Arrhythmien bleiben würden, und solchen, bei denen ein Rückfall wahrscheinlich war.
Ein Blick in die Blackbox der KI
Um zu verstehen, welche Informationen das Modell für seine Vorhersagen nutzte, wandten die Forschenden Interpretierbarkeitswerkzeuge an, die den Einfluss jeder Eingangsgröße schätzen. Bei den strukturierten Daten hatten vertraute klinische Faktoren wie die Dauer des Vorhofflimmerns, die Größe des linken Vorhofs und ob der Rhythmus intermittierend oder persistent war, das größte Gewicht. Aus dem Textbereich traten Begriffe hervor, die mit Ablationsschritten verbunden sind — etwa Beschreibungen der Lungenvenen und elektrischer Potentiale — und spiegelten zentrale Aspekte erfolgreicher Behandlung wider. Begriffe, die die Herzaktion in Ultraschallberichten betreffen, waren ebenfalls wichtig, was zur Annahme passt, dass Veränderungen in der Vorhofbewegung auf langbestehende Schäden hinweisen. Demgegenüber trugen Zusammenfassungen aus 24‑Stunden‑Herzmonitoren vergleichsweise wenig bei, vermutlich weil viele Patienten mit intermittierendem Vorhofflimmern während kurzer Überwachungszeiträume normale Rhythmen zeigen.
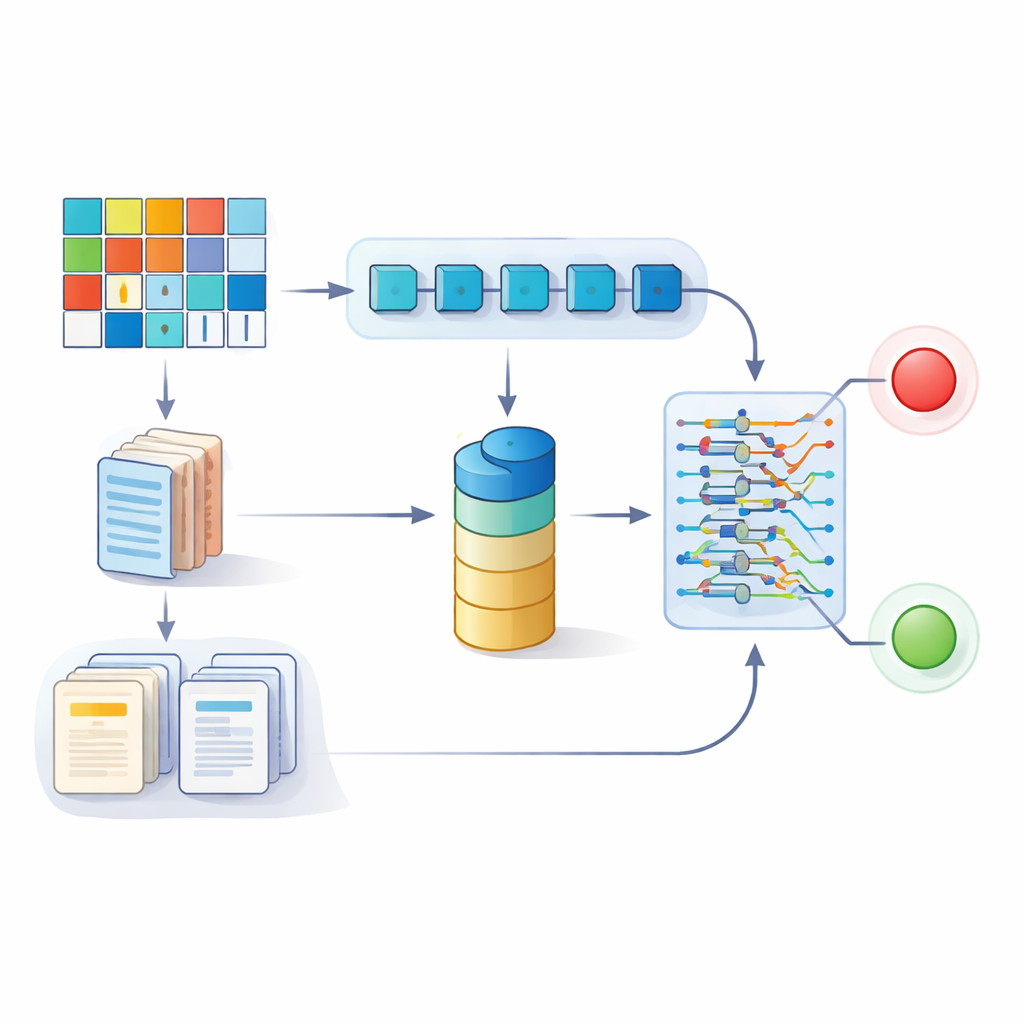
Vom Forschungsmodell zur klinischen Entscheidung
Über die rohe Genauigkeit hinaus prüfte das Team, wie gut ihr Werkzeug Personen in Hoch‑ und Niedrigrisikogruppen einteilte, mithilfe von Überlebensanalysen. Patienten, die vom MedGemma‑Fusion‑Modell als hochriskant eingestuft wurden, zeigten über die Zeit deutlich höhere Rezidivraten. Die Entscheidungsanalyse deutete darauf hin, dass die Anwendung des Modells über viele sinnvolle Schwellenwerte hinweg mehr Nettovorteil bieten würde als die alleinige Nutzung traditioneller Scores oder einzelner Messgrößen. Dennoch betonen die Autorinnen und Autoren wichtige Vorbehalte: Die Studie ist retrospektiv, die Stichprobengrößen — wenngleich für ein einzelnes Projekt groß — sind für Deep Learning moderat, und die Berichtsstile unterschieden sich zwischen den Krankenhäusern. Zukünftige Versionen großer Sprachmodelle und breitere Tests in anderen Gesundheitssystemen werden nötig sein, bevor solche Werkzeuge Routine werden. Nichtsdestotrotz zeigt diese Arbeit, wie die Kombination alltäglicher Zahlen in der Patientenakte mit der Nuance, die in narrativen Berichten verborgen liegt, Vorhersagen schärfen und langfristig helfen kann, Nachsorge und Behandlungsintensität für Menschen mit Vorhofflimmern besser zuzuschneiden.
Zitation: Jia, S., Yin, Y., Guan, Y. et al. A deep learning model integrating structured data and clinical text for predicting atrial fibrillation recurrence. npj Digit. Med. 9, 253 (2026). https://doi.org/10.1038/s41746-026-02436-5
Schlüsselwörter: Vorhofflimmern, Kathetereingriff (Ablation), Deep Learning, klinische Textanalyse, Risikovorhersage