Clear Sky Science · de
Physikalisch eingeschränktes Graph-Neural-Network zur Echtzeit-Vorhersage der Hämodynamik bei intrakraniellen Aneurysmen
Warum das für die Gehirngesundheit wichtig ist
Ausgebulkte, geschwächte Stellen in Hirnarterien, sogenannte intrakranielle Aneurysmen, können ohne Vorwarnung reißen und lebensbedrohliche Blutungen verursachen. Ärztinnen und Ärzte wissen, dass die Art und Weise, wie Blut über diese fragilen Wände strömt, beeinflusst, ob sie stabil bleiben oder nachgeben. Die heute verfügbaren Werkzeuge zur Simulation dieses Flusses sind jedoch so langsam und spezialisiert, dass sie im Alltag kaum genutzt werden. Diese Studie stellt eine schnelle KI-Methode vor, die detaillierte Blutfluss-Simulationen in Sekunden statt Stunden nachbilden kann und damit schnellere und personalisiertere Entscheidungen darüber ermöglicht, wer behandelt werden sollte und wie.
Von statischen Bildern zu bewegtem Blut
Derzeit basieren die meisten Aneurysma-Entscheidungen auf dem, was auf Bildern zu sehen ist: Größe, Form und Lage der Ausbuchtung sowie grundlegende Risikofaktoren wie Alter und Bluthochdruck. Diese Momentaufnahmen übersehen die unsichtbaren Kräfte des strömenden Bluts, etwa wie stark es an der Gefäßwand reibt oder wie stark diese Kraft im Verlauf eines Herzschlags variiert. Traditionelle Computational-Fluid-Dynamics-Methoden können diese Größen präzise berechnen, erfordern aber fachgerechte Einrichtung und lange Läufe auf leistungsstarken Rechnern. Daher können viele Krankenhäuser sie nicht realistisch einsetzen, wenn eine Antwort innerhalb einer Sprechstunde oder eines Notfalleingriffs nötig ist.
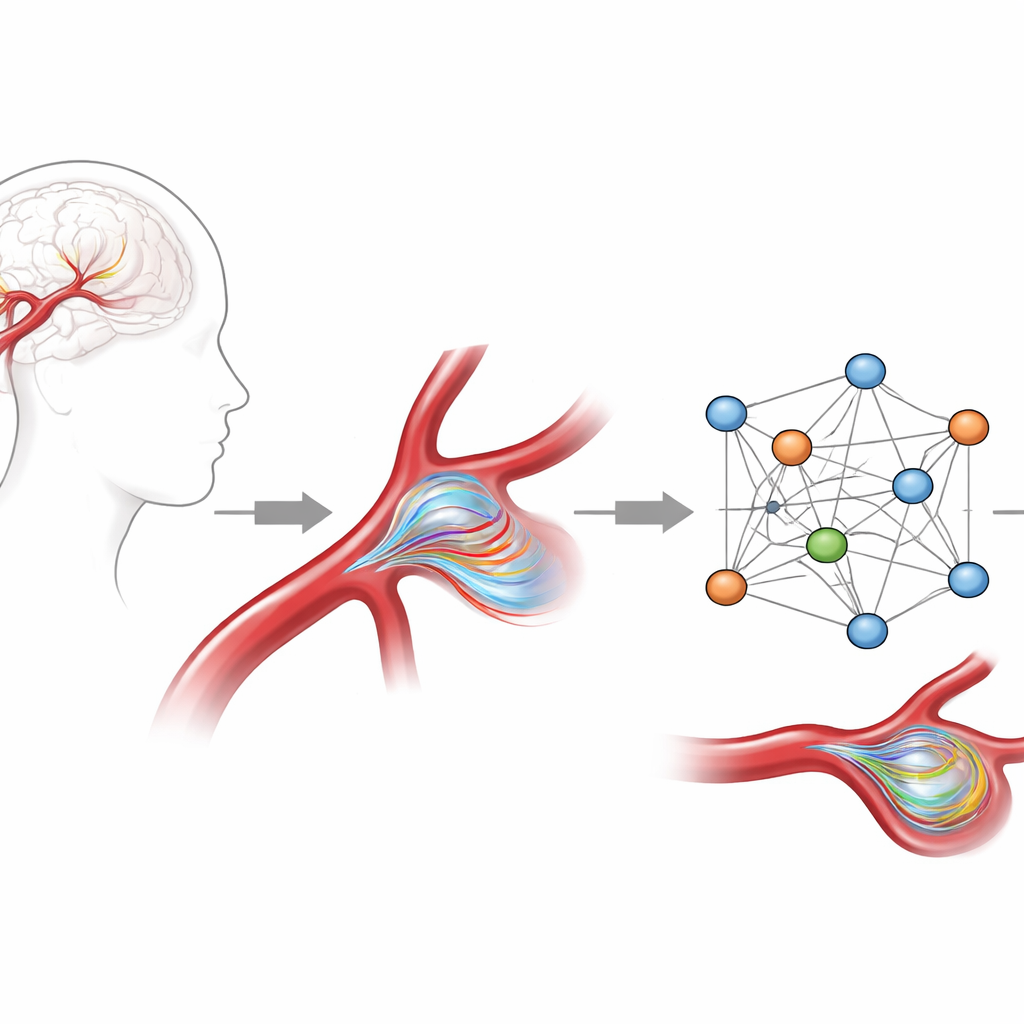
Der KI physikalische Regeln beibringen
Die Forschenden entwickelten ein KI-Modell auf Basis von Graph-Neural-Networks, einer Algorithmusklasse, die natürlicherweise auf verzweigten Strukturen wie Gefäßnetzen statt auf quadratischen Bildgittern arbeitet. Sie trainierten es mit hochwertigen Computersimulationen des Blutflusses in 105 Aneurysma-Formen, die aus realen Patientendaten stammten, mit Fokus auf einer häufigen Lage in einer wichtigen Hirnarterie. Jeder Fall enthielt vollständige dreidimensionale Geschwindigkeits- und Druckfelder über einen ganzen Herzschlag. Um dem Modell ein starkes Gespür für die zugrundeliegende Physik zu geben, baten sie es nicht nur, die simulierten Geschwindigkeiten zu kopieren: Sie fügten zusätzliche Merkmale hinzu, die beschreiben, wie schnell Blut in die Arterie eintritt und wie rasch es beschleunigt, und bestraften die KI, wenn ihre Vorhersagen grundlegende Fluidgesetze wie die Massenerhaltung verletzten.
Ein Blick ins Innere einer gefährlichen Ausbuchtung
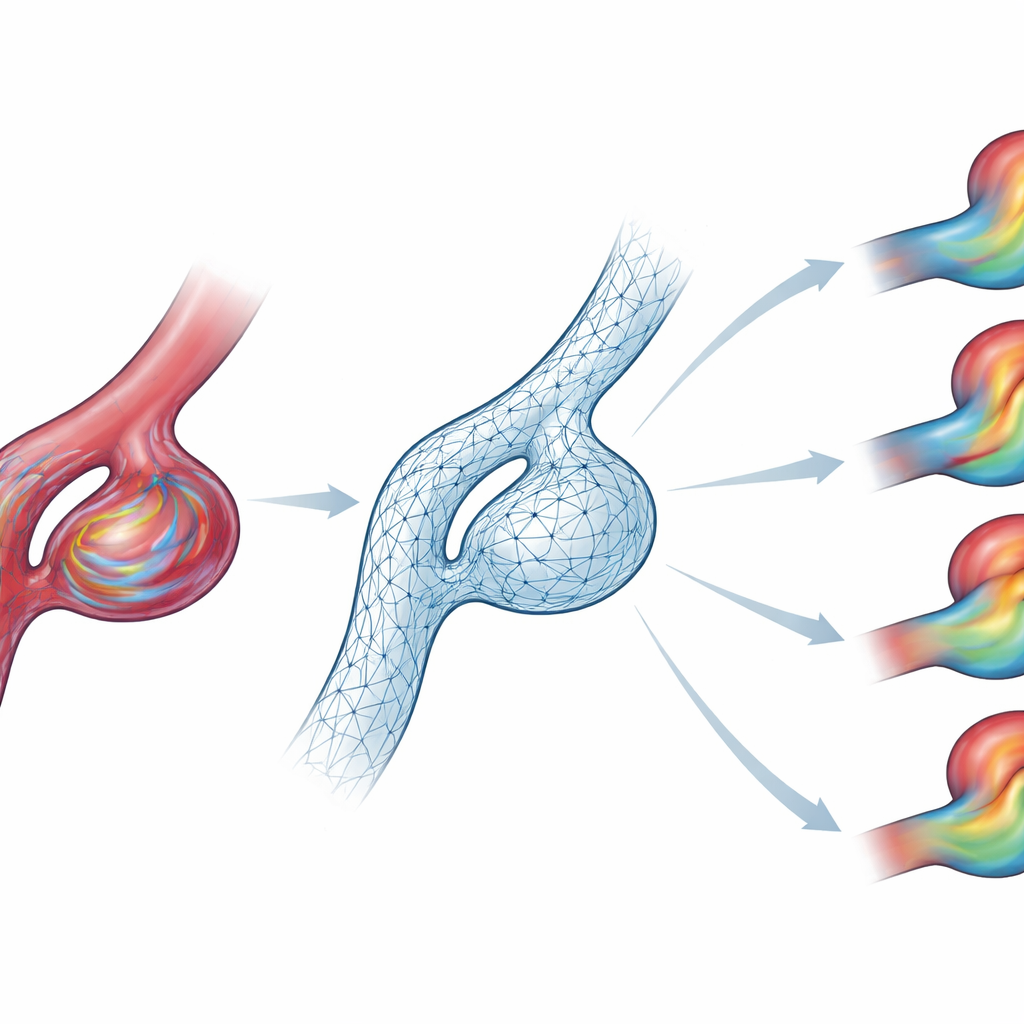
Nach dem Training konnte die KI aus einem Einzelbild von Blutflussinformationen rasch die zeitliche Entwicklung vorwärtsrechnen und die Wirbelmuster und Rezirkulationszonen im Inneren des Aneurysmasacks nachbilden. Im Vergleich zu den Originalsimulationen waren die Kurzzeitfehler bereits gering, aber der wirkliche Prüfstein war, ob diese Fehler anwachsen würden, wenn sie dutzende Schritte in die Zukunft vorhersagte. Die erweiterte, physikalisch eingeschränkte Version bestand diesen Test: über 50 Vorhersageschritte waren ihre Fehler mehr als sechsmal kleiner als die eines einfacheren Basismodells, und sie verfolgte die sich ändernden Strömungen selbst während der turbolentesten Phase des Herzschlags. Als das Team diese Geschwindigkeitsfelder in klinisch relevante Maße umrechnete — wie etwa die mittlere Wand-Schubspannung über der Aneurysmakuppel — blieb die KI bei etwa 10 Prozent der Referenzwerte und lokalisierte korrekt die Bereiche mit den höchsten Spannungen.
Über die Trainingsdaten hinaus generalisieren
Eine zentrale Frage für jede medizinische KI ist, ob sie mit zuvor ungesehenen Patientinnen und Patienten zurechtkommt. Das Team prüfte ihr Modell in zwei Arten ungewohnter Situationen, ohne zusätzliches Training. Zunächst veränderten sie die Zuflusswellenformen, um Muster zu entsprechen, die in anderen Hirnarterien gemessen wurden. Die KI folgte weiterhin dem neuen Timing und der Stärke jedes Pulses, hielt die Fehler moderat und erfasste den umgeformten Fluss innerhalb der Ausbuchtung. Zweitens testeten sie das Modell an vier vollständig patientenspezifischen Aneurysmageometrien mit unterschiedlichen Größen, Halsbreiten und Gefäßverläufen. Obwohl die exakten Geschwindigkeitsniveaus manchmal abwichen, reproduzierte das Modell die wichtigsten Strömungsstrukturen und Einschlagzonen, was darauf hindeutet, dass es das zugrundeliegende Verhalten gelernt und nicht nur die Trainingsformen auswendig gelernt hatte.
Schnellere Antworten am Krankenbett
Da diese KI etwa sechzigmal schneller läuft als die traditionellen Simulationen, von denen sie lernte, wird sie nach nur wenigen Dutzend Fällen effizienter als Standardverfahren und könnte schließlich Vollfeld-Blutflussvorhersagen in unter einer Minute liefern. Die Autoren betonen, dass ihr Werkzeug kein eigenständiger Rupturfolger ist; vielmehr ist es eine schnelle Engine zur Erzeugung physikalisch konsistenter Flusskarten und Wandspannungen, die andere Risikomodelle nutzen können. Sie stellen außerdem ihren 105-Fälle-Datensatz als öffentliches Benchmark zur Verfügung, damit andere Gruppen verbesserte Modelle entwickeln und vergleichen können. Mit weiterem Training an realistischeren Gefäßformen und patientenspezifischen Zuflussdaten könnte dieser Ansatz helfen, die anspruchsvolle Blutflussanalyse aus dem Supercomputer-Labor in die alltägliche Versorgung von Menschen mit Hirnaneurysmen zu bringen.
Zitation: Lannelongue, V., Garnier, P., Jeken-Rico, P. et al. Physics constrained graph neural network for real time prediction of intracranial aneurysm hemodynamics. npj Digit. Med. 9, 212 (2026). https://doi.org/10.1038/s41746-026-02404-z
Schlüsselwörter: Hirnaneurysma, Blutfluss, Graph-Neuronales Netz, Computationale Modellierung, Digitale Medizin