Clear Sky Science · de
Schnelle Vorhersage der kardialen Aktivierung im linken Ventrikel mit geometrischem Deep Learning: ein Schritt zur Planung der kardialen Resynchronisationstherapie
Warum Timing für ein angeschlagenes Herz wichtig ist
Für viele Menschen mit schwerer Herzinsuffizienz können kleine elektrische Impulse aus einem implantierten Gerät den Hauptpumpkammern des Herzens helfen, synchroner zusammenzuziehen. Diese Behandlung, kardiale Resynchronisationstherapie genannt, kann Symptome lindern und das Leben verlängern. Dennoch profitiert etwa ein Drittel der Patienten nur wenig, häufig weil der Stimulationsdraht auf der linken Herzhälfte nicht am optimalen Ort platziert werden kann. Diese Studie untersucht, ob Computermodelle, die moderne künstliche Intelligenz nutzen, schnell vorhersagen können, wie sich elektrische Aktivität auf der linken Herzhälfte ausbreitet, und so Ärzten helfen können, patientenspezifische Stimulationsorte auszuwählen.
Von langsamen Simulationen zu sofortigen Vorhersagen
Die derzeit genauesten Computermodelle des Herzens beruhen auf komplexen Gleichungen, die nachbilden, wie elektrische Signale durch den Herzmuskel laufen. Zwar detailliert, können diese Simulationen auf leistungsstarken Rechnern Minuten dauern — zu lange für den Routineeinsatz während eines Eingriffs. Die Autoren wollten schnelle „Surrogat“-Modelle bauen, die aus diesen aufwändigen Simulationen lernen und deren Ergebnisse nahezu sofort reproduzieren können. Sie konzentrierten sich auf den linken Ventrikel, die Hauptpumpkammer des Herzens, und auf die Vorhersage von „Aktivierungszeitkarten“, die zeigen, wie schnell verschiedene Regionen dieser Kammer während eines Herzschlags elektrisch eingeschaltet werden.
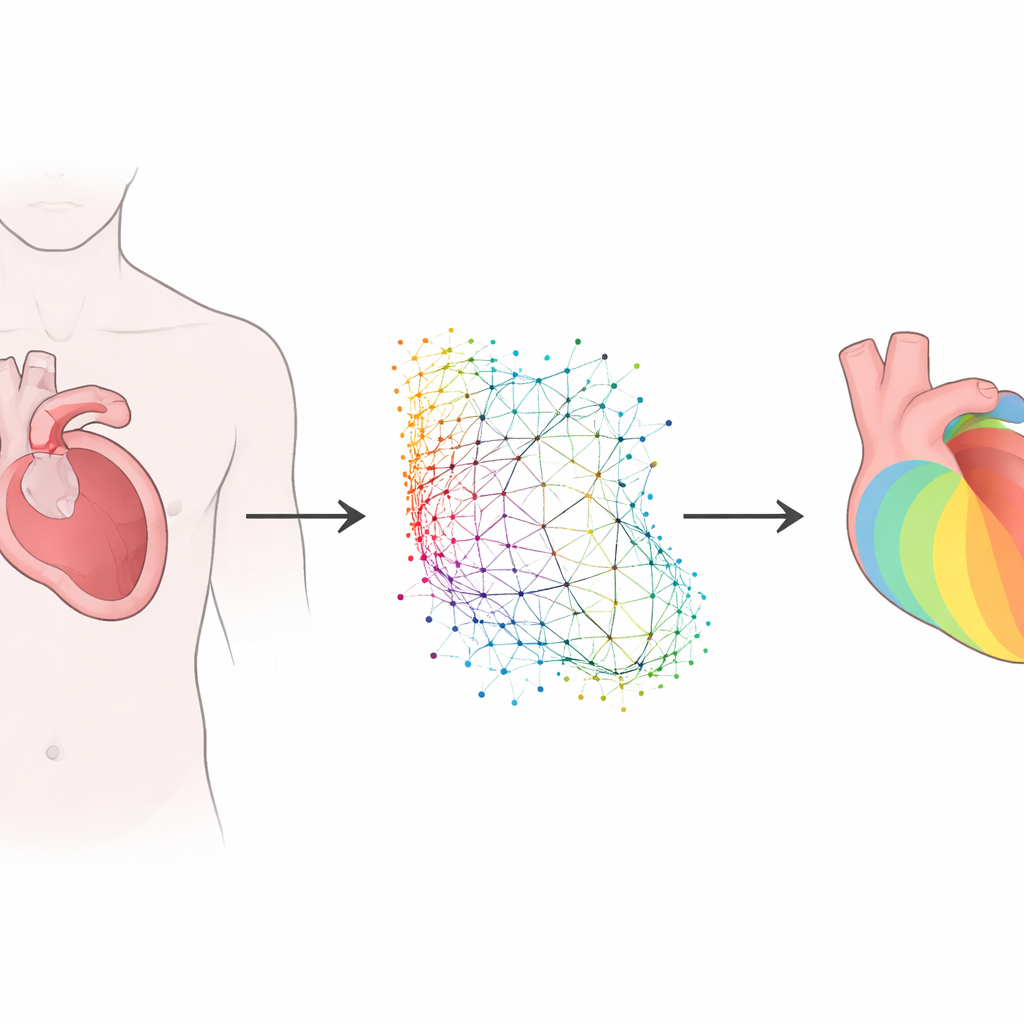
Der KI die Sprache der Herzformen beibringen
Das Herz eines jeden Menschen hat eine leicht unterschiedliche Form, und diese Unterschiede beeinflussen, wie sich elektrische Wellen ausbreiten. Anstatt alle Herzen in ein starres Gitter zu pressen, verwendeten die Forscher eine Gruppe von Methoden, die als geometrisches Deep Learning bekannt sind und direkt mit unregelmäßigen Formen arbeiten können. Sie entwickelten und verglichen zwei verwandte Ansätze. Der eine, basierend auf einem Graph-Neuronalen Netzwerk, behandelt den linken Ventrikel als Sammlung von Punkten, die wie ein Netz verbunden sind. Der andere, ein geometry-informed neural operator, kodiert zunächst die unregelmäßige Form auf ein reguläres internes Gitter, verarbeitet diese Darstellung und überträgt das Ergebnis zurück auf die ursprüngliche Anatomie. Beide Modelle nehmen die dreidimensionale Form des Herzens, die Stimulationsorte und die elektrische Leitfähigkeit des Gewebes als Eingaben und sagen voraus, wie sich die Aktivierung durch die Muskelwand ausbreitet.
Aufbau einer virtuellen Population von Herzen
Weil große Sammlungen realer Patientendaten mit vollständigen dreidimensionalen Aktivierungskarten selten sind, erzeugte das Team seinen eigenen virtuellen Datensatz. Sie starteten mit 75 realen linken Ventrikel‑Formen, die gesunde und erkrankte Herzen abdeckten, und nutzten ein statistisches Formmodell, um 35.000 synthetische Varianten zu erstellen. Für jede Variante wiesen sie realistische Muskelfaser-Richtungen zu, wählten ein oder zwei Stimulationsstellen und variierten die Gewebeleitfähigkeit über einen breiten Bereich. Detaillierte physikbasierte Simulationen erzeugten Aktivierungszeitkarten für all diese virtuellen Herzen, die dann zum Training und Testen der Deep‑Learning‑Modelle verwendet wurden. Die Modelle wurden außerdem mit höher aufgelösten Netzen und mit linken Ventrikel‑Geometrien aus zwei unabhängigen klinischen Kohorten konfrontiert, um zu prüfen, wie gut sie über das synthetische Trainingsset hinaus generalisieren.
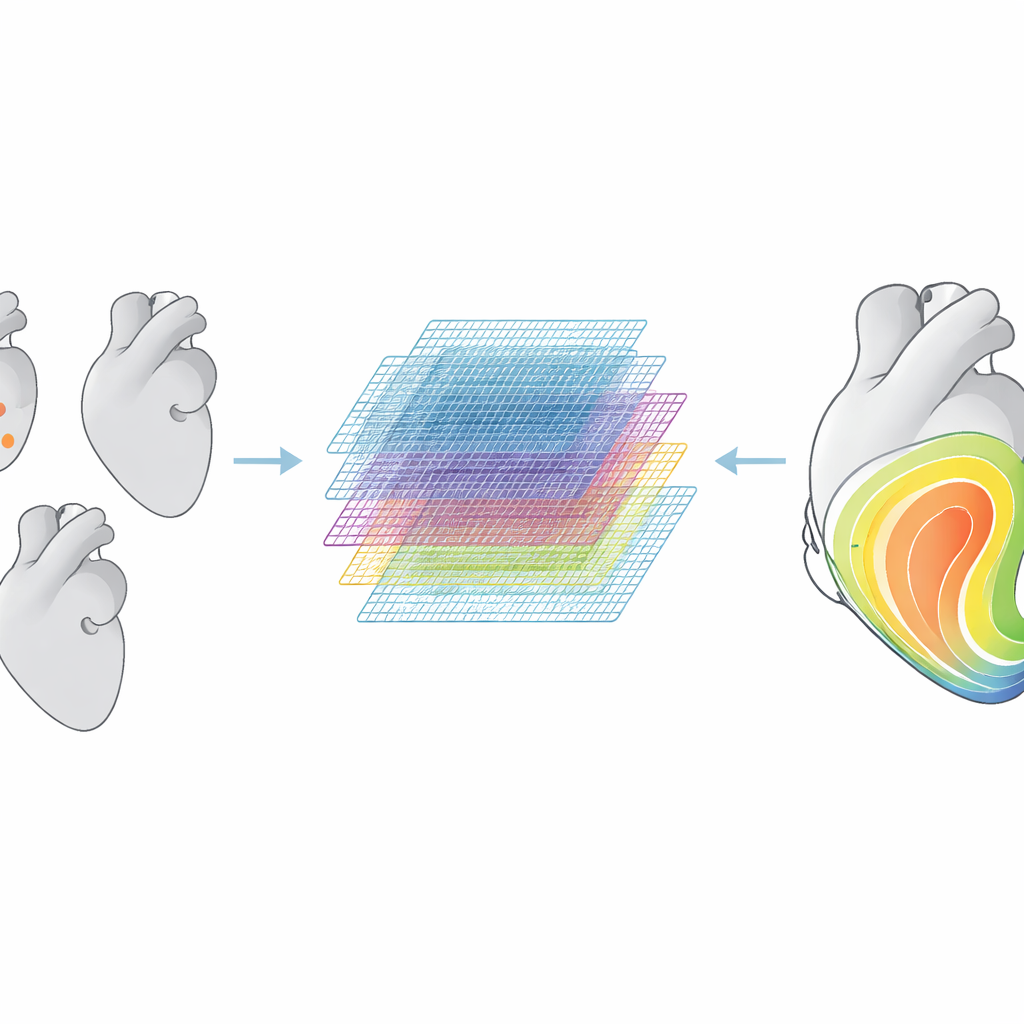
Wie gut schnitten die Modelle ab?
Bei synthetischen Herzen, die denen im Training ähnelten, sagten beide Modelle Aktivierungskarten mit geringen Fehlern voraus, wobei der geometry‑informed neural operator ungefähr doppelt so genau war wie das Graph‑Neuronale Netzwerk. Bei realen Herzformen wuchs der Fehler für beide Modelle, und ihre Leistung wurde vergleichbar. Das deutet darauf hin, dass die Hauptbegrenzung nicht in der Leistungsfähigkeit der Algorithmen liegt, sondern in der Lücke zwischen vereinfachten Trainingsformen und der vollen Komplexität der realen Patientenanatomie. Dennoch konnten die Modelle Vorhersagen in Millisekunden liefern — deutlich schneller als die etwa zehn Minuten, die eine traditionelle Simulation benötigt — und sind damit attraktiv für Aufgaben, die tausende wiederholte Auswertungen erfordern, etwa die Suche über viele mögliche Stimulationsorte.
Test eines virtuellen Planungstools
Das Team bettete die trainierten Modelle anschließend in einen Proof‑of‑Concept‑Planungsworkflow für die Resynchronisationstherapie ein. Ausgehend von einer linken Ventrikel‑Form und einer verrauschten Aktivierungskarte, die klinische Messungen nachahmen sollte, arbeitete der Workflow zunächst rückwärts, um die intrinsische Stimulationsstelle des Patienten und die Gewebeleitfähigkeit zu schätzen. Anschließend suchte er über die Oberfläche des Ventrikels nach einer zweiten Stimulationsstelle, die die gesamte Aktivierungszeit minimieren würde — eine Größe, die in früheren Studien mit besserem Therapieansprechen verknüpft war. Beide Deep‑Learning‑Modelle konnten aus verrauschten Daten die subjekspezifischen Schlüsselfaktoren rückgewinnen und Stimulationsorte vorschlagen, die die Aktivierungszeit deutlich verkürzten, und das alles in wenigen zehn Sekunden auf einer einzelnen Grafikkarte. Die Autoren bauten zudem eine webbasierte Oberfläche, auf der Nutzer Geometrien hochladen, Stimulationsszenarien untersuchen und diese Optimierung interaktiv ausführen können.
Was das für Patienten bedeutet
Diese Arbeit zeigt, dass sorgfältig trainierte Deep‑Learning‑Modelle detaillierte elektrische Simulationen des linken Ventrikels über viele Formen und Stimulationskonfigurationen nachahmen können und dies schnell genug, um in Planungswerkzeugen eingesetzt zu werden. Während die aktuellen Modelle auf synthetischen Trainingsdaten beruhen und nur das elektrische Verhalten im linken Ventrikel betrachten, legen sie das Fundament für umfassendere digitale Zwillinge, die beide Herzhälften und die mechanische Pumpfunktion einschließen. Mit reichhaltigeren realen Daten und weiterer Verfeinerung könnten solche Werkzeuge eines Tages Klinikern ermöglichen, viele Stimulationsstrategien am Computer zu testen, bevor sie in die Klinik gehen, und so die Chancen verbessern, dass jeder Patient eine Gerätekonfiguration erhält, die den Herzrhythmus tatsächlich wiederherstellt.
Zitation: Naghavi, E., Wang, H., Ziaei-Rad, V. et al. Rapid prediction of cardiac activation in the left ventricle with geometric deep learning: a step towards cardiac resynchronization therapy planning. npj Digit. Med. 9, 225 (2026). https://doi.org/10.1038/s41746-026-02399-7
Schlüsselwörter: kardiale Resynchronisationstherapie, geometrisches Deep Learning, kardiale Elektrophysiologie, patientenspezifische Modellierung, digitaler Zwilling