Clear Sky Science · de
CFG-MambaNet: Kontext- und Frequenzgesteuertes Mamba-Netzwerk für die Segmentierung medizinischer Bilder
Warum klarere medizinische Bilder wichtig sind
Wenn Ärztinnen und Ärzte Herzscans, Kolonoskopien, Hautfotos oder Gewebeschnitte untersuchen, benötigen sie oft die Hilfe eines Computers, um genau nachzuzeichnen, wo ein Tumor, ein Organ oder ein verdächtiger Befund beginnt und endet. Dieser Schritt des Nachzeichnens, Segmentierung genannt, bildet die Grundlage für Diagnose, Behandlungsplanung und sogar Entscheidungen über Operationen. Die Arbeit stellt CFG‑MambaNet vor, ein neues System der künstlichen Intelligenz (KI), das diese Grenzen über viele Bildtypen hinweg genauer und zuverlässiger ziehen soll.
Die Herausforderung, präzise Ränder zu ziehen
Moderne KI-Werkzeuge können medizinische Bilder bereits markieren, stoßen aber in klinischen Alltagssituationen auf Probleme. Manche Methoden betrachten nur kleine Pixelumgebungen und verlieren so das größere Bild. Andere erfassen das ganze Bild, benötigen dafür aber enorme Rechenressourcen, was den Einsatz bei großen, hochauflösenden Scans erschwert. Viele Systeme tun sich schwer, wenn das Zielgebiet schwach, unscharf, sehr klein oder ungewöhnlich geformt ist. In der Folge können traditionelle Systeme Teile einer Herzwand abschneiden, die Größe eines Polypen im Dickdarm falsch einschätzen oder den schmalen Rand einer Hautläsion übersehen — Fehler, die zu fehlerhaften Messungen oder verzögerter Diagnose führen können.
Eine neue Art, wie KI das Gesamtbild wahrnimmt
CFG‑MambaNet begegnet diesen Problemen, indem es neu denkt, wie ein KI-Netzwerk ein Bild „sieht“. Im Kern steht ein Visual State Space Block, basierend auf einer aktuellen Architektur namens Mamba. Anstatt in vielen Transformer-basierten Modellen jeden Pixel mit jedem anderen zu vergleichen — ein rechenintensiver Schritt — scannt dieser Block das Bild in geordneter Weise und verfolgt dabei langfristige Muster mit deutlich geringerem Rechenaufwand. Dadurch kann das Netzwerk nachvollziehen, wie weit auseinanderliegende Bildbereiche zueinander in Beziehung stehen, etwa die gesamte Form einer Herzkammer in einem Scan, ohne bei hochauflösenden Daten stark zu verlangsamen.
Form und feine Details trennen
Eine zweite Idee in CFG‑MambaNet ist, jedes Bild ein wenig wie ein Musikstück zu behandeln, mit tiefen und hohen Tönen. Im frequenzgesteuerten Repräsentationsmodul teilt die KI die Bildinformation in glatt verlaufende, langsam veränderliche Komponenten (die die Gesamtform eines Organs erfassen) und schnelle Änderungen (die Kanten und Texturen erfassen). Indem diese beiden Teile getrennt angepasst und anschließend wieder vereint werden, kann das System verschwommene Ränder schärfen und zugleich die größere Struktur erhalten. Das ist besonders nützlich bei Läsionen, deren Ränder in den Hintergrund ausblassen, wie manche Hautflecken oder subtile Gewebeveränderungen in Pathologieschnitten.
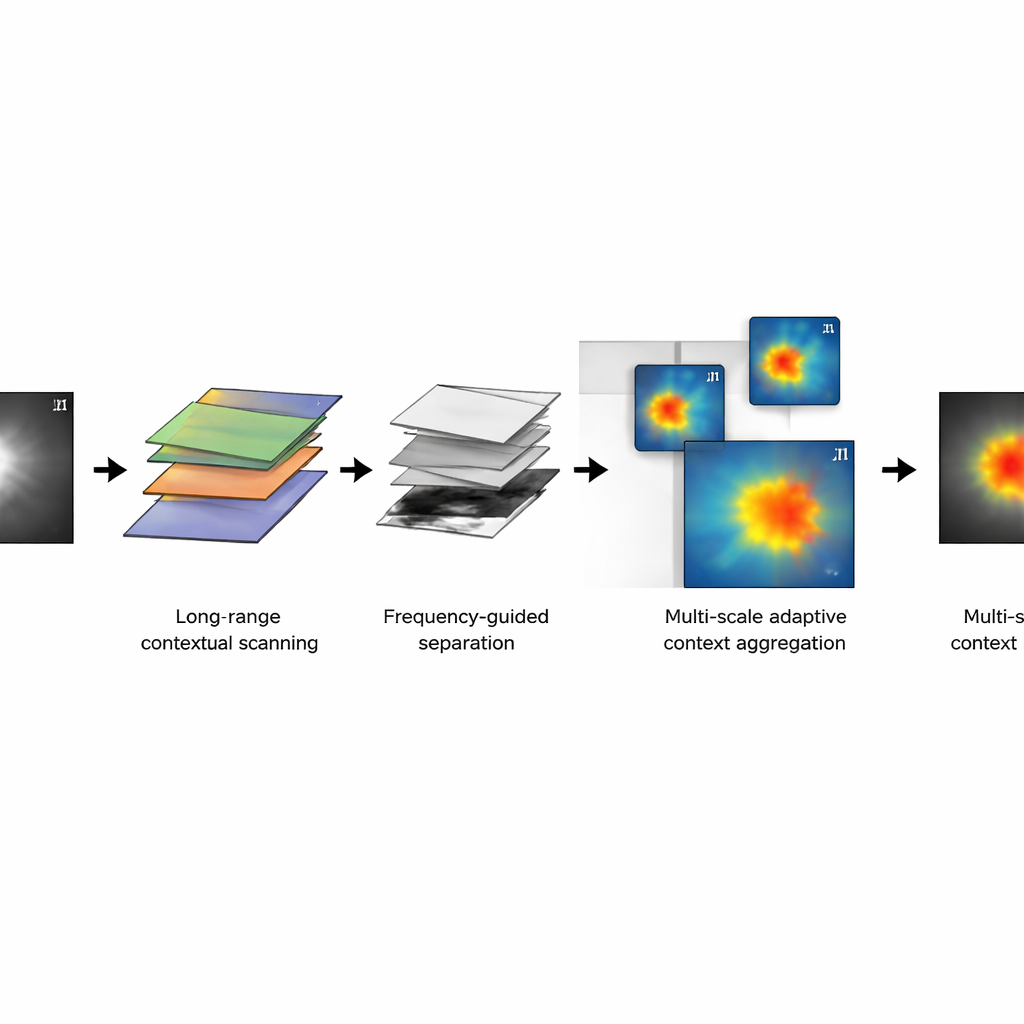
Anpassung an winzige Punkte und große Strukturen
Medizinische Bilder enthalten oft sowohl sehr große als auch sehr kleine Strukturen: ein ganzes Herz und eine dünne Herzwand, eine weite Kolonaufnahme und einen winzigen Polypen. CFG‑MambaNet integriert ein Multi‑Scale Adaptive Context Aggregation Modul, das jede Szene gleichzeitig auf mehreren „Zoom‑Ebenen“ betrachtet. Ein Zweig konzentriert sich auf breite Hintergrundstrukturen, ein anderer folgt flexibel unregelmäßigen Formen, und ein dritter erfasst Muster mittlerer Reichweite. Das Netzwerk lernt dann, wie viel Vertrauen es jeder Zoom‑Ebene in unterschiedlichen Situationen schenken sollte und hebt die jeweils wichtigsten Bereiche hervor. Zusätzliche Trainingsmethoden — etwa eine kombinierte Verlustfunktion, die Flächenpräzision und Kantenschärfe ausbalanciert, sowie Supervision auf mehreren Tiefen im Netzwerk — stabilisieren das Lernen und verfeinern die Grenzen weiter.
Nachgewiesene Verbesserungen bei vier Bildtypen
Zur Evaluierung testeten die Autorinnen und Autoren CFG‑MambaNet auf vier öffentlichen Datensätzen mit Herz‑MRI, Kolonoskopiebildern, Hautläsionsfotos und mikroskopischen Pathologieschnitten. In allen vier Anwendungsgebieten übertraf die neue Methode eine breite Palette führender Segmentierungsmodelle, darunter klassische Faltungsnetzwerke, Transformer-basierte Systeme und andere Mamba‑ähnliche Designs. Sie erreichte größere Überlappung zwischen vorhergesagten und tatsächlichen Regionen, geringere durchschnittliche Abstände zwischen vorhergesagten und tatsächlichen Grenzen und bessere Sensitivität gegenüber schwer erkennbaren Läsionen. Das bedeutet schärfere Konturen von Herzkammern, genauere Polypmasken im Darm, klarere Ränder bei unregelmäßigen Hautläsionen und treuere Nachzeichnungen von Tumorgewebe unter dem Mikroskop.
Was das für die zukünftige Versorgung bedeutet
Aus laienhafter Sicht ist CFG‑MambaNet ein intelligenteres, effizienteres „Nachzeichnungs‑Assistenzsystem“ für Ärztinnen und Ärzte. Indem es sowohl das große Ganze als auch feine Details erkennt und auf mehrere sehr unterschiedliche Bildtypen anwendbar ist, rückt automatisierte Segmentierung näher an die routinemäßige klinische Nutzung. Obwohl weitere Tests an größeren, realen Patientengruppen nötig sind, könnte dieser Ansatz letztlich zu verlässlicheren Messungen, früherer Krankheitsentdeckung und besserer Behandlungsplanung in Kardiologie, Gastroenterologie, Dermatologie und Onkologie beitragen.
Zitation: Ren, G., Chen, Z., Su, P. et al. CFG-MambaNet: Contextual and Frequency-Guided Mamba Network for medical image segmentation. npj Digit. Med. 9, 202 (2026). https://doi.org/10.1038/s41746-026-02393-z
Schlüsselwörter: Segmentierung medizinischer Bilder, Deep Learning, Mamba-Netzwerk, Multi-Skalen-Bildgebung, klinische Diagnostik