Clear Sky Science · de
Quantifizierung der PET‑Aktivierung im Fettgewebe aus nicht-kontastverstärkten CT‑Scans
Warum das Scannen von Fett ohne zusätzliche Strahlung wichtig ist
Ärztinnen und Ärzte wissen, dass nicht jedes Körperfett gleich ist. Eine spezielle Form, das braune Fett, hilft beim Energieverbrauch und steht in Zusammenhang mit besserer Herz‑ und Stoffwechselgesundheit. Die beste Methode, um zu sehen, wie aktiv dieses Fett aktuell ist, ist ein PET‑Scan — dieser ist teuer, zeitaufwendig und verursacht zusätzliche Strahlung. Diese Studie stellt eine einfache, aber folgenreiche Frage: Lässt sich dieselbe Information mit Hilfe künstlicher Intelligenz aus gewöhnlichen CT‑Scans gewinnen, die viele Patientinnen und Patienten ohnehin erhalten, sodass das fehlende metabolische Bild „ergänzt“ werden kann?
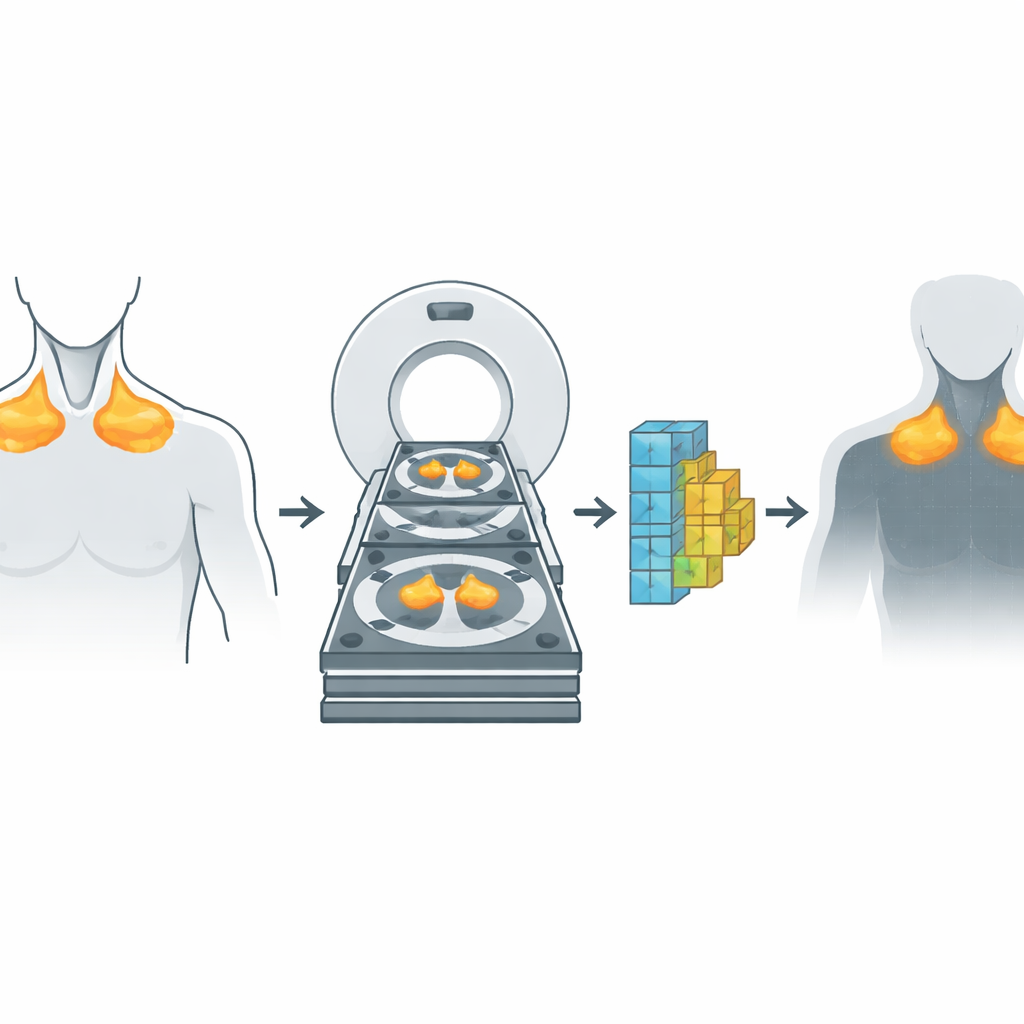
Zwei Scan‑Arten, ein schlaueres Bild
PET‑ und CT‑Scans liefern sehr unterschiedliche Informationen. CT zeigt die detaillierte Anatomie: Knochen, Organe und Fettstrukturen mit hoher Auflösung. PET zeigt Funktion und hebt Bereiche hervor, in denen Zellen Zucker verbrauchen — ein Indikator für metabolische Aktivität. Traditionell verlassen sich Ärzte auf PET, um aktives braunes Fett zu erkennen, weil es beim Verbrennen von Treibstoff stark aufleuchtet. Die Forschenden haben diese Welten zusammengeführt, indem sie gepaarte PET/CT‑Scans von zwei Erwachsenengruppen sammelten — eine kohortenbasiert zur Untersuchung von braunem Fett und eine weitere aus Patientinnen und Patienten mit Lungenkrebs. Für jede Person brachten sie die PET‑ und CT‑Bilder sorgfältig in Übereinstimmung, sodass jeder Punkt im Körper in Struktur und Funktion übereinstimmte, mit besonderem Augenmerk auf Fett im Nacken und um die obere Brust‑Aorta, wo braunes Fett häufig vorkommt.
Ein neuronales Netz beibringen, PET zu imitieren
Mithilfe dieser gepaarten Bilder trainierte das Team eine Form von Tiefenlernmodell, ein sogenanntes konditionales Generative Adversarial Network. Im Kern baten sie das Netzwerk, eine Reihe von CT‑Schnitten anzusehen und zu erzeugen, wie ein PET‑Bild im gleichen Bereich aussehen würde. Das Modell wurde darauf abgestimmt, nur auf Fett zu achten und Gewebe innerhalb des für Fett typischen Dichtebereichs zu isolieren. Durch die Fokussierung auf Fett allein reduzierten sie Ablenkungen durch benachbarte Strukturen wie Herz, Lymphknoten oder Tumore. Sie evaluierten außerdem verschiedene Trainingsstrategien: ein Modell nur mit der Braunes‑Fett‑Kohorte, ein zweites nur mit der Lungenkrebs‑Kohorte und ein drittes, das beide kombinierte, um zu prüfen, wie gut jede Vorgehensweise auf neue Patientinnen und Patienten generalisiert.
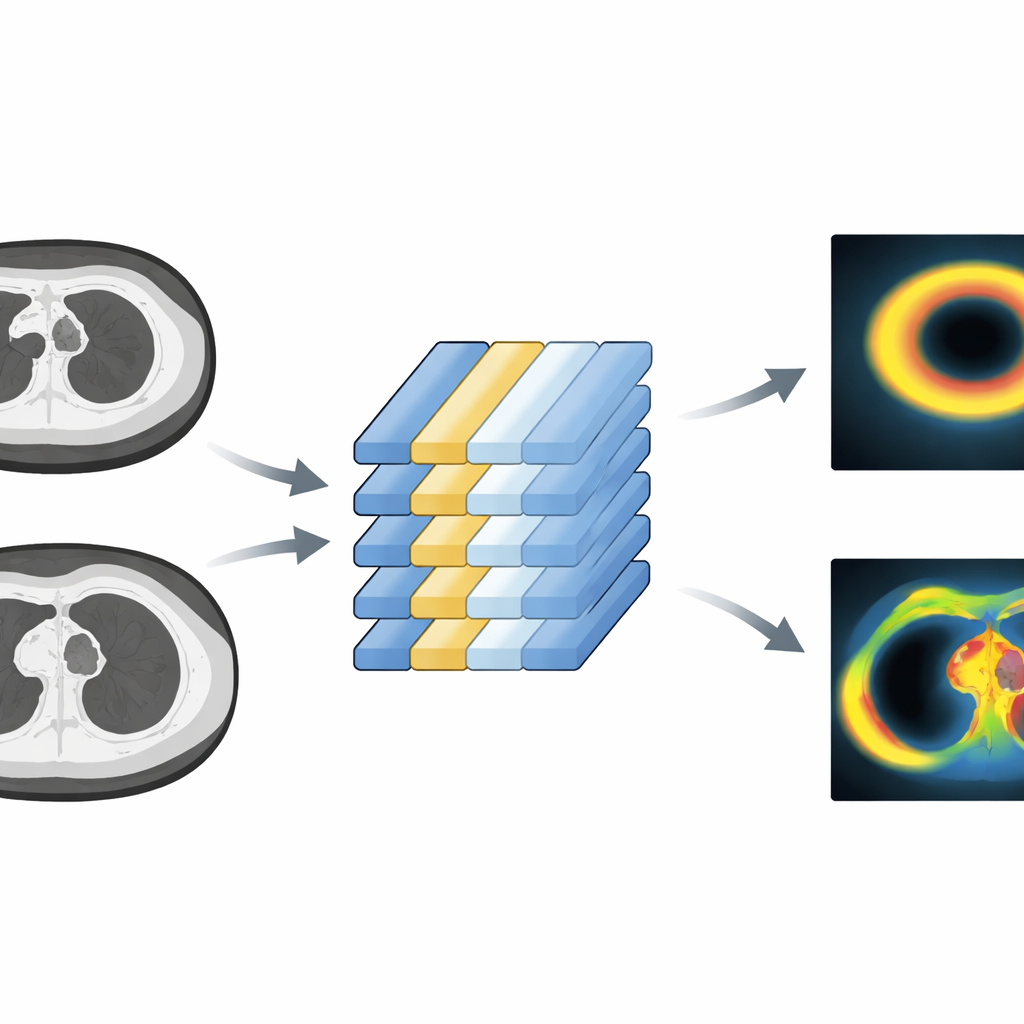
Wie nah ist das synthetische PET am Original?
Um den Erfolg zu bewerten, verglichen die Forschenden die vom Modell vorhergesagte metabolische Aktivität im Fett mit den tatsächlichen PET‑Messungen. Sie verwendeten mehrere statistische Tests, die sowohl einzelne Bildpunkte als auch Mittelwerte über definierte Fettregionen betrachteten. Insgesamt folgten die Vorhersagen den realen PET‑Werten gut, mit kleinen mittleren Abweichungen und relativ starken Korrelationen sowohl im Nacken als auch im oberen Brustbereich. Die Übereinstimmung hielt nicht nur innerhalb des für das Training genutzten Datensatzes, sondern auch, als das Modell an der unabhängigen Lungenkrebs‑Kohorte getestet wurde — trotz der größeren Heterogenität in Bildqualität und Patientenmerkmalen dieser Scans. Eine zusätzliche Analyse, bei der kleine CT‑Bildbereiche selektiv unscharf gemacht wurden, zeigte, dass die Beeinträchtigung fettreicher Bereiche die Modellleistung am stärksten verschlechterte. Das deutet darauf hin, dass das Modell gelernt hat, sich auf physiologisch sinnvolle Strukturen und nicht auf irrelevanten Hintergrund zu stützen.
Grenzen, Vorbehalte und offene Fragen
Die Methode ist nicht perfekt, und die Autorinnen und Autoren benennen ihre Grenzen vorsichtig. Die Leistung sank etwas in der heterogeneren Lungenkrebs‑Gruppe, vermutlich aufgrund unterschiedlicher Scan‑Protokolle und dem Vorhandensein von Tumoren und Entzündungen, die ebenfalls PET‑Signale verändern. Das Modell versucht nicht, braune Fettaktivität von anderen Aufnahmequellen innerhalb des Fetts zu trennen, und es wurde nur an zwei Körperregionen trainiert; sein Verhalten in anderen Körperbereichen bleibt daher unbekannt. Kleine Fehlanpassungen zwischen PET und CT können das Netzwerk ebenfalls in die Irre führen, insbesondere wenn starke PET‑Signale benachbarter Gewebe im Trainingsbild in Fett „auslaufen“. Schließlich verbesserten gängige Bildtricks, etwa das Umformen der Helligkeitsverteilung von PET‑Werten, um seltene Hotspots sichtbarer zu machen, nicht die Ergebnisse und destabilisierten manchmal das Training. Deshalb hielten die Forschenden an standardisierten, physiologisch aussagekräftigen PET‑Maßen fest.
Was das für Patientinnen, Patienten und künftige Versorgung bedeutet
Trotz dieser Unsicherheiten zeigt die Studie, dass Routine‑CT‑Scans ohne Kontrastmittel in PET‑ähnliche Karten der metabolischen Aktivität im Fett verwandelt werden können, ohne radioaktiven Tracer zu injizieren. Diese Fähigkeit könnte den Weg für groß angelegte Studien ebnen, die untersuchen, wie aktive Fettdepots mit Gewichtskontrolle, Diabetes und Herzkrankheiten zusammenhängen — und zwar unter Nutzung jener Scans, die viele Patientinnen und Patienten bereits aus anderen Gründen erhalten. Während das aktuelle Werkzeug eher forschungsorientiert als diagnostisch ausgelegt ist, weist es in eine Zukunft, in der ein einziger Struktur‑Scan stillschweigend auch ein Fenster zur Gewebefunktion öffnet und Ärztinnen und Ärzten hilft zu verstehen, nicht nur wie viel Fett eine Person hat, sondern wie „lebendig“ dieses Fett ist.
Zitation: Cano-Espinosa, C., Subrize, M.W., Franquet, E. et al. Quantification of PET activation in adipose tissue from non-contrast CT scans. npj Digit. Med. 9, 209 (2026). https://doi.org/10.1038/s41746-026-02392-0
Schlüsselwörter: braunes Fettgewebe, Tiefenlernbildgebung, PET CT, metabolische Gesundheit, Körperzusammensetzung