Clear Sky Science · de
Entschlüsselung der ERS–CAF‑immunregulatorischen Achse mittels multimodaler KI und ihr pan‑kanzerogener prognostischer und therapeutischer Vorhersagewert
Blick in Tumoren ohne Skalpell
Krebsärzte erkennen zunehmend, dass das Umfeld eines Tumors genauso wichtig sein kann wie der Tumor selbst. Wiederholte Probenentnahmen dieses verborgenen Umfelds per Biopsie sind jedoch invasiv und oft unpraktisch. Diese Studie zeigt, wie künstliche Intelligenz (KI) routinemäßige medizinische Scans und Mikroskopbilder lesen kann, um schwer messbare immunologische und narbenähnliche Prozesse innerhalb von Tumoren zu erschließen und so alltägliche Bildgebung potenziell in eine Art „digitale Biopsie“ zu verwandeln, die über verschiedene Krebsarten hinweg anwendbar ist.
Die verborgenen Stütz‑Zellen, die Krebs formen
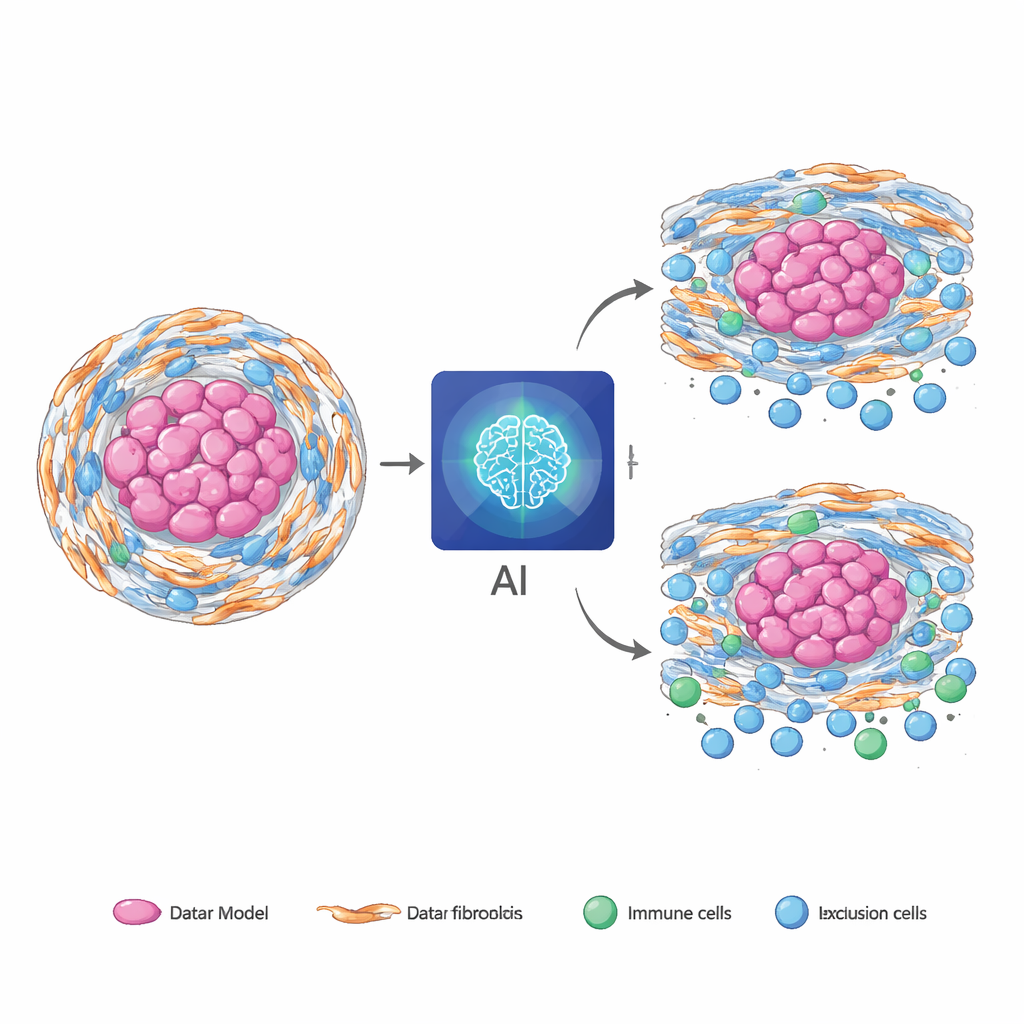
Viele solide Tumoren sind von einer dichten, faserigen Hülle umgeben, die von spezialisierten Stütz‑Zellen, den Fibroblasten, gebildet wird. Sind diese Zellen im endoplasmatischen Retikulum unter Stress, nehmen sie einen aggressiven, den Krebs fördernden Zustand an. Beim Chordom, einem seltenen Knochentumor, bauen diese gestressten Fibroblasten eine dichte Matrix auf und halten Immunzellen fern, wodurch Therapien weniger effektiv werden. Ähnliche fibrotische, immun‑arme Umgebungen treten auch bei anderen Tumoren wie Bauchspeicheldrüsen‑ und kolorektalen Tumoren auf, was darauf hindeutet, dass diese Biologie nicht auf eine einzige Erkrankung beschränkt ist. Das Problem ist, dass aktuelle Methoden zur Messung dieser gestressten Fibroblasten und ihres immune‑blockierenden Verhaltens auf Gewebeproben und komplexen molekularen Tests beruhen, die schwer zu wiederholen sind und wichtige Regionen des Tumors übersehen können.
Der KI beibringen, unsichtbare Biologie zu sehen
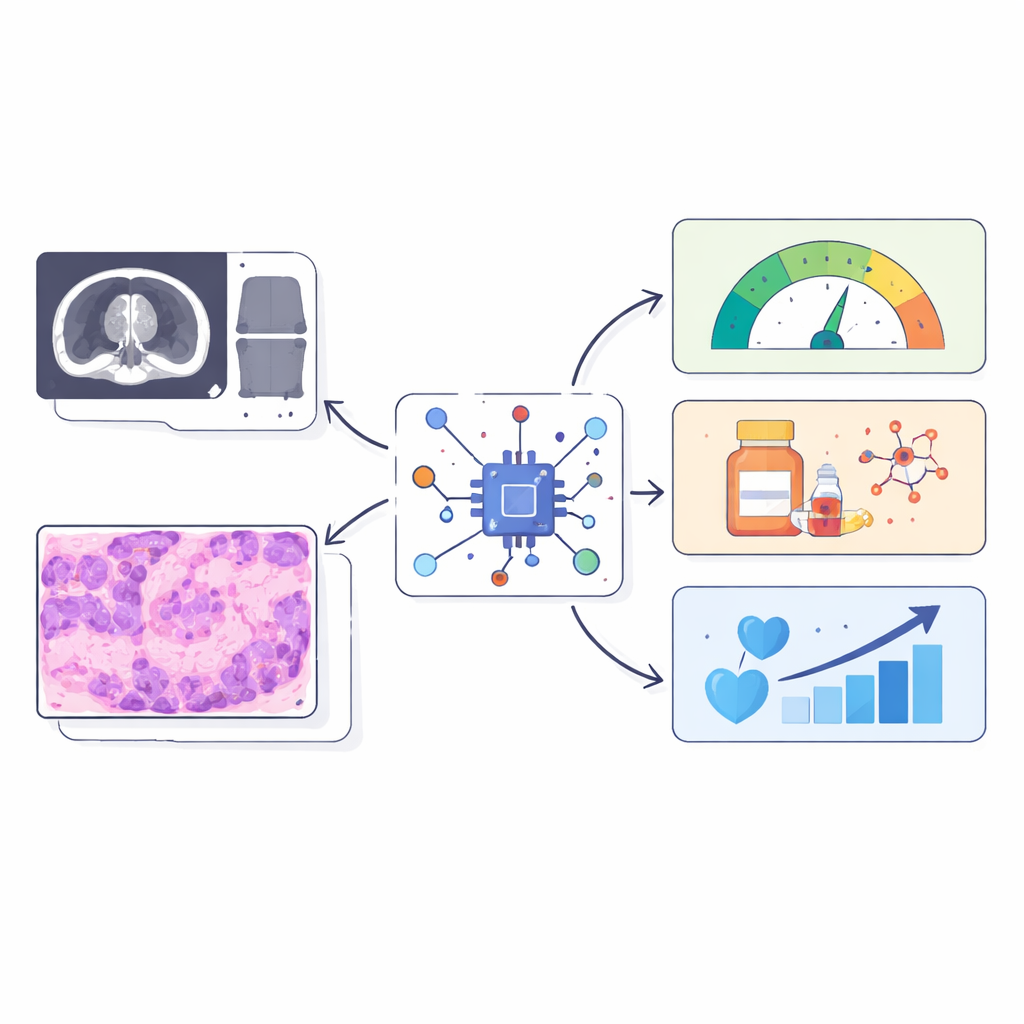
Die Forschenden fragten, ob Standard‑MRT‑Aufnahmen vor einer Operation und routinemäßige H&E‑Pathologie‑Präparate bereits visuelle Hinweise auf diese gestresste‑Fibroblasten‑Immunbarriere enthalten. Sie erstellten drei numerische „Referenz‑Scores“ aus Tumor‑RNA‑Sequenzierungsdaten: einen, der erfasst, wie aktiv das Stressprogramm in Fibroblasten ist, einen, der zusammenfasst, wie stark diese Zellen offenbar mit Immunzellen kommunizieren, und einen, der die Vielfalt der umgebenden Immun- und Stütz‑Zellpopulationen beschreibt. Statt Tausende Gene vorherzusagen, wurde die KI darauf trainiert, nur diese drei biologisch aussagekräftigen Scores allein aus Bildern zu prognostizieren. Dafür kombinierten die Forschenden zwei Zweige: einen, der MRT‑Textur‑ und Formmerkmale analysiert, und einen anderen, der tausende kleiner Regionen auf dem digitalen Schnitt scannt und einen sprachgesteuerten Aufmerksamkeitsmechanismus verwendet, um Bereiche zu fokussieren, die Expertenbeschreibungen von fibrotischem, immunarmen Gewebe entsprechen.
Scans und Schnitte verschmelzen für stärkere Signale
Bei 126 Chordom‑Patienten mit abgeglichenen MRT‑Bildern, Pathologie‑Präparaten, RNA‑Daten und Follow‑up übertraf das fusionierte KI‑Modell Modelle, die nur MRT oder nur Schnitte nutzten. Seine Vorhersagen der drei molekularen Scores stimmten eng mit den RNA‑basierten Messungen überein und blieben über verschiedene Krankenhäuser und Scanner hinweg gut kalibriert. Als Pathologen unabhängig fibrotische und immun‑ausgeschlossene Regionen markierten, leuchteten die KI‑„Hotspots“ tendenziell in denselben Bereichen auf, was nahelegt, dass sie echte biologische Merkmale und nicht nur Tumorgröße erfasste. Das Modell erfasste auch Prognoseinformationen: höhere vorhergesagte Stress‑Fibroblasten‑ und Signal‑Scores waren mit schlechterem Überleben verbunden, während größere vorhergesagte Mikroumgebungs‑Vielfalt einen teilweisen Schutz bot. Die Hinzunahme dieser KI‑abgeleiteten Scores zu routinemäßigen klinischen Faktoren verbesserte die Fähigkeit, Hoch‑ und Niedrigrisiko‑Patienten im Zeitverlauf zu trennen.
Von seltenen Tumoren zu häufigen Krebsarten
Ein zentraler Test war, ob ein ausschließlich in Chordom trainiertes Modell „wie es ist“ in anderen, häufigeren Krebsarten verwendet werden kann. Ohne weiteres Fein‑Tuning angewandt auf Bauchspeicheldrüsen‑, Magen‑ und kolorektale Tumoren aus großen öffentlichen Datensätzen zeigte die nur‑Schnitt‑Version des Modells weiterhin eine sinnvolle Übereinstimmung zwischen ihren bildbasierten Vorhersagen und neu berechneten RNA‑basierten Scores. In einigen dieser Krebsarten verbesserten die KI‑Scores die Vorhersage des Patientenüberlebens gegenüber Standardklinikinformationen und halfen zu unterscheiden, welche Patienten eher von einer Chemotherapie profitieren würden. Um den Einsatz dort zu erleichtern, wo digitale Pathologie begrenzt ist, destillierte das Team das vollständige multimodale Modell in eine nur‑MRT‑Version, die den Großteil der Vorhersagekraft behielt, dabei schneller lief und weniger Rechenressourcen benötigte.
Was das für Patienten bedeuten könnte
Zusammengefasst stützen die Ergebnisse die Idee, dass routinemäßige medizinische Bilder stillschweigend Informationen über gestresste Stütz‑Zellen, Immun‑Ausschluss und Mikroumgebungs‑Vielfalt kodieren — Merkmale, die normalerweise teure molekulare Tests erfordern. Auch wenn die aktuelle Arbeit retrospektiv ist und prospektive Bestätigung braucht, deutet sie auf eine Zukunft hin, in der eine Standardaufnahme und ein Routinepräparat nichtinvasiv Tumoren mit einer feindlichen, fibrotischen Immunbarriere markieren können, zeigen, welche Patientinnen und Patienten von zusätzlichen Tests oder maßgeschneiderten Therapien profitieren könnten, und das über mehrere Krebsarten hinweg, ohne zusätzliche Belastung für die Betroffenen.
Zitation: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Schlüsselwörter: Tumormikroumgebung, Krebsbildgebung, künstliche Intelligenz, Fibroblasten, Immuntherapie