Clear Sky Science · de
Algorithmische Antibiotika-Entscheidungsfindung bei Harnwegsinfektionen unter Verwendung verschreibungsbezogener Vorhersagen des Nutzens der Behandlung
Intelligentere Antibiotika für häufige Infektionen
Harnwegsinfektionen (HWI) gehören zu den häufigsten Gründen, warum Menschen Antibiotika erhalten. Die Wahl des richtigen Wirkstoffs ist jedoch ein Balanceakt: Ärztinnen und Ärzte müssen die Infektion heilen, schwere Nebenwirkungen vermeiden und gleichzeitig die Gesellschaft vor zunehmender Antibiotikaresistenz schützen. Diese Studie stellt eine neue Art von Entscheidungsalgorithmus vor, der Klinikerinnen und Kliniker unterstützen soll, indem er groß angelegte Krankenhausdaten mit den realen Prioritäten der verschreibenden Ärzte kombiniert und so hilft, Antibiotika auszuwählen, die sowohl für den einzelnen Patient wirksam als auch für die breitere Gemeinschaft schonender sind.
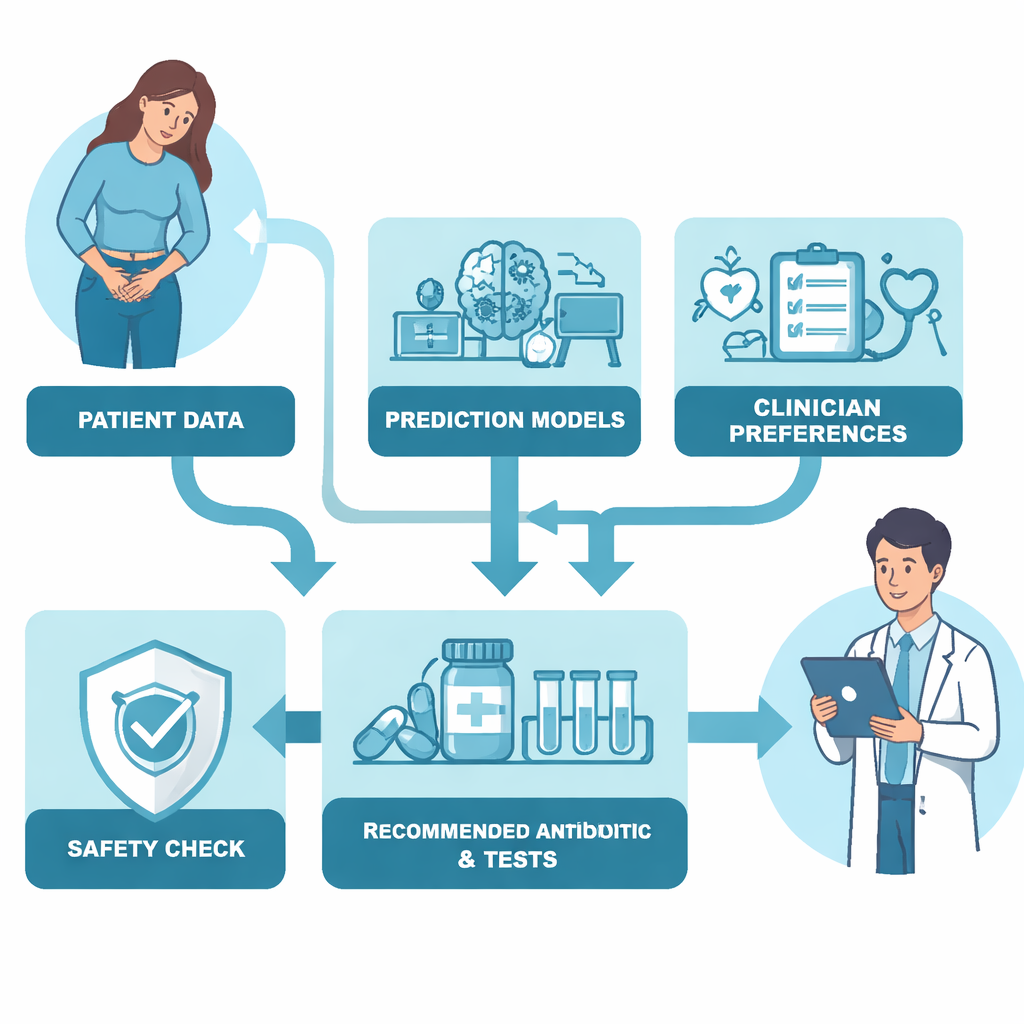
Das Problem mit starken Wirkstoffen
Die moderne Medizin ist auf Antibiotika angewiesen, doch der Übergebrauch breit wirksamer „Großkaliber“-Medikamente treibt eine globale Krise der antimikrobiellen Resistenz voran. Die Vereinten Nationen haben ein Ziel gesetzt: Bis 2030 sollen 70 % des weltweiten Antibiotikaeinsatzes aus schmaler wirkenden, first-line‑Medikamenten stammen, den sogenannten „Access“-Antibiotika der Weltgesundheitsorganisation. In der Praxis tendieren viele Behandler zu breiter wirkenden Mitteln, die als „Watch“ oder „Reserve“ eingestuft sind, weil sie befürchten, dass eine engere Option bei resistenten Erregern versagen könnte, insbesondere bei sehr kranken Patienten. Dadurch tauschen wir oft langfristige Resistenzrisiken gegen kurzfristige Sicherheit ein, ohne klare Werkzeuge, die beurteilen, wann ein sichereres, schmaleres Antibiotikum tatsächlich genauso gut wirken würde.
Dem Algorithmus beibringen, wie ein Kliniker zu denken
Die Forschenden entwickelten einen Antibiotika‑Entscheidungsalgorithmus für HWI auf Basis detaillierter elektronischer Daten von fast 94.000 hospitalisierten Patienten in Boston. Zunächst trainierten sie Vorhersagemodelle, um für 13 verschiedene Antibiotika abzuschätzen, wie wahrscheinlich es ist, dass die HWI‑auslösenden Bakterien empfindlich sind, und wie wahrscheinlich die Behandlung Probleme wie Clostridioides-difficile‑Infektion oder schwere Arzneitoxizität auslöst. Anschließend baten sie 49 britische Klinikerinnen und Kliniker aus verschiedenen Fachrichtungen, eine Online‑Rangliste auszufüllen, in der sie sich zwischen fiktiven Antibiotika mit unterschiedlichen Eigenschaften wie Nebenwirkungsrisiko, Eignung für HWI, Kosten, Access‑ oder Watch/Reserve‑Kategorie und oraler oder intravenöser Verabreichung entscheiden sollten. Durch die Analyse dieser Rangierungen quantifizierte das Team, wie stark Ärzte und Ärztinnen jede Eigenschaft bewerten — zum Beispiel wie sehr sie UTI‑spezifische, wenig toxische orale Medikamente gegenüber riskanteren oder stärker wirkenden Optionen bevorzugen.
Ein Sicherheitsnetz für sehr kranke Patienten
Der finale Algorithmus verband diese beiden Bestandteile: datengestützte Vorhersagen und die Werturteile der Kliniker. Für jeden Patienten berechnete er einen „Behandlungswert“ für jedes Antibiotikum, wobei die vorhergesagte Wahrscheinlichkeit, dass das Mittel wirkt, die Wahrscheinlichkeit schwerer Nebenwirkungen, die Access/Watch/Reserve‑Kategorie und die orale bzw. intravenöse Darreichungsform berücksichtigt wurden. Entscheidend war, dass der Algorithmus auch einen Sicherheitsmechanismus auf Basis des Schweregrads der Erkrankung im Emergency Department einbaute. Mit zunehmender Schwere der Erkrankung legte der Algorithmus automatisch mehr Gewicht auf eine aggressive Behandlung und auf die Verfügbarkeit einer intravenösen Option. Anders ausgedrückt: Bei leicht erkrankten Patienten versuchte er, schmale, orale Arzneien zu bevorzugen; wurden Patienten jedoch schwerer krank, war er zunehmend bereit, stärkere, intravenöse Antibiotika zu empfehlen, um Versagen der Behandlung zu verhindern.
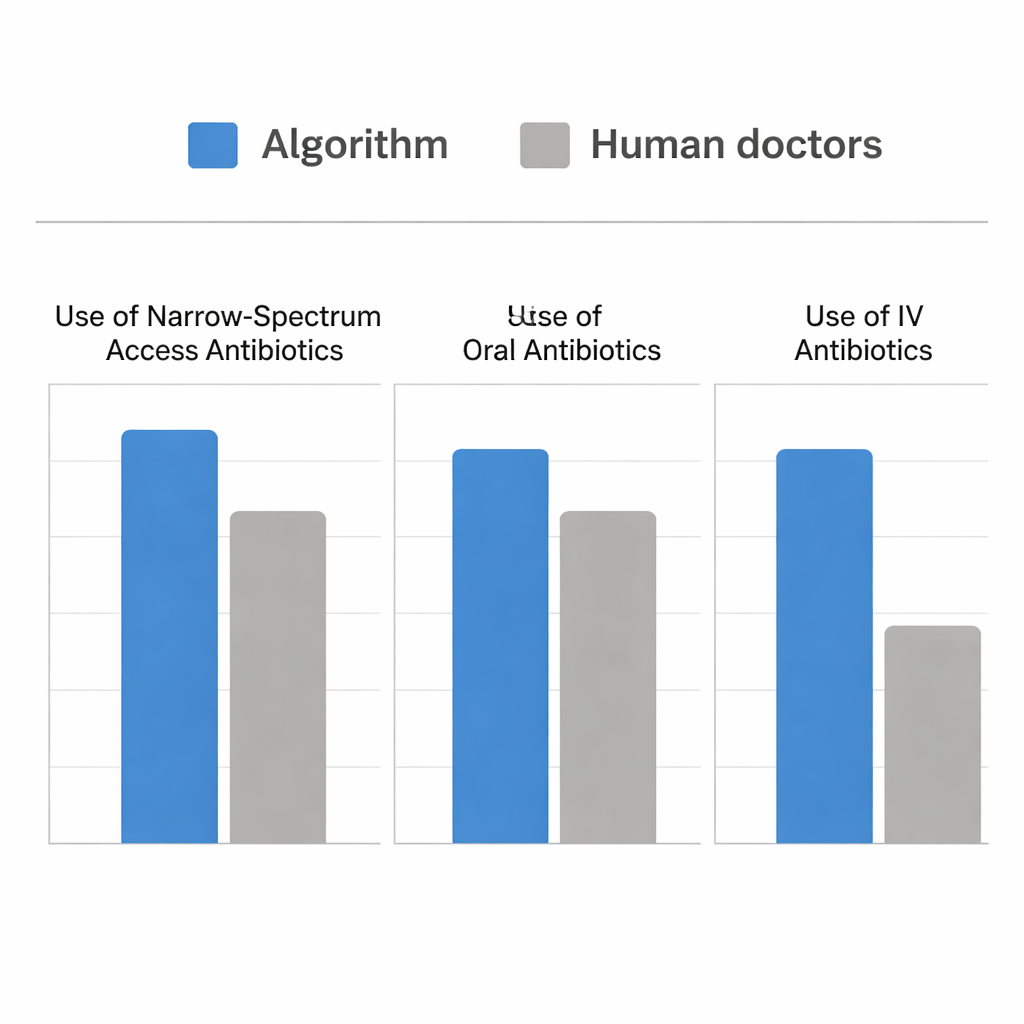
Wie der Algorithmus im Vergleich zu Ärzten abschnitt
Das Team führte anschließend eine Simulation mit realen Fällen aus der Notaufnahme durch, bei denen Patienten HWI hatten und Urinkulturen entnommen wurden. Sie verglichen die Antibiotika, die menschliche Behandler tatsächlich verabreicht hatten, mit den Medikamenten, die der Algorithmus zum Zeitpunkt der Kulturenwahl empfohlen hätte. Beide Ansätze waren ähnlich gut darin, ein Antibiotikum zu wählen, das die Erreger des Patienten abdeckte. Der Algorithmus tat dies jedoch, während er deutlich häufiger schmal wirkende Access‑Medikamente und deutlich mehr orale Behandlungen auswählte und weniger intravenöse Antibiotika verwendete. Bei schwereren Patienten verhielt sich der Algorithmus ähnlich wie menschliche Verschreiber und verlagerte die Empfehlungen angemessen in Richtung intravenöser und stärker wirkender Mittel. Wo er sich unterschied, war in der Erkennung zusätzlicher Gelegenheiten — besonders bei mäßig erkrankten Patienten — sicher mit oralen Access‑Medikamenten wie Nitrofurantoin und Ampicillin‑Sulbactam zu behandeln, anstatt reflexartig zu breiteren Optionen zu greifen.
Was das für die tägliche Versorgung bedeutet
Für eine fachlich interessierte Leserschaft ist die Kernbotschaft, dass dieses System Ärztinnen und Ärzte nicht ersetzt; vielmehr wirkt es wie ein Rechner für komplexe Risiko‑Nutzen‑Abwägungen, die Kliniker bereits berücksichtigen, die sich aber nicht exakt im Kopf berechnen lassen. Indem es die Prioritäten der Behandler mit großflächigen Evidenzen zur Leistung von Antibiotika verknüpft, kann der Algorithmus Behandlungen vorschlagen, die für einzelne Patienten ebenso wirksam sind, aber schonender für den Körper und die öffentliche Gesundheit — Pillen statt Tropf, wenn es sicher ist, und schmalere Wirkstoffe statt letzter Reserve, wo immer möglich. Wenn solche Werkzeuge in weiteren Umgebungen validiert werden, könnten sie Krankenhäuser und Gesundheitssysteme näher an globale Ziele für verantwortungsvollen Antibiotikaeinsatz bringen, ohne die Sicherheit von Menschen zu gefährden, die mit schwerer Infektion eintreffen.
Zitation: Howard, A., Green, P.L., Zhong, Y. et al. Algorithmic antibiotic decision-making in urinary tract infection using prescriber-informed prediction of treatment utility. npj Digit. Med. 9, 136 (2026). https://doi.org/10.1038/s41746-026-02369-z
Schlüsselwörter: Harnwegsinfektion, Antibiotika‑Stewardship, klinische Entscheidungsunterstützung, antimikrobielle Resistenz, Maschinelles Lernen in der Medizin