Clear Sky Science · de
Annotierungsfreie 3D-Rekonstruktion und Quantifizierung der retinalen Mikrovaskulatur mit RADAR
Gesundheit durch das Augenhintergrund sehen
Die winzigen Blutgefäße im Augenhintergrund tun weit mehr, als nur die Netzhaut zu versorgen. Da sie nichtinvasiv sichtbar sind, dienen sie als lebende Landkarte der kleinen Blutgefäße des Körpers und liefern frühe Hinweise auf Erkrankungen wie Diabetes, Nierenerkrankungen und Herzprobleme. Diese Studie stellt eine neue Rechenmethode vor — RADAR — die Augen-Scan-Daten in detaillierte dreidimensionale Modelle dieser feinen Gefäße verwandelt, ohne auf arbeitsintensive manuelle Beschriftung oder empfindliches KI-Training angewiesen zu sein. 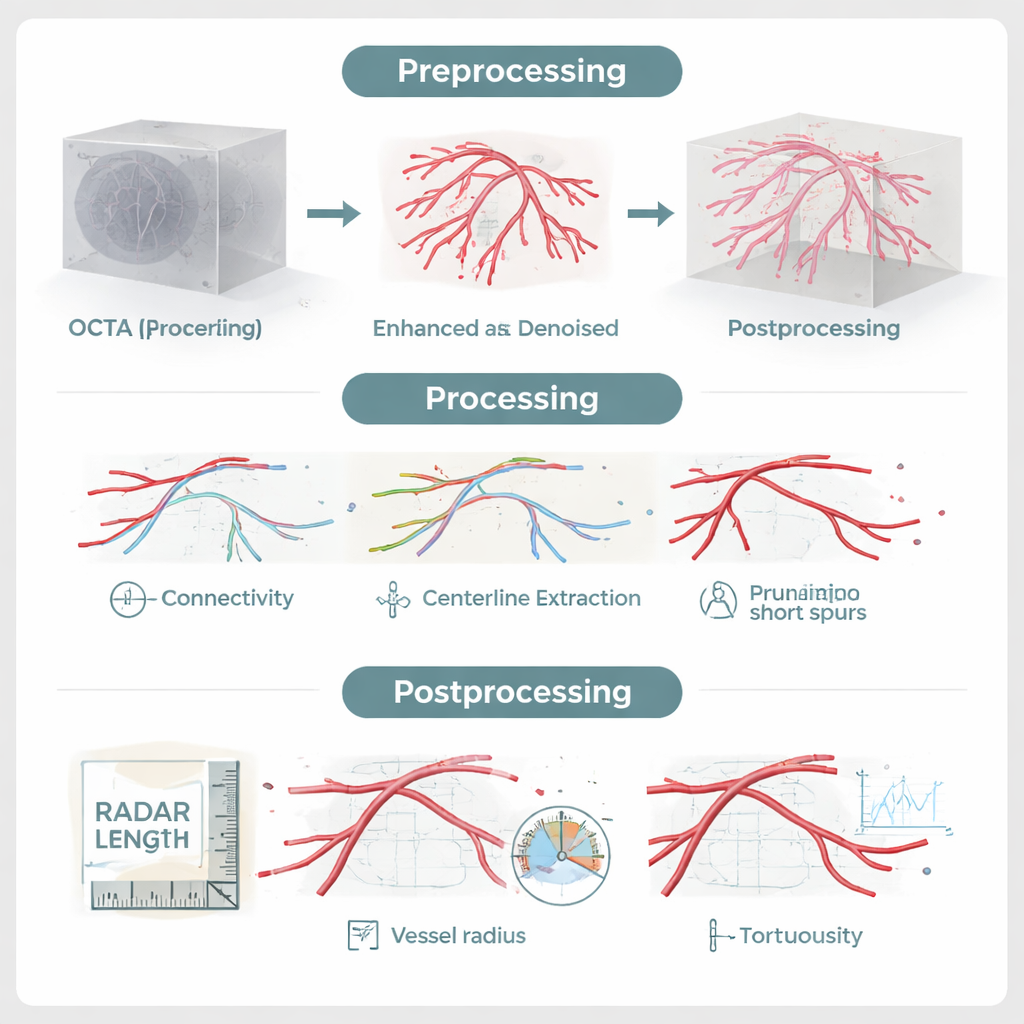
Warum flache Bilder wichtige Hinweise verbergen
Moderne Augen-Scanner, bekannt als optische Kohärenztomographie-Angiographie (OCTA), können ein vollständiges 3D-Volumen des Blutflusses in der Netzhaut erfassen. In der Klinik werden diese umfangreichen Datensätze jedoch meist zu flachen, von oben betrachteten Bildern komprimiert. Wenn alle Gefäßschichten auf eine Ebene zusammengedrückt werden, überlagern sich Strukturen in unterschiedlichen Tiefen, kleine Lücken werden verdeckt und subtile Verluste von Kapillaren können unsichtbar werden. Das ist eine ernste Einschränkung, denn frühe Schäden durch Diabetes und andere Erkrankungen beginnen oft in den feinsten Kapillaren, lange bevor deutliche Zeichen einer Retinopathie oder ein Sehverlust auftreten.
Eine Karte, die auf physikalischen Prinzipien statt auf Vermutungen beruht
Die meisten jüngeren Versuche, das Gefäßnetz aus OCTA-Scans zu extrahieren, haben sich dem Deep Learning zugewandt, wobei neuronale Netze Muster aus tausenden vorbeschrifteten Beispielen lernen. Diese Ansätze können gut funktionieren, bringen aber Nachteile mit sich: Sie erfordern große, sorgfältig annotierte Datensätze, können versagen, wenn Scanner oder Bildgebungsprotokoll wechseln, und verhalten sich oft wie eine "Black Box". RADAR geht anders vor. Es ist eine modellbasierte Pipeline, die kodiert, wie Gefäße in drei Dimensionen aussehen und sich verhalten sollten — kontinuierliche, gebogene Röhren, die verzweigen und sich wieder verbinden — statt zu versuchen, alles allein aus Daten zu lernen. Ein spezialisierter Rauschfilter verstärkt Signale von röhrenförmigen Strukturen, während ihre Krümmungen erhalten bleiben, und ein Konnektivitätsschritt nutzt wahrscheinlichkeitbasierte Pfade, um durch Lärm oder Bewegungsartefakte verursachte Unterbrechungen zu überbrücken, geleitet von der lokalen Gefäßrichtung statt einfachen Helligkeitsschwellen.
Von Pixelgewirr zu messbaren Netzwerken
Sobald die Gefäße verstärkt und wieder verbunden sind, extrahiert RADAR deren zentrale "Skelettlinie", identifiziert Verzweigungspunkte und Enden und entfernt winzige Stummel, die wahrscheinlich Artefakte sind. Übrig bleibt ein klares 3D-Netz der retinalen Zirkulation. Aus diesem Modell kann die Software direkt klinisch relevante Merkmale messen: wie viele Gefäßsegmente vorhanden sind, deren Gesamtlänge und Oberfläche, mittlere Breite und wie stark sie gewunden (tortuos) sind. Entscheidend ist, dass dies getrennt für die oberflächliche, mittlere und tiefe Schicht der Netzhaut erfolgen kann, nachdem das Gefäßnetz mit der individuellen retinalen Anatomie ausgerichtet wurde. Die Validierung gegen mühsame manuelle 3D-Nachzeichnungen zeigte, dass RADARs Segmentierungen hochgenau sind, und der gesamte Prozess — vom Rohscan bis zum vollständigen Satz von Kennzahlen — dauert etwa sechs Minuten pro Auge. 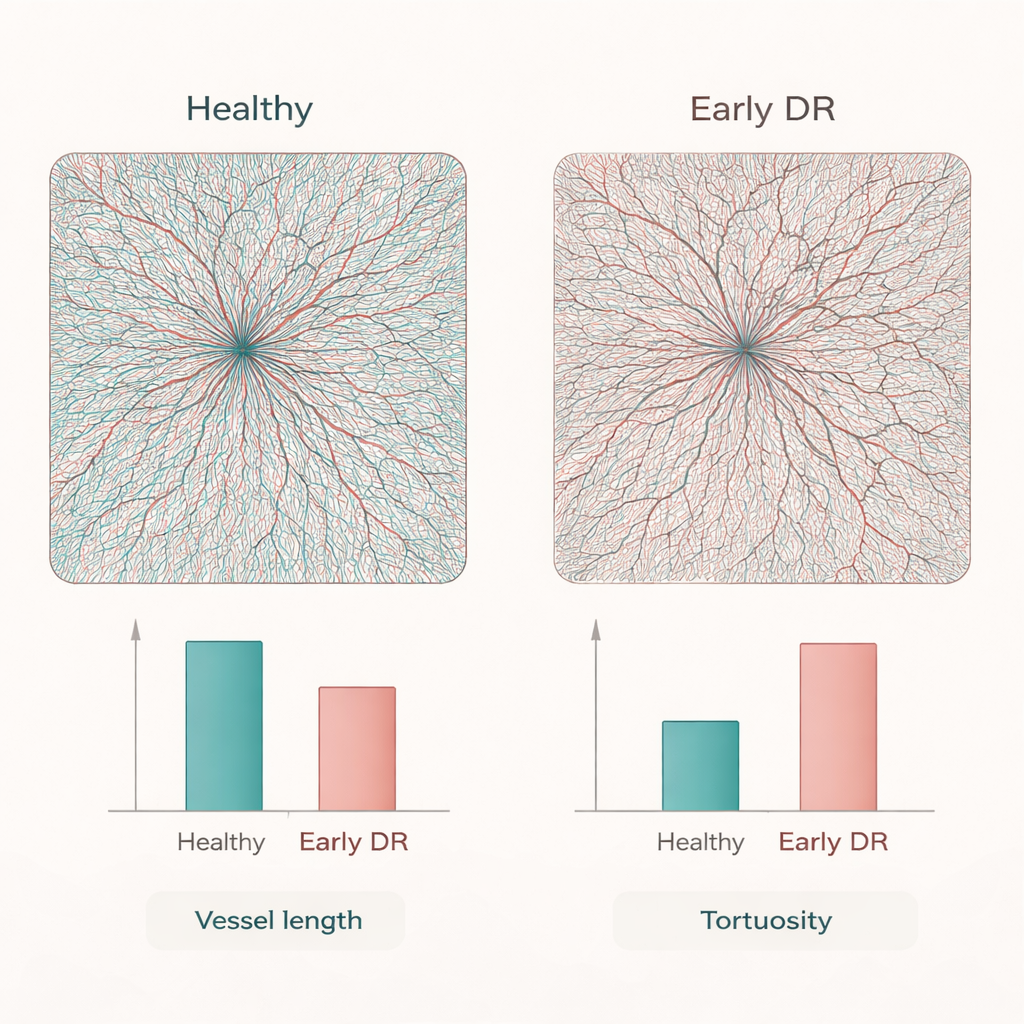
Was sich bei früher diabetischer Augenerkrankung ändert
Um den praktischen Nutzen zu prüfen, wandten die Forscher RADAR auf OCTA-Scans von 50 gesunden Erwachsenen und 50 Patienten mit früher diabetischer Retinopathie an. Auf standardmäßigen flachen Bildern wirkten beide Gruppen ähnlich. Die 3D-Rekonstruktionen hingegen zeigten, dass diabetische Augen bereits weniger und kürzere Gefäßsegmente, eine geringere gesamte Gefäßoberfläche sowie mehr Endpunkte bei weniger Verzweigungen hatten — Anzeichen für Kapillarausfall und ein vereinfachtes Netzwerk. Gleichzeitig waren die verbleibenden Gefäße, insbesondere die kleineren, stärker verdreht. Indem diese Veränderungen in leicht interpretierbare Kennzahlen kondensiert wurden, etwa das Verhältnis von Segmenten zu Verzweigungspunkten oder Tortuositätsmuster nach Gefäßgröße, deckte RADAR krankheitsbedingte Umbauten auf, die mit den aktuellen 2D-Methoden wahrscheinlich übersehen würden.
Was das für Patienten bedeuten könnte
Für Nicht-Spezialisten ist die Kernbotschaft: Diese Technik verwandelt Augen-Scans in eine höchst detaillierte 3D-Karte der kleinsten Blutgefäße und macht frühe Schäden sichtbar, lange bevor das Sehvermögen betroffen ist. Da sie nicht auf menschliche Beschriftung oder ein erneutes Training für jeden neuen Scanner angewiesen ist, könnte RADAR in Kliniken skaliert werden, um die mikrovaskuläre Gesundheit über die Zeit zu überwachen, Ärzten helfen, diabetische Augenerkrankungen früher zu erkennen, und potenziell Risiken für umfassendere kardiovaskuläre Probleme signalisieren. Langfristig könnten solche 3D-"vaskulären Fingerabdrücke" aus dem Auge zu routinemäßigen Markern werden, die Prävention und Behandlung lange vor irreversiblen Schäden leiten.
Zitation: Zhang, H., Liu, X., Wu, J. et al. Annotation-free 3D reconstruction and quantification of retinal microvasculature by RADAR. npj Digit. Med. 9, 181 (2026). https://doi.org/10.1038/s41746-026-02366-2
Schlüsselwörter: retinale Mikrovaskulatur, OCTA, 3D-Rekonstruktion, diabetische Retinopathie, vaskuläre Biomarker