Clear Sky Science · de
LLM-gesteuertes Kollaborationsframework zur wissensgestützten Beurteilung und Behandlung von Tumorschmerzen
Warum klügere Schmerzversorgung wichtig ist
Tumorschmerz ist nicht nur eine unangenehme Begleiterscheinung – er kann die letzten Monate oder Jahre eines Menschen beherrschen und Schlaf, Bewegung und selbst einfache Gespräche erschweren. Obwohl starke Schmerzmittel existieren, ist deren sichere und wirkungsvolle Anwendung schwierig, zumal bei jedem Patienten Krebs, Begleiterkrankungen und Medikamente unterschiedlich sind. Dieser Artikel beschreibt OncoPainBot, ein neues KI-Framework, das auf großen Sprachmodellen (LLMs) basiert und Ärztinnen und Ärzten helfen soll, komplexe Befunde zu sichten, aktuelle Leitlinien zu berücksichtigen und sicherere, individuellere Schmerzpläne für Menschen mit Krebs zu entwerfen.
Ein schwieriges Problem in der täglichen Krebsversorgung
Schmerz bei Krebs hat viele Ursachen: Tumoren, die auf Knochen oder Nerven drücken, Operationen, Chemotherapie und Strahlentherapie. Bis zu 70 % der Menschen mit fortgeschrittenem Krebs leiden unter relevanten Schmerzen, doch die Linderung bleibt oft unvollständig. Ärztinnen und Ärzte müssen Opioide, nicht-opioide Medikamente und ergänzende Therapien gegeneinander abwägen und gleichzeitig gefährliche Nebenwirkungen im Blick behalten, insbesondere bei Patienten mit eingeschränkter Leber- oder Nierenfunktion. Aktuelle Schmerzbewertungsinstrumente stützen sich stark auf kurze Skalen und Freitextnotizen, die von einem Kliniker zum nächsten und von einem Krankenhaus zum anderen variieren können. Das führt dazu, dass Behandlungsentscheidungen stark schwanken und Chancen zur Verbesserung des Komforts übersehen werden können.
Medizinischen Text in verwertbare Erkenntnisse verwandeln
LLMs wie ChatGPT und Claude können lange, unübersichtliche Dokumente lesen und zusammenfassen, weshalb sie für medizinische Aufgaben attraktiv sind. Gewöhnliche "Chatbots" sind für Tumorschmerz jedoch unsicher, weil sie Details erfinden, Wechselwirkungen übersehen oder neueste Leitlinien ignorieren können. OncoPainBot begegnet diesen Problemen, indem es LLMs mit einer kuratierten Wissensbasis verknüpft, die Leitlinien großer onkologischer Organisationen enthält, und die Arbeit in vier kooperierende "Agenten" aufteilt, die jeweils eine reale klinische Rolle widerspiegeln. Ein Agent extrahiert Schlüsselinformationen zum Schmerz aus elektronischen Akten, ein anderer beurteilt die zugrundeliegende Schmerzart, ein dritter entwirft einen Behandlungsplan und ein vierter führt eine Sicherheitsüberprüfung durch, die sich auf Wechselwirkungen, Organfunktion und Überwachungsbedarf konzentriert.
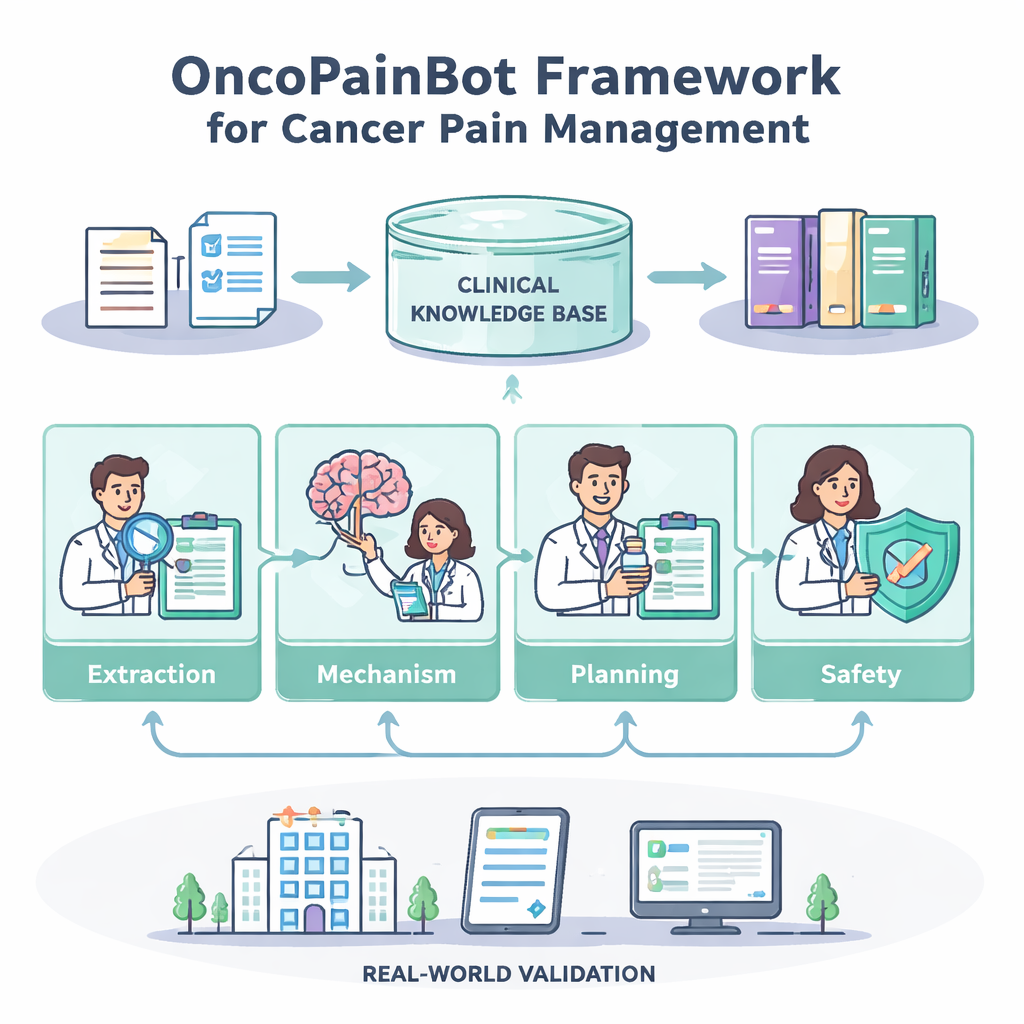
Wie das Vier-Agenten-Team arbeitet
Der Pain-Extraction-Agent liest Freitextnoten und verwandelt sie in ein strukturiertes Bild: wo der Schmerz liegt, wie stark er empfunden wird, was ihn bessert oder verschlechtert und welche Medikamente bereits versucht wurden. Der Pain-Mechanism-Reasoning-Agent nutzt dieses Bild, um abzuleiten, ob der Schmerz hauptsächlich durch Gewebeschaden, Nervenschädigung oder eine Mischung verursacht wird – ein wichtiger Hinweis für die Wahl der geeigneten Medikamente. Anschließend konsultiert der Treatment-Planning-Agent die leitlinienbasierte Wissensbasis mittels einer Technik namens retrieval-augmented generation, die dem Modell erlaubt, spezifische, aktuelle Passagen einzubeziehen, statt sich allein auf sein internes Wissen zu stützen. Er schlägt schrittweise Pläne vor – typischerweise orientiert an der WHO‑"Schmerzlinderungstreppe" –, einschließlich Anfangsdosen, Anpassungsstrategien und Notfallgaben für akute Schmerzspitzen. Schließlich agiert der Safety-Check-Agent wie ein vorsichtiger Apotheker: Er prüft auf Dosierungsprobleme, riskante Kombinationen und fehlende Laborwerte und markiert Fälle, in denen die Datenlage zu dünn ist, um eine verbindliche Empfehlung abzugeben.
Wie das System getestet wurde
Um das beste zugrunde liegende Sprachmodell zu wählen, verglichen die Forschenden sieben führende Systeme in mehreren medizinischen Frage-Antwort-Tests. Claude 4 erwies sich als am genauesten, wenn auch nicht als das schnellste, und wurde daher als "Gehirn" von OncoPainBot ausgewählt. Sie evaluierten dann verschiedene Wege, dieses Gehirn mit der Leitlinienbibliothek zu verbinden, und stellten fest, dass eine "Hybrid"-Retrieval-Strategie – mit Stichwortabgleich und tieferer semantischer Suche kombiniert – die zuverlässigsten Antworten lieferte. Mit dieser Konfiguration setzten sie OncoPainBot auf 516 reale Tumorschmerzfälle eines großen chinesischen Krankenhauses an. Die schriftlichen Berichte des Systems stimmten in Sprache und Inhalt eng mit den Notizen der Kliniker überein, und seine Therapieempfehlungen deckten sich in etwa 84 % der Fälle mit den tatsächlichen Verordnungen. Wichtig ist, dass die meisten Abweichungen aus subtilen, patientenspezifischen Nuancen resultierten – etwa nicht dokumentierter Opioid-Toleranz oder komplexem Organversagen – und nicht aus offensichtlich falschen Medikamentenwahl.
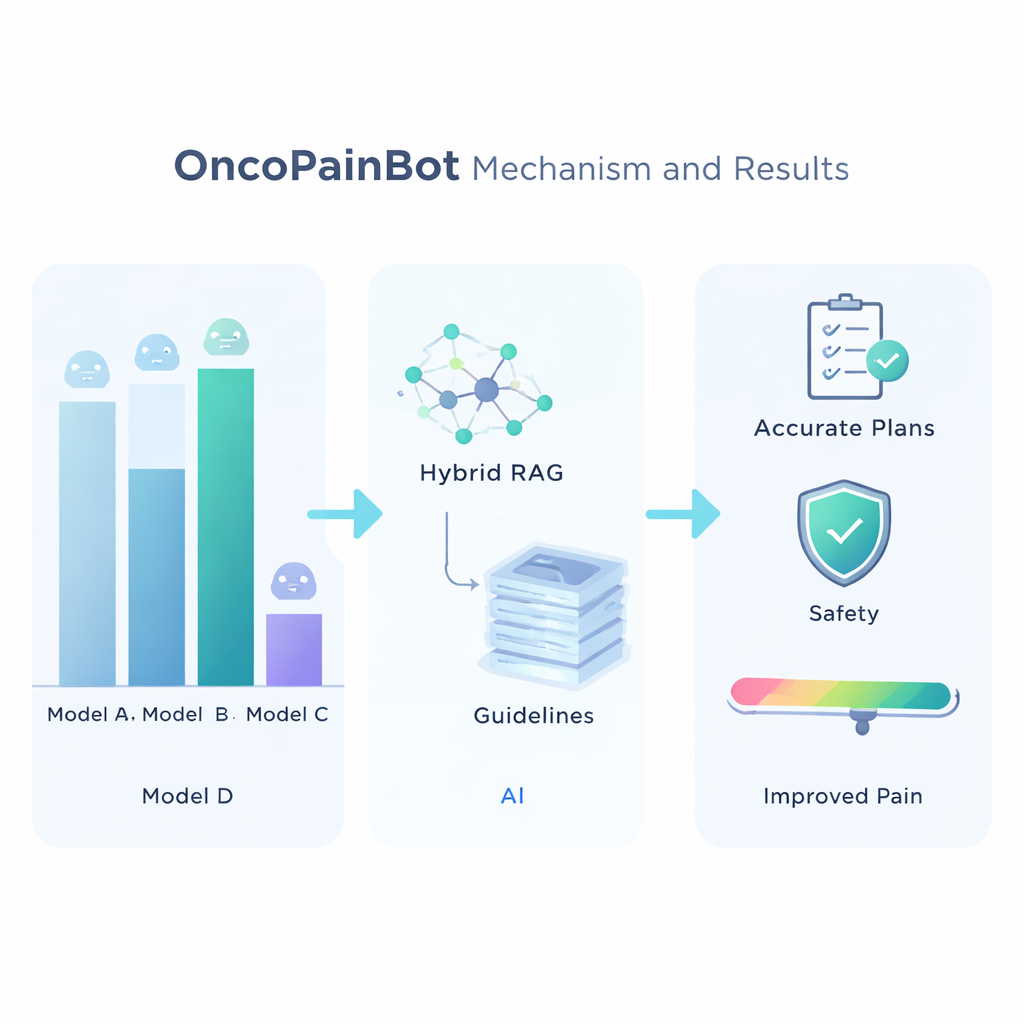
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit Krebs liegt das Versprechen von OncoPainBot nicht darin, dass eine Maschine die Behandlung übernimmt, sondern darin, dem Behandlungsteam eine präzisere, konsistentere zweite Meinung zu liefern. Das Framework ist als "Clinician-in-the-loop"-Tool konzipiert: Es hebt Schmerzmerkmale hervor, die in den Notizen verborgen bleiben könnten, schlägt leitlinienkonforme Optionen vor und weist auf Sicherheitsrisiken hin, während die endgültige Entscheidung bei den behandelnden Ärztinnen und Ärzten bleibt. Die Autorinnen und Autoren betonen, dass ihre Arbeit noch in einem frühen, retrospektiven Stadium ist und bislang nur in einem Zentrum getestet wurde; Echtzeit-Studien über mehrere Krankenhäuser sind noch erforderlich. Dennoch deuten die Ergebnisse darauf hin, dass sorgfältig gestaltete KI – fundiert auf belastbarer Evidenz und transparenter Argumentation – dazu beitragen könnte, die Schmerzversorgung bei Krebs zu standardisieren, gefährliche Dosierungsfehler zu reduzieren und vor allem dafür zu sorgen, dass Patienten weniger Zeit mit Leiden und mehr Zeit mit Leben verbringen.
Zitation: Liu, H., Hu, Y., Li, D. et al. LLM-driven collaborative framework for knowledge-enhanced cancer pain assessment and management. npj Digit. Med. 9, 180 (2026). https://doi.org/10.1038/s41746-026-02362-6
Schlüsselwörter: Schmerzmanagement bei Krebs, klinische Entscheidungsunterstützung, große Sprachmodelle, Opioidtherapie, retrieval-augmented generation