Clear Sky Science · de
HMC-Transducer: hierarchischer Mamba‑CNN‑Transducer für robuste Lebertumorsegmentierung
Warum bessere Tumorkarten wichtig sind
Bei Patientinnen und Patienten mit Leber‑ oder Nierenkrebs verlassen sich Ärztinnen und Ärzte auf CT‑Scans, um zu entscheiden, ob Operationen, Bestrahlung oder andere Behandlungen möglich sind. Ein zentraler Schritt besteht darin, in drei Dimensionen präzise Konturen um jeden Tumor zu zeichnen — eine Aufgabe, die von Hand langsam, mühsam und inkonsistent ist. Diese Arbeit stellt ein neues KI‑System vor, das diese Tumoren automatisch genauer und gleichmäßiger nachzeichnen kann als frühere Methoden und damit potenziell Klinikern hilft, Behandlungspläne schneller und mit größerer Sicherheit zu erstellen.
Das Ganze im 3D‑Scan sehen
Lebertumoren sind besonders schwer abzugrenzen, weil sie stark in Größe und Form variieren und oft im umliegenden Gewebe verschwimmen. Traditionelle Deep‑Learning‑Werkzeuge wie Convolutional Neural Networks (CNNs) sind sehr gut darin, feine Details in Bildern zu erkennen, haben aber Schwierigkeiten, langfristige Zusammenhänge zu erfassen — also wie eine Struktur in einem Bereich des Scans zu einer weit entfernten Struktur in Beziehung steht. Neuere Modelle, die sogenannten Transformer, können diesen weiten Kontext erfassen, werden jedoch bei großen 3D‑CT‑Volumina extrem rechenintensiv, was ihre Praktikabilität in echten Kliniken einschränkt. Die Autoren argumentieren, dass ein System sowohl detailorientiert als auch global aufmerksam sein muss, ohne Supercomputer‑ähnliche Rechenleistung zu verlangen.
Ein neues hybrides Gehirn für medizinische Bilder
Um diesem Bedarf gerecht zu werden, entwarfen die Forschenden den HMC‑Transducer, eine hybride Architektur, die CNNs mit einer neueren Modellfamilie namens State‑Space‑Models verbindet, speziell einem Modell namens Mamba. Die CNN‑Teile konzentrieren sich auf scharfe lokale Details wie klare Tumorränder. Die Mamba‑Teile verfolgen, wie sich Informationen über ein ganzes 3D‑Scanvolumen hinweg ausbreiten, und arbeiten dabei mit nur linear wachsendem Rechenaufwand, wodurch die steilen Kostenanstiege von Transformern vermieden werden. Ein speziell entwickelter „richtungsbewusster 3D‑Mamba“‑Block verarbeitet den Scan entlang der drei Achsen — Kopf‑Fuß, links‑rechts und vorne‑hinten — sodass das Modell die echte anatomische Struktur respektiert, statt das Volumen in eine eindimensionale Zahlenfolge zu pressen.
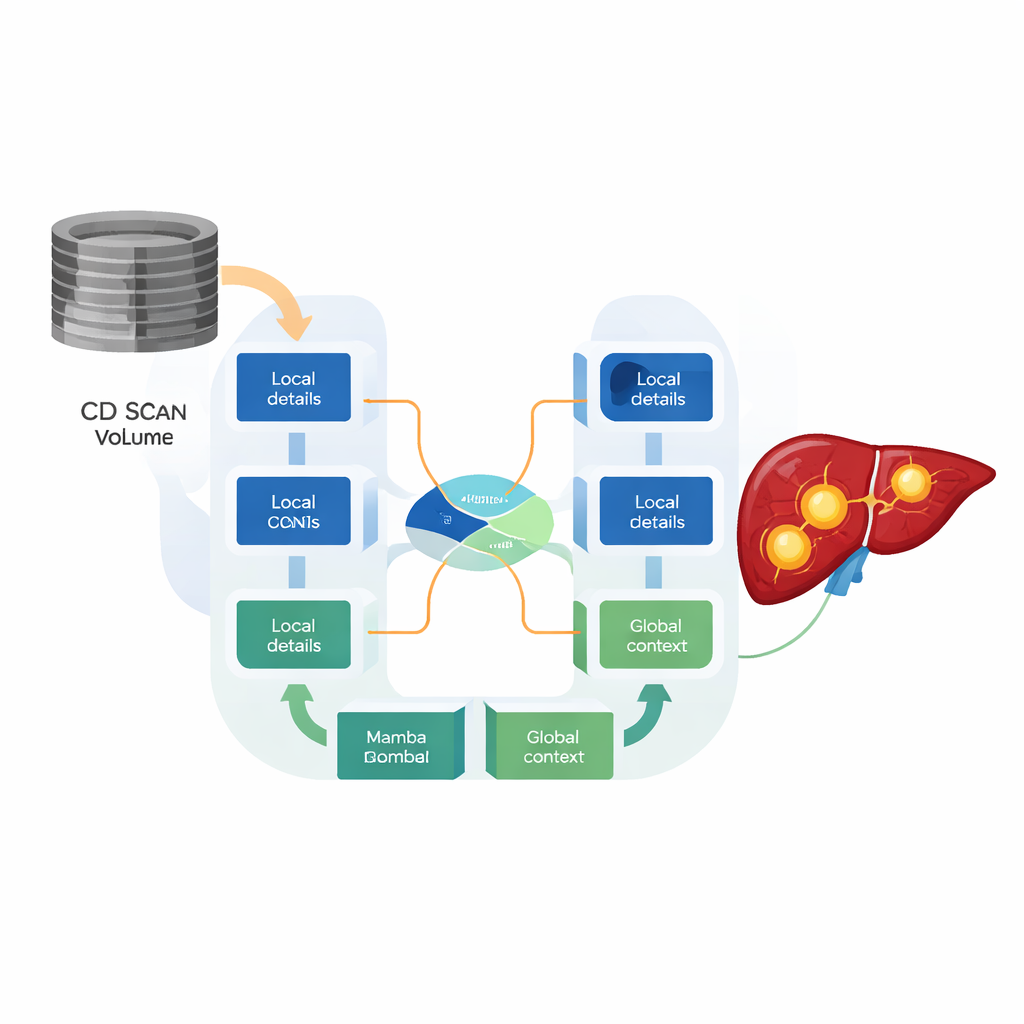
Das Modell entscheiden lassen, was wo zählt
Eine zentrale Innovation ist die Art und Weise, wie diese beiden Merkmalstypen kombiniert werden. Anstatt die CNN‑ und Mamba‑Ausgaben einfach zu addieren oder zu stapeln, nutzt der HMC‑Transducer einen gated Fusion‑Mechanismus, der für jede kleine Region im Scan lernt, wie sehr lokalen Details gegenüber dem globalen Kontext vertraut werden sollte. In Bereichen mit klaren, scharfen Grenzen kann das Gate auf CNN‑Merkmale setzen; sind Tumoren diffus, infiltrativ oder in der Nähe großer Blutgefäße, kann es der breiteren Sicht von Mamba mehr Gewicht geben. Experimente zeigen, dass dieses adaptive Mischen engere, stabilere Segmentierungen liefert als allein CNNs oder Mamba‑basierte Modelle und deutliche Verbesserungen gegenüber früheren hybriden Designs erzielt, die Merkmale auf feste, nicht‑adaptive Weise fusionierten.
Getestet über Organe, Scanner und Krankenhäuser hinweg
Das Team bewertete seinen Ansatz auf drei großen öffentlichen Datensätzen: LiTS17 und MSD‑Liver für Lebertumoren sowie KiTS21 für Nierentumoren. Über diese Benchmarks hinweg erreichte der HMC‑Transducer konsistent eine bessere Überlappung mit von Expertinnen und Experten gezeichneten Tumorkarten als starke Baselines, darunter das weit verbreitete nnU‑Net sowie führende Transformer‑ und Mamba‑Modelle. Er generalisierte auch besser, wenn er auf einem Leberdatensatz trainiert und auf einem anderen, in verschiedenen Krankenhäusern erhobenen Datensatz getestet wurde — ein Szenario, das reale Einsätze mit variierenden Scannern und Bildgebungsprotokollen nachahmt. In direkten Vergleichen lagen große „Foundation Models“ wie SAM und dessen medizinische Varianten, die ohne spezialisiertes Training direkt eingesetzt wurden, deutlich zurück, was unterstreicht, dass aufgabenspezifische, sorgfältig abgestimmte Systeme für pixelgenaue Entscheidungen im medizinischen Kontext weiterhin nötig sind.
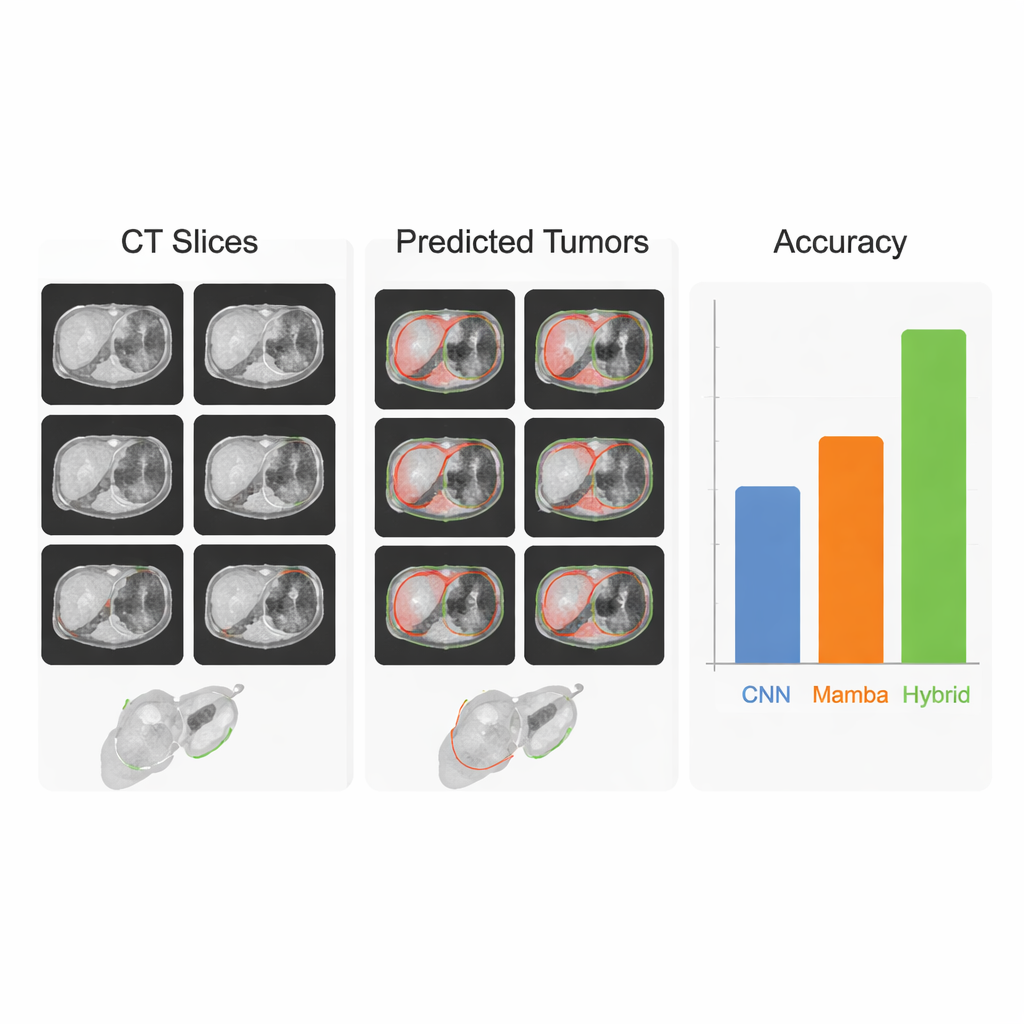
Von Laborergebnissen zur klinischen Hilfe
Für Nicht‑Fachleute lautet die Kernbotschaft: Diese Arbeit bringt die Tumorkartierungs‑Software näher an das, was Ärztinnen und Ärzte tatsächlich brauchen — ein Werkzeug, das sowohl vertrauenswürdig als auch effizient ist. Indem zwei sich ergänzende Sichtweisen kombiniert werden — eine, die bei kleinen Details hervorsticht, und eine, die das große Ganze erfasst — zeichnet der HMC‑Transducer Leber‑ und Nierentumoren genauer und verlässlicher als frühere Systeme, und das bei Ausführung auf standardmäßiger, leistungsstarker Krankenhaushardware. Obwohl vor einer routinemäßigen klinischen Anwendung noch weitere Schritte nötig sind, einschließlich breiterer Tests an anderen Organen und Bildgebungsarten, stellt der Ansatz einen vielversprechenden Fortschritt hin zu automatisierten 3D‑Tumorkarten dar, die schnellere Diagnosen, präzisere Operationen und individuellere Krebsbehandlungen unterstützen könnten.
Zitation: Zhu, J., Xu, C., Lei, C. et al. HMC-transducer: hierarchical mamba-CNN transducer for robust liver tumor segmentation. npj Digit. Med. 9, 176 (2026). https://doi.org/10.1038/s41746-026-02361-7
Schlüsselwörter: Lebertumorsegmentierung, medizinische Bildgebung KI, Tiefes Lernen, CT‑Scan‑Analyse, hybride neuronale Netze