Clear Sky Science · de
Anwendung und Perspektive künstlicher Intelligenz in der bildgebenden Diagnostik des Prostatakarzinoms
Warum intelligentere Untersuchungen für die Männergesundheit wichtig sind
Das Prostatakarzinom gehört zu den häufigsten Krebserkrankungen bei Männern, und ein frühzeitiger Befund kann den Unterschied zwischen einem überschaubaren Gesundheitsproblem und einer lebensbedrohlichen Erkrankung ausmachen. Diese Übersicht erklärt, wie künstliche Intelligenz (KI) in moderne medizinische Bildgebung integriert wird, um Prostatakrebs früher zu entdecken, seine Gefährlichkeit einzuschätzen und den Therapieerfolg zu überwachen. Für Leserinnen und Leser bietet sie einen Einblick, wie Computer stille Partner im Befundungsraum werden, Ärzten helfen, schneller und konsistenter Entscheidungen zu treffen, und zugleich neue Fragen zu Daten, Fairness und Vertrauen aufwerfen.
Von unscharfen Schatten zu datenreichen Bildern
Ärztinnen und Ärzte nutzen mehrere bildgebende Verfahren zur Suche nach Prostatakrebs. Der Ultraschall ist schnell und kostengünstig, hat aber Schwierigkeiten, Krebs von gutartiger Vergrößerung oder Entzündung zu unterscheiden. Die Magnetresonanztomographie (MRT) liefert detailreiche Ansichten von Weichgewebe und ist heute der bevorzugte Test für klinisch relevante Prostatakarzinome, benötigt jedoch Zeit zur Auswertung, und selbst Expertinnen und Experten sind sich oft uneinig. PET/CT-Untersuchungen mit Tracern, die an ein Protein namens PSMA auf Krebszellen binden, eignen sich hervorragend, um Tochtergeschwülste in Knochen und Lymphknoten zu finden, können aber sehr kleine Läsionen übersehen und sind kostenintensiv. KI ersetzt diese Geräte nicht; sie setzt auf die von ihnen erzeugten Bilder auf. Algorithmen bereinigen und segmentieren zunächst die Aufnahmen und extrahieren dann subtile Muster in Helligkeit, Textur und Form. Diese unsichtbaren Hinweise, kombiniert mit Laborbefunden wie PSA-Werten, werden verwendet, um Modelle zu trainieren, die verdächtige Bereiche markieren, das Krebsrisiko schätzen und vorschlagen, wo biopsiert werden sollte oder wie der Therapieansprechen beurteilt werden kann.
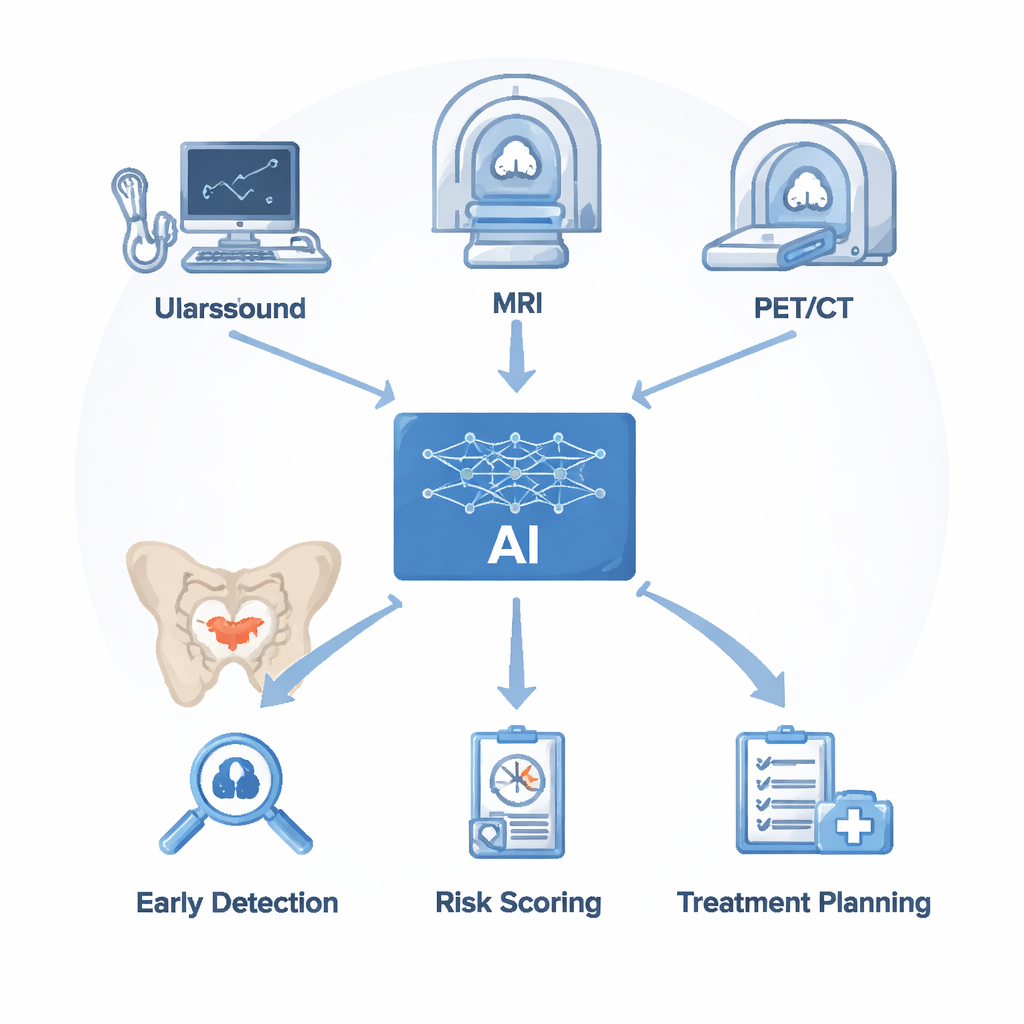
Computern beibringen, das zu sehen, was Radiologinnen und Radiologen übersehen
Beim Ultraschall lernen KI-Systeme aus Hunderten von Beispielen, tumoröse Regionen zu erkennen, die sich in den Hintergrund einfügen können. Deep‑Learning‑Modelle können die Prostata automatisch lokalisieren und wahrscheinliche Tumoren in Echtzeit hervorheben, wobei sie manchmal mit erfahrenen Sonographen gleichziehen oder sie übertreffen, während sie schnell arbeiten und kleine Läsionen seltener übersehen. Radiomics-Ansätze gehen noch einen Schritt weiter und wandeln Ultraschallbilder in große Zahlenmengen um, die Gewebemuster erfassen, die für das menschliche Auge zu komplex sind. Auf diesen Merkmalen basierende Machine‑Learning‑Modelle übertreffen deutlich den herkömmlichen Ultraschall und PSA allein, insbesondere bei Männern mit PSA-Werten in der verwirrenden „Grauzone“, in der ältere Verfahren oft fast die Hälfte der Fälle falsch klassifizieren. Ähnliche Ideen treiben KI in der MRT an, wo fortgeschrittene Netzwerke die Prostata und ihre inneren Zonen automatisch skizzieren, das manuelle Konturieren von rund 20 Minuten auf knapp über eine Minute reduzieren und die Übereinstimmung zwischen verschiedenen Leserinnen und Lesern deutlich verbessern.
Präzisere Risikoabschätzungen und klügeres Therapietracking
KI entfaltet ihre Stärken besonders dann, wenn sie Informationen aus mehreren MRT‑Sequenzen zusammenführt, die Anatomie, Wasserbewegung und Durchblutung zeigen. Transformer‑basierte Modelle, abgeleitet aus der Sprachverarbeitung, verschmelzen diese Eingaben zu Wahrscheinlichkeitskarten klinisch relevanter Tumoren. In Tests an großen Patientengruppen haben solche Systeme mit erfahrenen Radiologinnen und Radiologen gleichgezogen oder sie übertroffen, insbesondere bei kleinen Tumoren unter einem Zentimeter, die Menschen oft übersehen. Bei dynamischen Kontrast‑MRTs können Zeitreihenmodelle die sich ändernden Helligkeitskurven des injizierten Kontrastmittels lesen, um abzuschätzen, wie durchlässig die Blutgefäße des Tumors sind – ein Indikator, der mit aggressiverer Erkrankung und höherem Rückfallrisiko verknüpft ist. In PSMA PET/CT erkennen dreidimensionale Netzwerke, die auf Ganzkörperscans trainiert wurden, automatisch Knochen‑ und Lymphknotenmetastasen, messen die gesamte Tumorlast und setzen sie in Beziehung zur progressionsfreien Überlebenszeit. Andere KI‑Werkzeuge vergleichen Aufnahmen vor und kurz nach Hormon‑ oder Chemotherapie und sagen das Therapieergebnis über mehrere Monate deutlich früher vorher als traditionelle Regeln, die auf einfachen Änderungen der Traceraufnahme beruhen.
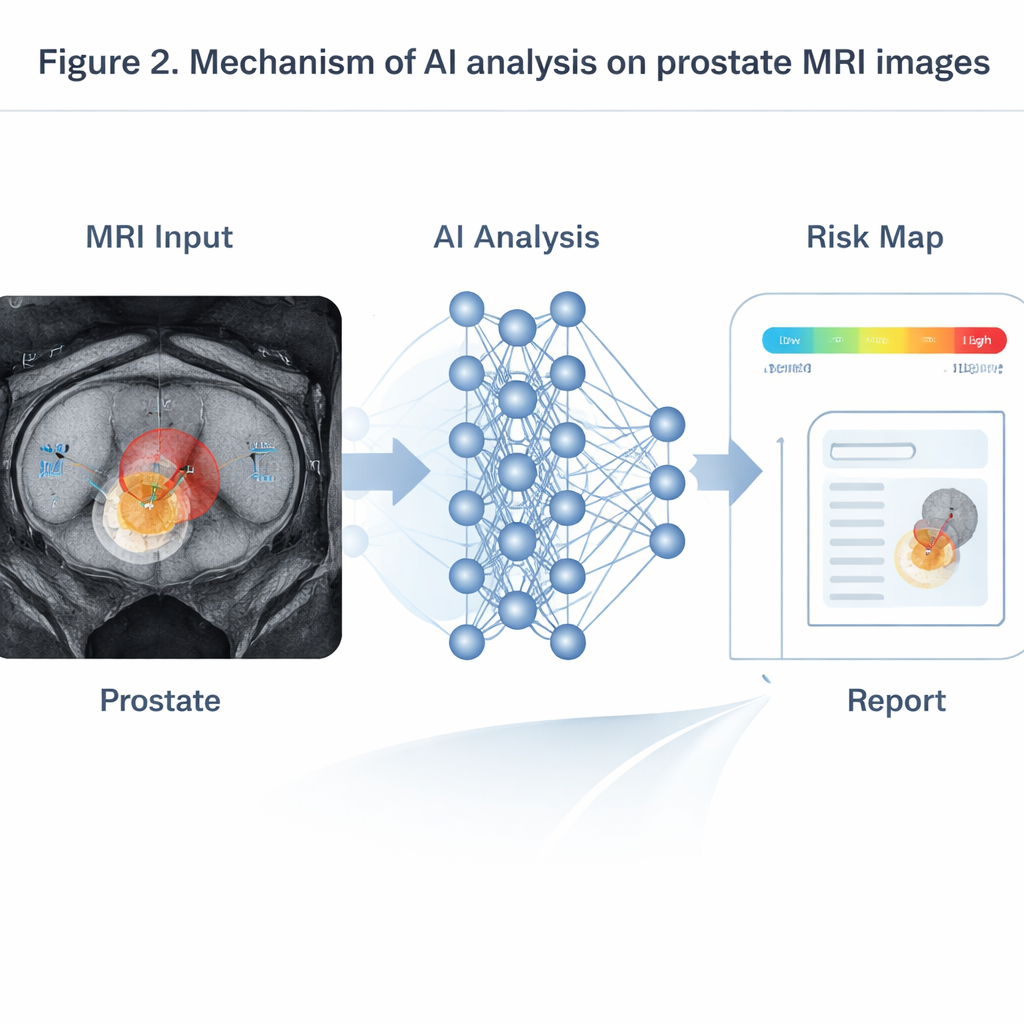
Hindernisse: Datenlücken, Black‑Boxes und gerechte Anwendung
Trotz dieser Fortschritte steht die reale Implementierung vor ernsthaften Hürden. Hochwertige, gut annotierte Bilddaten sind weiterhin begrenzt und zugunsten großer Universitätskliniken verzerrt, während Scans aus kleineren Zentren und vielfältigen Bevölkerungsgruppen unterrepräsentiert sind. Feine Unterschiede zwischen Geräten, Einstellungskonfigurationen und Bildqualität können dazu führen, dass in einem Zentrum trainierte Modelle an anderer Stelle versagen. Viele leistungsfähige KI‑Systeme agieren als „Black Boxes“ und liefern nur eine Risikobewertung ohne klare Erklärung, was das Vertrauen der Ärzte untergräbt – besonders wenn der Computer der eigenen Erfahrung widerspricht. Die Übersicht weist zudem auf Bedenken hinsichtlich Datenschutz, Beschränkungen beim Datenaustausch und das Risiko hin, dass Modelle für bestimmte Gruppen schlechter funktionieren und so gesundheitliche Ungleichheiten vergrößern könnten, wenn sie nicht sorgfältig überwacht und angepasst werden.
Vertrauenswürdige Partner in der Klinik entwickeln
Für die Zukunft sehen die Autorinnen und Autoren KI eher als vertrauenswürdige Teamkollegin denn als rätselhaften Orakel. Sie skizzieren Bestrebungen, große, geteilte Datensätze über Krankenhäuser hinweg aufzubauen und dabei die Privatsphäre mit Techniken wie föderiertem Lernen zu schützen, bei dem nur Modellaktualisierungen – nicht Rohpatientendaten – ausgetauscht werden. Neue „erklärbare KI“-Werkzeuge zielen darauf ab, aufzuzeigen, welche Bildregionen eine Entscheidung beeinflusst haben, und diese mit bekannter Pathologie zu verknüpfen, sodass Ärztinnen und Ärzte greifbare Gründe haben, einer Empfehlung zuzustimmen oder sie zu hinterfragen. Statt Einheitsmodellen werden maßgeschneiderte Systeme einzelne Aufgaben übernehmen: Screening in überfüllten Kliniken, Anleitung von Biopsien, Überwachung der Therapie oder Nachsorge bei Hochrisikopatienten. Die Kombination von Bildgebung mit genetischen und klinischen Daten könnte Prognosen weiter verfeinern und Therapien personalisieren. Für Patientinnen und Patienten lautet die Quintessenz ermutigend: Werden diese technischen, ethischen und regulatorischen Herausforderungen gut bewältigt, könnte KI‑gestützte Bildgebung eine frühere Erkennung, weniger unnötige Biopsien, schnellere Ergebnisse und individuellere Behandlungspläne beim Prostatakrebs bedeuten.
Zitation: Wang, X., Zhong, S., Fang, K. et al. Application and prospect of artificial intelligence in diagnostic imaging of prostate cancer. npj Digit. Med. 9, 168 (2026). https://doi.org/10.1038/s41746-026-02354-6
Schlüsselwörter: Prostatakrebs-Bildgebung, künstliche Intelligenz, MRT und Ultraschall, PSMA PET/CT, Radiomics