Clear Sky Science · de
Maskiertes Autoencoding, generalisierbares Pretraining und integrierte Expertensysteme für verbesserte Gliom-Segmentierung
Warum schlauere Scans bei Hirntumoren wichtig sind
Hirntumoren, die als Gliome bezeichnet werden, gehören zu den tödlichsten Krebsarten, und dennoch verbringen Ärztinnen und Ärzte viel Zeit damit, Tumorgrenzen in MRT-Aufnahmen manuell nachzuzeichnen. Diese sorgfältige Umrandung leitet Operationen und Bestrahlungen, kann aber 15–20 Minuten pro Patient beanspruchen und muss über die Zeit wiederholt werden. Die Studie stellt MAGPIE vor, ein KI‑System, das aus Zehntausenden unlabeled Hirnscans lernt und danach nur eine Handvoll fachgerecht annotierter Fälle benötigt, um Gliome zuverlässig zu kartieren. Für Patientinnen und Patienten könnte das schnellere, konsistentere Therapieplanung bedeuten — selbst in Kliniken ohne große, kuratierte Datensätze.
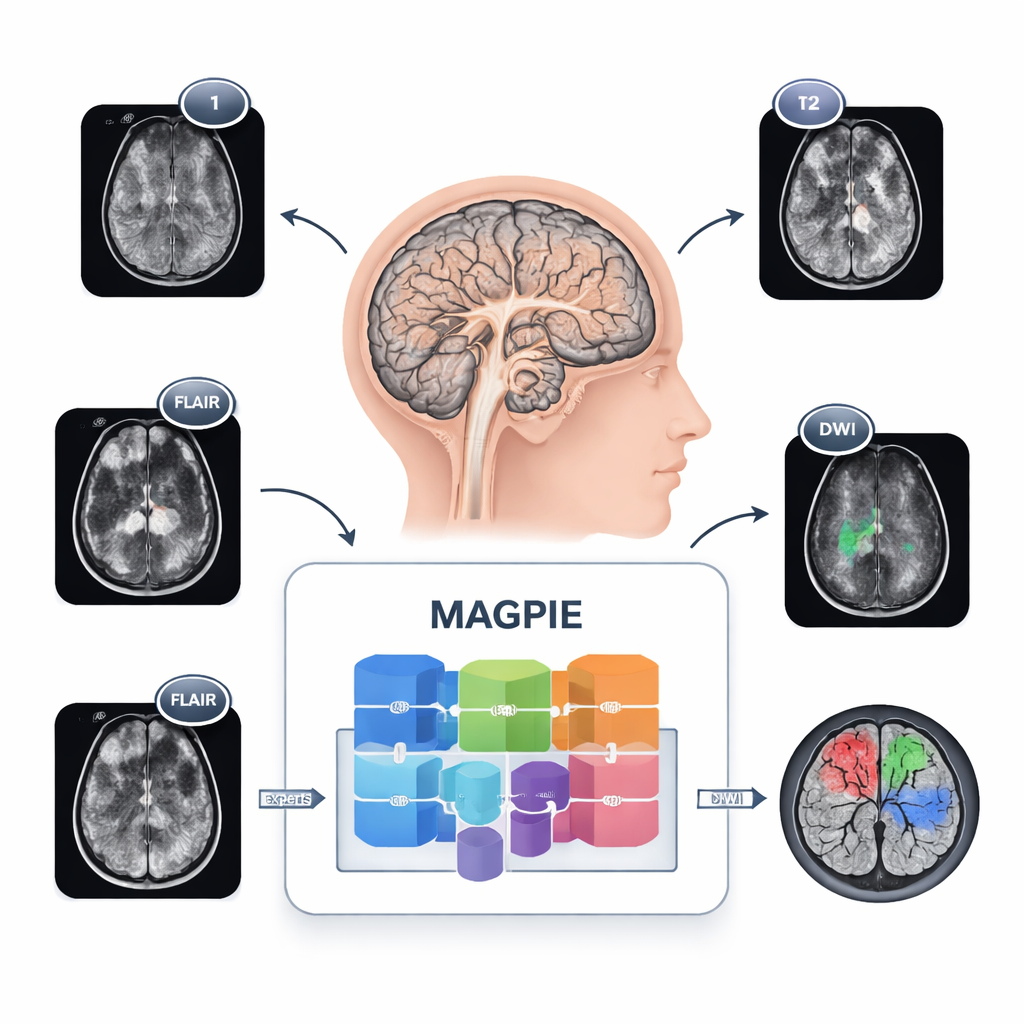
Tumoren neu sehen
Gliome sind schwer abzubilden, weil sie keine sauberen Kugeln bilden. Krebszellen breiten sich entlang neuronaler Bahnen aus, erzeugen unscharfe Ränder und winzige Satellitenherde, die schwer zu erkennen sind. Verschiedene Kliniken verwenden zudem unterschiedliche MRT‑Protokolle und Sequenzkombinationen, sodass ein an einem Ort trainiertes Werkzeug an einem anderen scheitern kann. MAGPIE geht all das gleichzeitig an. Zunächst wurde es mit 43.505 unlabeled Hirn‑MRTs aus vielen Studien und Gerätetypen konfrontiert. In dieser Phase lernte es allgemeine Muster gesunden und erkrankten Hirngewebes, indem es fehlende Bildteile rekonstruierte und verschiedene augmentierte Ansichten desselben Gehirns verglich, wodurch es gezwungen wurde, sich auf stabile, sinnvolle Merkmale statt auf fragile Pixel‑Details zu konzentrieren.
Mehrere Experten teilen sich die Arbeit
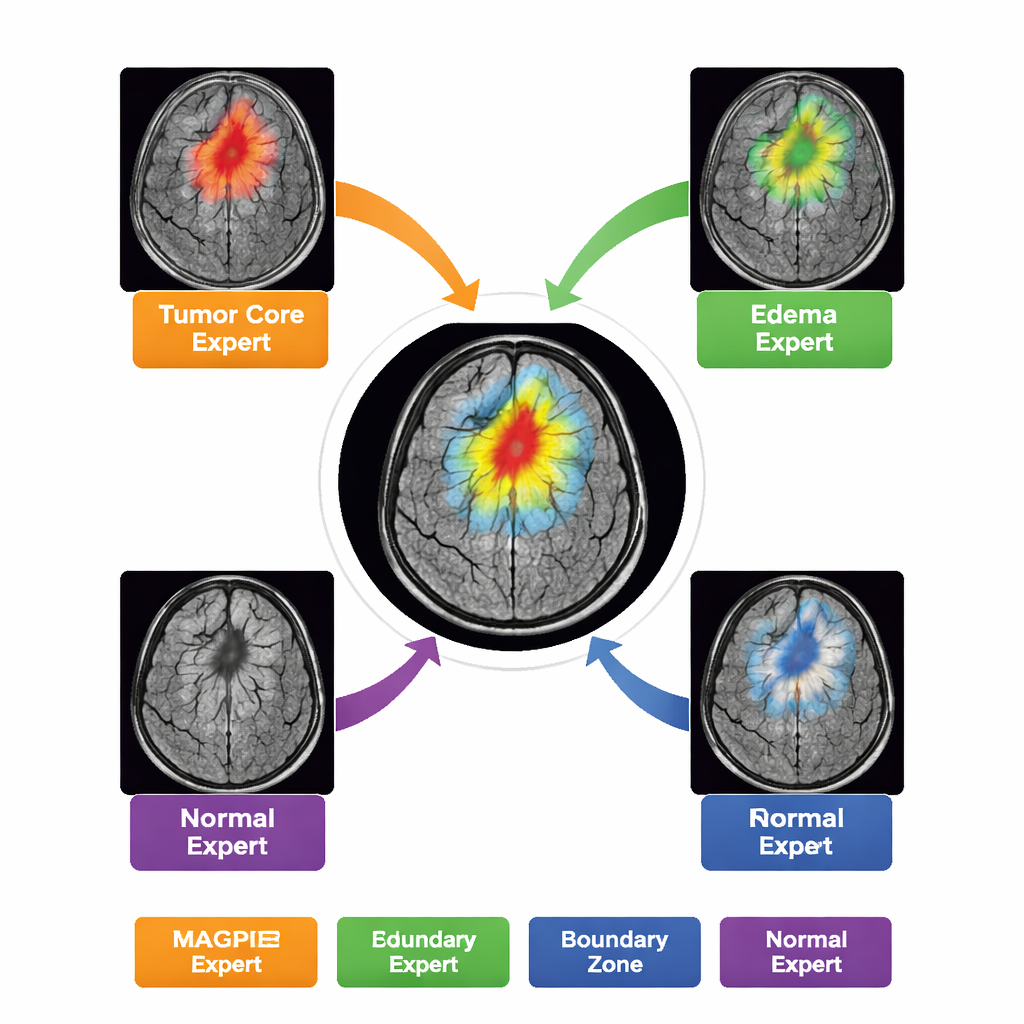
Statt als ein einzelnes, monolithisches Modell aufzutreten, enthält MAGPIE eine "Mixture of Experts" im Inneren. Beim Analysieren eines neuen Scans aktiviert es für jeden Bereich des Bildes nur eine kleine Auswahl von acht spezialisierten Subnetzwerken. Im Training teilen sich diese Experten die Aufgabe auf natürliche Weise: Einige werden empfindlich für den hellen, aktiv wachsenden Tumorrand, andere erkennen den nekrotischen Kern, wieder andere lernen den verschwommenen Rand der Schwellung um den Tumor, und einige konzentrieren sich hauptsächlich auf normales Hirnhintergrundgewebe und Grenzen. Die Autoren zeigen dies, indem sie messen, wie stark die Aktivität jedes Experten mit den verschiedenen von Radiologinnen und Radiologen gezeichneten Tumorzonen überlappt. Diese Arbeitsteilung verbessert die Genauigkeit bei gleichzeitig überschaubarem Rechenaufwand — nur etwa die Hälfte der Modellparameter ist für einen gegebenen Bildausschnitt aktiv.
Umgang mit unordentlichen Real‑World‑Scans
Klinische MRT‑Protokolle sind alles andere als einheitlich. Manche Patienten haben vier Sequenzen, andere weniger; Geräte verschiedener Hersteller liefern leicht unterschiedliche Bilder. MAGPIE behandelt jede MRT‑Sequenz als eigenes "Token" und lernt im laufenden Betrieb, wie viel Gewicht jeder Token erhalten soll, anstatt eine feste Eingabekombination in fester Reihenfolge zu erwarten. Dieser kanalagnostische Ansatz erlaubt dem System, sich anzupassen, wenn etwa eine kontrastverstärkte Sequenz fehlt, aber FLAIR vorhanden ist. Das Modell nutzt außerdem fortgeschrittene Aufmerksamkeitsmechanismen, die ihm erlauben, sowohl "weit zu sehen" — also die langreichweitige Ausbreitung entlang weißer Substanzbahnen zu erfassen — als auch "präzise zu sehen", um sehr kleine Läsionen von nur wenigen Millimetern zu erkennen.
Mehr erreichen mit deutlich weniger Labels
Nach dem Pretraining feinjustierten die Forschenden MAGPIE an nur 20 vollständig annotierten Gliomfällen und verglichen es mit Standardmodellen, die unter denselben Bedingungen von Grund auf neu trainiert wurden. Auf einem wichtigen Hirntumor‑Benchmark (BraTS21) erreichte MAGPIE eine Dice‑Score — ein übliches Überlappungsmaß in der medizinischen Bildgebung — von etwa 61 %, schlug damit die beste von Grund auf trainierte Version um rund 2,6 Prozentpunkte und übertraf eine frühere starke selbstüberwachte Methode, ohne schädliche "negative Transfer"‑Effekte zu zeigen. Auf herausfordernden Out‑of‑Distribution‑Daten — Scans von anderen Erkrankungen, Gerätetypen und Bildeinstellungen — hielt es ebenfalls besser durch und erreichte auf einem Datensatz mit weißer Substanz‑Läsionen über 70 % Dice ohne zusätzliche Feinabstimmung. Entscheidend ist, dass dieses Leistungsniveau üblicherweise etwa 400 annotierte Fälle erfordert; MAGPIE erreicht es mit nur etwa 5 % dieses Aufwands.
Was das für Patientinnen, Patienten und Kliniken bedeuten könnte
Für Nicht‑Expertinnen und Nicht‑Experten ist die zentrale Botschaft: MAGPIE verwandelt einen Berg unlabeled MRT‑Scans in eine potente Assistenz, die sehr wenig Expertenannotation braucht, um klinisch nützlich zu werden. Es kann komplexe Hirntumoren mit realistischen Grenzen umreißen, kleine Satellitenherde erkennen, die andere Systeme übersehen, und zuverlässig weiterarbeiten, wenn Scans von ungewohnten Geräten stammen oder bestimmte Sequenzen fehlen. Diese Kombination könnte die Annotierungszeit von Radiologinnen und Radiologen um rund 95 % reduzieren, die Hürde für kleinere Krankenhäuser senken, fortschrittliche Bild‑KI einzusetzen, und präzisere Operations‑ und Strahlentherapieplanung unterstützen. Zwar sind weitere Validierungen bei seltenen Tumorarten und niedriggradigen Fällen noch nötig, doch zeigt die Studie, wie sorgfältig gestaltetes selbstüberwachtes Lernen robuste, daten‑effiziente Hirntumorsegmentierung näher an den klinischen Alltag bringen kann.
Zitation: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Schlüsselwörter: Gliom-Segmentierung, Hirn-MRT, selbstüberwachtes Lernen, Mischung von Experten, KI in der medizinischen Bildgebung