Clear Sky Science · de
Klinisch geleitete Modelle oder Foundation-Modelle? Vorhersage der zervikalen spondylotischen Myelopathie aus elektronischen Gesundheitsakten
Warum es wichtig ist, dieses Rückenmarksproblem früher zu erkennen
Zervikale spondylotische Myelopathie (ZSM) ist ein sperriger Begriff, bedroht aber bei vielen älteren Menschen still das Rückenmark. Sie kann als Ungeschicklichkeit, schlurfender Gang oder Probleme im Bad beginnen und allmählich zu schwerer Behinderung oder sogar zur Lähmung fortschreiten. Ärztinnen und Ärzte übersehen sie oft jahrelang, weil die Zeichen subtil sind und häufigeren Problemen wie Arthrose oder Karpaltunnelsyndrom ähneln. Diese Studie stellt eine drängende Frage: Können in elektronischen Gesundheitsakten verborgene Muster Menschen Jahre vor einer formellen Diagnose als gefährdet für ZSM ausweisen, und welche Art von künstlicher Intelligenz (KI) eignet sich dafür am besten?
Eine verborgene Erkrankung in einer alternden Bevölkerung
ZSM entsteht, wenn altersbedingter Verschleiß den Wirbelkanal im Hals verengt und das Rückenmark komprimiert. Die Erkrankung ist bei älteren Menschen verbreitet: Bildgebung des Halses zeigt bei etwa einem Drittel der über 60-Jährigen eine Rückenmarkskompression, und ein erheblicher Teil von ihnen entwickelt später Symptome. Studien legen nahe, dass Patienten oft zwei bis sechs Jahre zwischen den ersten Anzeichen und einer korrekten Diagnose warten und so wertvolle Zeit verlieren, in der eine Operation oder andere Maßnahmen dauerhafte Schäden verhindern könnten. Mit einer alternden Bevölkerung und Hausärzten, die mit überfüllten Praxen und begrenzter Erfahrung mit Wirbelsäulenleiden zu kämpfen haben, wächst der Bedarf an skalierbaren Wegen, ZSM früh zu erkennen.
Medizinische Akten in ein Frühwarnsystem verwandeln
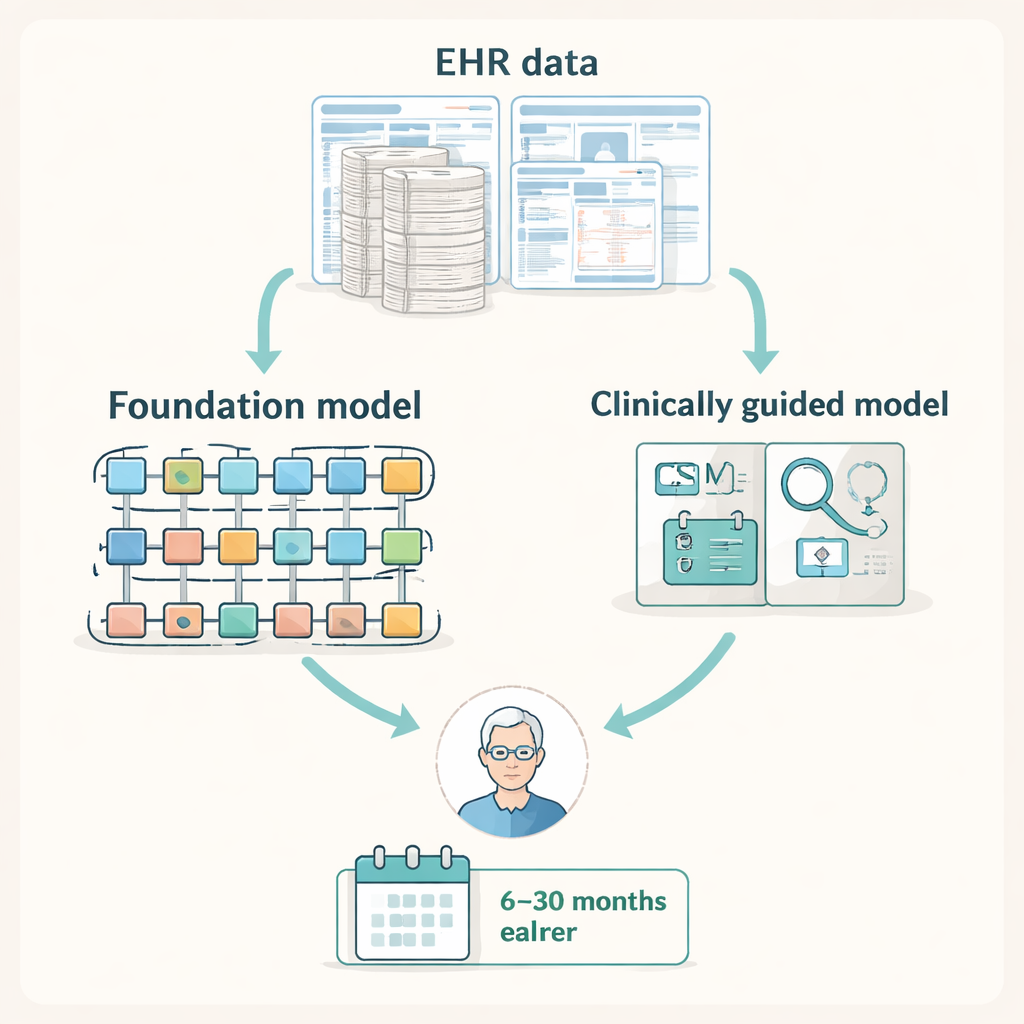
Moderne elektronische Gesundheitsakten (EHRs) erfassen eine detaillierte Spur von Diagnosen, Labortests, Eingriffen und Klinikbesuchen. Die Forscher gingen davon aus, dass diese Spur Hinweise auf frühe ZSM enthalten könnte — etwa wiederholte Stürze, Nerventests oder Physiotherapie — lange bevor jemand spezialisierte Wirbelsäulenbildgebung anordnet. Sie stellten Daten von etwa 2 Millionen Patienten aus zwei großen US-Datensätzen zusammen: einer nationalen Versicherungsanspruchsdatenbank und den Aufzeichnungen eines regionalen Gesundheitssystems. Darin identifizierten sie Zehntausende von Menschen, bei denen später eine ZSM-Diagnose gestellt wurde, und verglichen sie mit ähnlichen Patienten ohne Diagnose, um ein groß angelegtes Testfeld zu schaffen, in dem geprüft wurde, ob KI vorhersagen kann, wer zu Zeitpunkten zwischen 6 und 30 Monaten später eine ZSM-Diagnose erhalten würde.
Große Allzweck-KI versus schlanke, klinisch geleitete Werkzeuge
Das Team verglich mehrere Arten von maschinellen Lernmodellen, die EHR-Daten verarbeiten. Auf der einen Seite standen große „Foundation-Modelle“ — leistungsfähige, auf Transformern basierende Systeme, die ursprünglich auf Millionen von Patientendatensätzen trainiert wurden, um allgemeine Muster in Gesundheitsdaten zu erlernen. Auf der anderen Seite standen kleinere Modelle, die nur aus einer kompakten Liste von 497 Diagnosen-, Prozedur- und Medikationscodes bestanden, die Wirbelsäulenspezialisten als besonders relevant für ZSM ausgewählt hatten. Die Forscher bewerteten die Leistung mit Kennzahlen, die für seltene Erkrankungen geeignet sind, und fragten, wie viel besser jedes Modell als reines Raten darin war, Patienten zu identifizieren, die später eine ZSM entwickeln würden, über verschiedene Vorhersagezeiträume hinweg.
Genauigkeit zu Hause, Zuverlässigkeit unterwegs
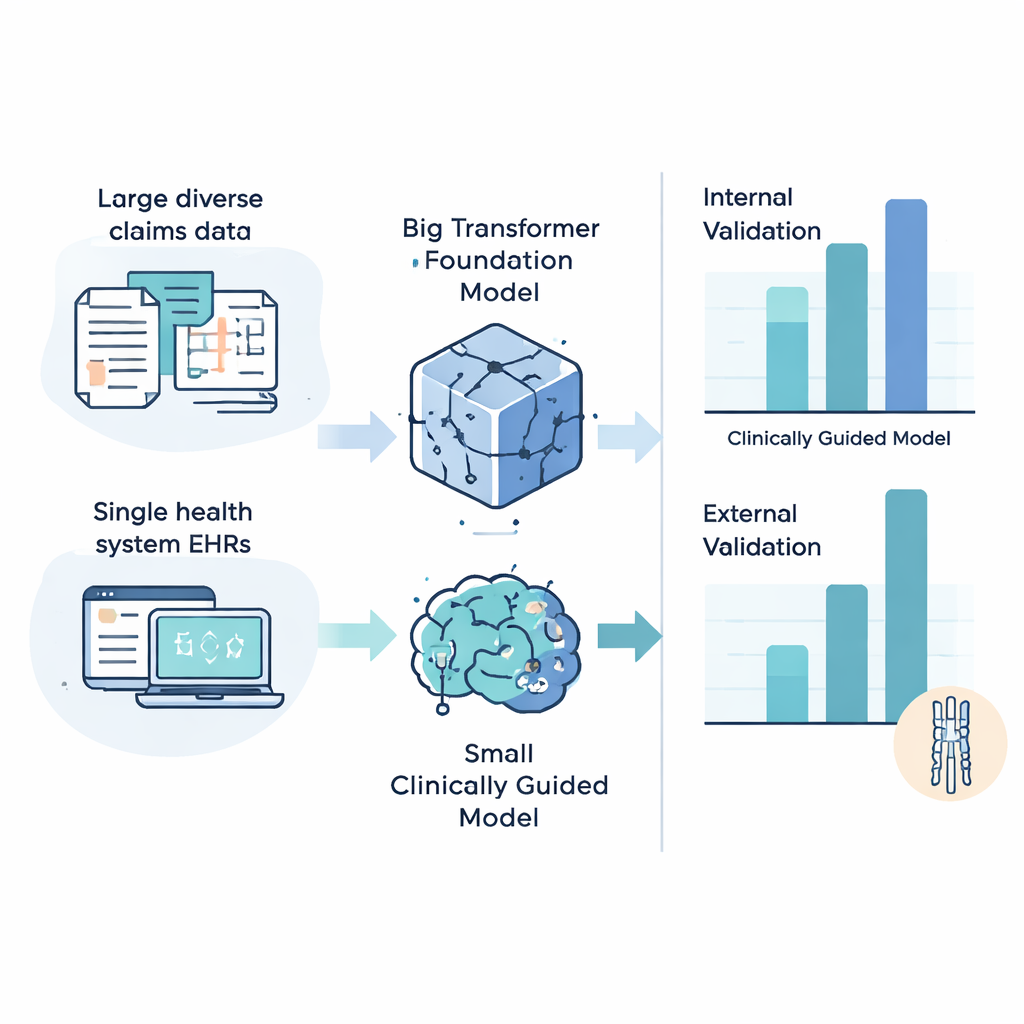
Wurden Modelle innerhalb desselben großen, heterogenen Versicherungsdatensatzes trainiert und getestet, schnitt das größte Foundation-Modell meist am besten ab und erzielte bis zu etwa das sechs- bis siebenfache der Genauigkeit eines nicht-informativen Klassifikators. Das Bild änderte sich jedoch, als die Modelle am unabhängigen Gesundheitssystem evaluiert wurden. Dort übertrafen die einfacheren, klinisch geleiteten Modelle in der Regel die komplexen Transformer und erreichten in einigen Fällen bis zu 13-fach bessere Leistung als reiner Zufall bei der Vorhersage, welche Patienten bald eine ZSM-Diagnose erhalten würden. Ein umgekehrtes Experiment — Training im einzelnen Gesundheitssystem und Test im nationalen Datensatz — erzählte eine ähnliche Geschichte: Kleinere, klinisch fokussierte Modelle ließen sich tendenziell besser zwischen Institutionen übertragen. Subgruppenanalysen zeigten außerdem, dass alle Modelle für Patienten mit häufigeren Arztbesuchen am besten funktionierten, was Fragen zur Fairness gegenüber Menschen aufwirft, die seltener medizinische Versorgung in Anspruch nehmen.
Was das für Patienten und Ärztinnen bedeutet
Die Ergebnisse deuten darauf hin, dass KI helfen könnte, Menschen mit hohem ZSM-Risiko bis zu zweieinhalb Jahre vor der Diagnose zu identifizieren und so Ärztinnen und Ärzte früher zu neurologischen Untersuchungen und Wirbelsäulenbildgebung zu lenken. Die Studie macht jedoch auch einen Kompromiss deutlich: Während große, ausgefeilte KI-Modelle in den Daten, auf denen sie trainiert wurden, glänzen können, sind kleinere, sorgfältig entworfene Modelle auf klinischem Fachwissen basierend möglicherweise verlässlicher, wenn sie in neue Krankenhäuser und Patientengruppen übertragen werden. Für Patienten lautet die Quintessenz hoffnungsvoll, aber nuanciert: Die intelligente Nutzung routinemäßiger Gesundheitsdaten könnte die lange diagnostische Odyssee vieler Betroffener verkürzen, doch der Erfolg hängt nicht nur von leistungsfähigen Algorithmen ab, sondern auch von durchdachtem Modelldesign, sorgfältigen Tests in vielfältigen Umgebungen und Aufmerksamkeit für Gerechtigkeit, damit die Vorteile früher Erkennung breit geteilt werden.
Zitation: Yakdan, S., Warner, B., Ghogawala, Z. et al. Clinically-guided models or foundation models? predicting cervical spondylotic myelopathy from electronic health records. npj Digit. Med. 9, 153 (2026). https://doi.org/10.1038/s41746-026-02337-7
Schlüsselwörter: zervikale spondylotische Myelopathie, elektronische Gesundheitsakten, maschinelles Lernen, Foundation-Modelle, frühe Diagnose