Clear Sky Science · de
Die Wirkung von Midostaurin bei AML wird von einem progenitorähnlichen Zellzustand geprägt, der selektiv durch SMAC‑Mimetika angegriffen wird
Warum einige Leukämie‑Medikamente nicht mehr wirken
Für viele Menschen mit einer Form von Blutkrebs, der akuten myeloischen Leukämie (AML), brachten neue zielgerichtete Therapien Hoffnung — doch nicht alle profitieren, und die Wirksamkeit lässt oft nach. Diese Studie stellt eine einfache, aber entscheidende Frage: Warum ignorieren manche Leukämiezellen das weit verbreitete Medikament Midostaurin, und lässt sich eine intelligente Kombination finden, die diese hartnäckigen Zellen zum Absterben zwingt?
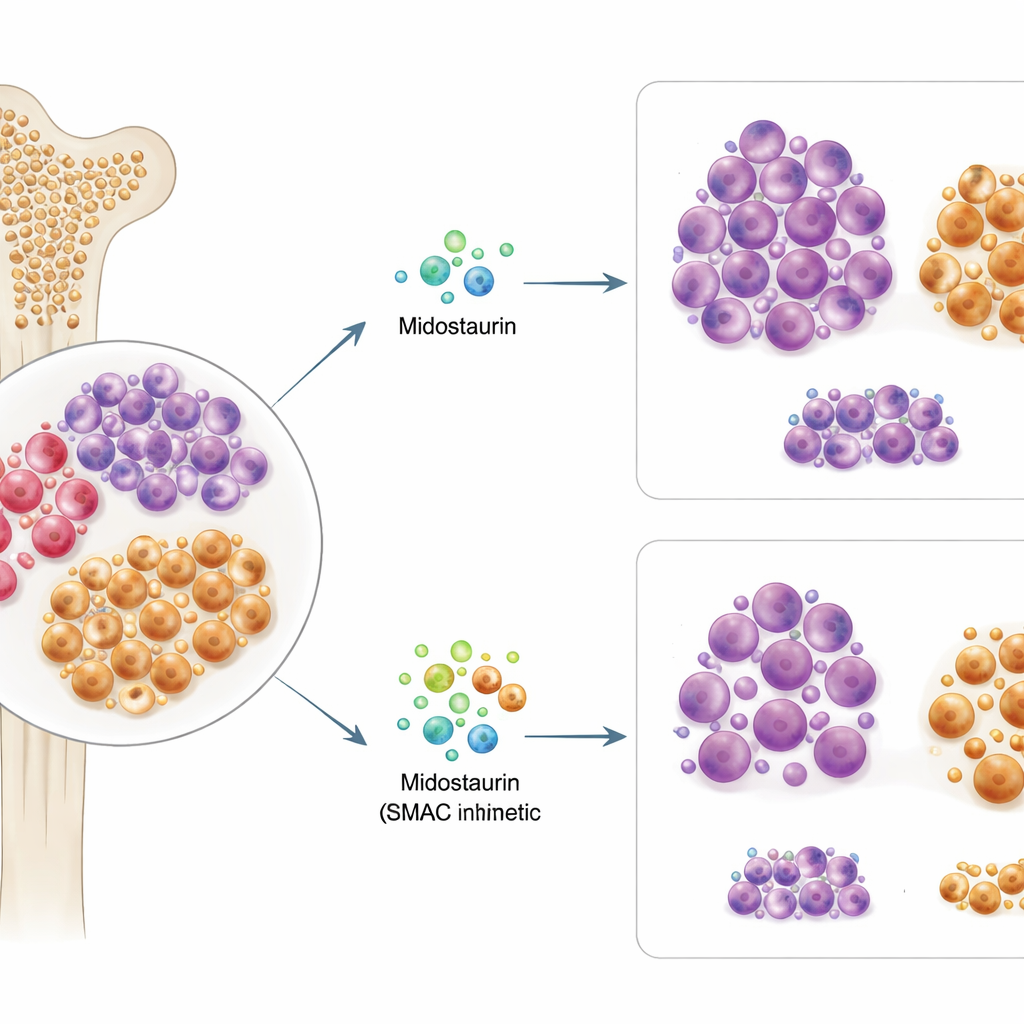
Über die Hauptmutation hinausblicken
Etwa einer von drei AML‑Patienten trägt eine Veränderung im Gen FLT3, die das Leukämiewachstum antreibt und der Grund dafür ist, dass Midostaurin verschrieben wird. Die Forschenden testeten Knochenmark‑ und Blutproben von 63 Patientinnen und Patienten mit FLT3‑mutierter AML und setzten die Zellen im Labor Midostaurin sowie mehr als 500 weiteren Krebswirkstoffen aus. Sie fanden heraus, dass die Empfindlichkeit der Zellen eines Patienten gegenüber Midostaurin ex vivo eng mit der späteren klinischen Reaktion dieses Patienten übereinstimmte. Überraschenderweise sagte weder der genaue Typ der FLT3‑Mutation noch ihre Häufigkeit zuverlässig den Erfolg von Midostaurin voraus, was darauf hindeutet, dass Genetik allein nicht erklärt, wer profitiert.
Ein verstecktes Reservoir hartnäckiger „Samen“zellen
Bei tiefergehenden Analysen verglich das Team die Gesamtmuster von Proteinen und Genaktivität zwischen Midostaurin‑empfindlichen und -resistenten Zellen. Nicht‑ansprechende Proben zeigten vermehrt Merkmale unreifer, stammszellähnlicher Progenitorzellen — Zellen, die näher an der Wurzel der Blutbildung stehen und als „Samen“ fungieren können, die die Leukämie wieder neu entfachen. Im Gegensatz dazu ähnelten ansprechende Proben eher teilweise ausgereiften immunologischen und myeloiden Zellen. Mithilfe fortgeschrittener Einzelzellmethoden identifizierten die Forschenden eine spezifische Population leukämischer Zellen, markiert durch die Oberflächenproteine CD38 und CD45RA, die sich wie diese progenitorähnlichen Samen verhielten. Diese Zellen zeigten eine ungewöhnliche Organisation ihrer äußeren Membran, was darauf hindeutet, dass wichtige Signalproteine so angeordnet sind, dass sie das Überleben begünstigen.
Überlebensverkabelung: ein Schalter in Signalwegen
Midostaurin ist darauf ausgelegt, die FLT3‑Signalgebung zu blockieren, die normalerweise eine Signalkette einschließt, zu der auch das Molekül STAT5 gehört und die Zellwachstum antreiben kann. Als das Team die Signalaktivität in Zelllinien und Patientenproben nach Midostaurin‑Behandlung untersuchte, beobachteten sie zwei unterschiedliche Muster. In Midostaurin‑empfindlichen Zellen fiel die STAT5‑Aktivität schnell ab, konsistent mit einer effektiven FLT3‑Hemmung. In resistenten Zellen dominierte jedoch ein anderer Weg: PI3K/AKT, eine klassische Überlebensroute, die Zellen hilft, dem Zelltod zu widerstehen. Diese resistenten Zellen behielten nach der Behandlung eine erhaltene oder sogar gesteigerte AKT‑Aktivität und wiesen höhere Spiegel antiapoptotischer Proteine auf. Anders gesagt schien die Verkabelung innerhalb dieser progenitorähnlichen Zellen so umlenkt zu sein, dass sie Überleben begünstigt, selbst wenn FLT3 blockiert ist.
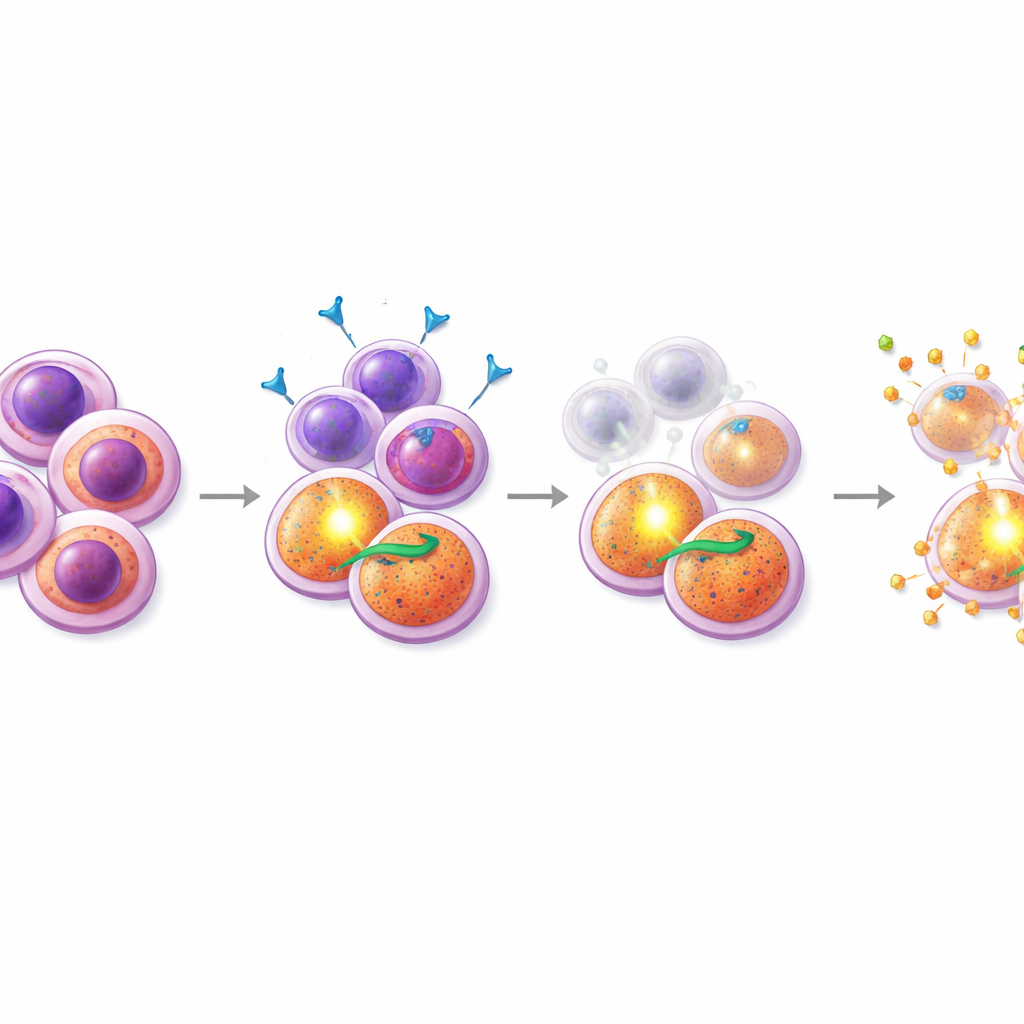
Ein Partnerwirkstoff, der die Schwachstelle trifft
Mit diesem Wissen durchsuchten die Forschenden Kombinationen aus Midostaurin und Hunderten anderer Verbindungen, wobei der Fokus auf Wirkstoffen lag, die den Zelltod beeinflussen. Eine herausragende Gruppe waren SMAC‑Mimetika — Wirkstoffe, die die „Inhibitoren der Apoptose“ (IAPs) außer Kraft setzen, auf die PI3K/AKT‑getriebene Zellen angewiesen sind. In resistenten Patientenproben und in einer resistenten FLT3‑mutierten Zelllinie erzeugte die Zugabe von SMAC‑Mimetika wie Birinapant zusammen mit Midostaurin starke Synergie: Gemeinsam töteten die Wirkstoffe deutlich mehr Zellen als jeweils allein. Wichtig: Detaillierte Durchflusszytometrie‑Experimente zeigten, dass die Midostaurin–SMAC‑Mimetikum‑Kombination selektiv die CD38+CD45RA+ progenitorähnliche Population dezimierte und deren charakteristische Oberflächenmarker reduzierte. Das legt nahe, dass diese Therapie gezielt die schwer zu vernichtenden Samen angreift. Im Gegensatz dazu wirkten Kombinationen mit dem zugelassenen BCL‑2‑Inhibitor Venetoclax stärker gegen eine andere, CD34‑reiche Untergruppe und zeigten nicht denselben fokussierten Effekt auf die resistenten Zellen.
Was das für Patientinnen und Patienten bedeutet
Die Arbeit legt nahe, dass die Resistenz gegen Midostaurin nicht nur von der FLT3‑Mutation selbst abhängt, sondern vom „Zustand“ der Leukämiezellen — ihrem Reifegrad, der Membranorganisation und den bevorzugten Überlebenswegen. Eine progenitorähnliche CD38+CD45RA+ Untergruppe scheint ein wichtiges Reservoir der Resistenz zu sein und verlagert ihre Signalgebung vom üblichen STAT5‑Weg hin zu einem überlebensfreundlichen PI3K/AKT‑Programm. Durch die Kombination von Midostaurin mit SMAC‑Mimetika konnten die Forschenden diese Zellen im Labor wieder empfindlich machen und zum Zelltod treiben. Obwohl größere klinische Studien noch nötig sind, deuten die Befunde auf eine Zukunft hin, in der Ärztinnen und Ärzte funktionelle Tests und Zell‑Zustandsprofilierung — nicht nur DNA‑Sequenzierung — nutzen könnten, um FLT3‑gerichtete Kombinationen auszuwählen, die sowohl die Masse der Leukämie als auch ihre widerstandsfähigsten Samen ausschalten.
Zitation: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Schlüsselwörter: akute myeloische Leukämie, FLT3‑Inhibitoren, Medikamentenresistenz, leukämische Stammzellen, SMAC‑Mimetika