Clear Sky Science · de
COL3A1-hohe krebsassoziierte Fibroblasten orchestrieren metabolische und immunologische Mikroumgebungen und verleihen Brustkrebs Chemoresistenz
Warum einige Brusttumoren Chemotherapie trotzen
Chemotherapie kann beim Brustkrebs Leben retten, doch bei vielen Patientinnen reagieren die Tumoren irgendwann nicht mehr oder sprechen von vornherein kaum an. Diese Studie blickt über die Krebszellen hinaus in ihre Nachbarschaft und fragt: Welche umliegenden Zellen helfen Tumoren, eine Behandlung zu überstehen, und wie tun sie das? Die Antwort konzentriert sich auf eine spezielle Gruppe von Stützzellen, die sowohl die Nährstoffversorgung des Tumors als auch die lokale Immunlage umprogrammiert, um Krebszellen vor Chemotherapie zu schützen.
Die verborgenen Helfer rund um den Tumor
Brusttumoren bestehen nicht nur aus Krebszellen; sie sind gemischte Gemeinschaften mit Blutgefäßen, Immunzellen und Bindegewebszellen, den Fibroblasten. Leben Fibroblasten im Tumor, nennt man sie krebsassoziierte Fibroblasten (CAFs), und sie können Krebs hemmen oder fördern. Durch die Kombination mehrerer leistungsfähiger genetischer Profilierungsverfahren an Patientenproben — Einzelzell-, räumliche- und Bulk-Analysen — zusammen mit Labor- und Tierversuchen, identifizierten die Forschenden eine CAF-Untergruppe, die hohe Mengen eines Moleküls namens COL3A1 produziert, einem Bestandteil des Gewebegerüsts. Patientinnen, deren Tumoren mehr dieser COL3A1‑reichen CAFs enthielten, zeigten häufiger schlechte Chemotherapieansprechen und ein schlechteres Überleben.
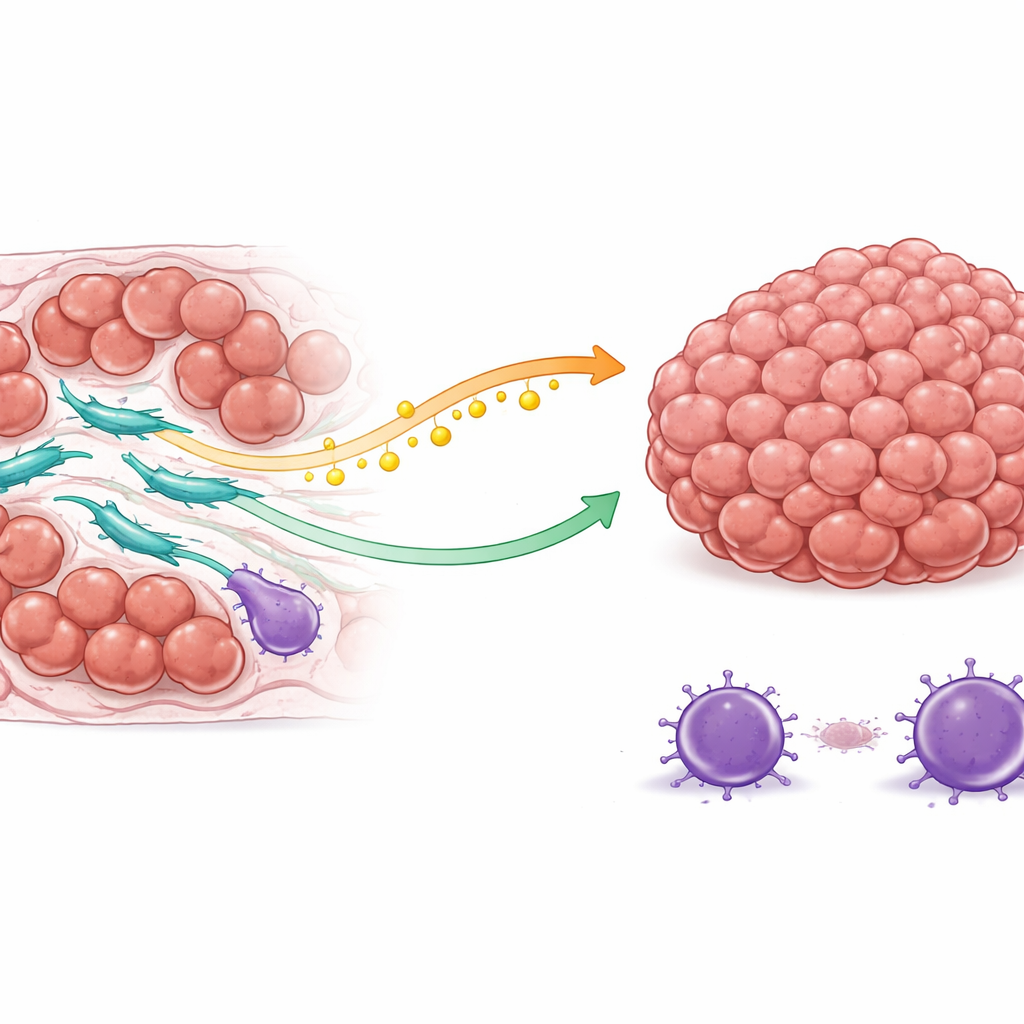
Ein zweigleisiger Schutz: Treibstoff und Abschirmung
Das Team fand heraus, dass COL3A1‑reiche CAFs Krebszellen auf zwei Hauptarten schützen. Erstens verändern sie ihren Umgang mit Fetten. Diese Fibroblasten steigern die Aktivität eines Enzyms, das Ölsäure herstellt, eine Fettsäure. Statt diesen Treibstoff zu behalten, geben sie ihn in die Tumornachbarschaft ab. Krebszellen nehmen die Ölsäure über ein Oberflächenprotein auf und schalten daraufhin einen inneren Überlebensweg an, der dafür bekannt ist, Zellen gegen Todesreize zu helfen. Folglich sind diese Krebszellen, wenn die Chemotherapie zelluläre Selbstzerstörungsprogramme auslösen will, besser gerüstet, dem zu widerstehen und weiter zu proliferieren.
Gestaltung einer unfreundlichen Immunumgebung
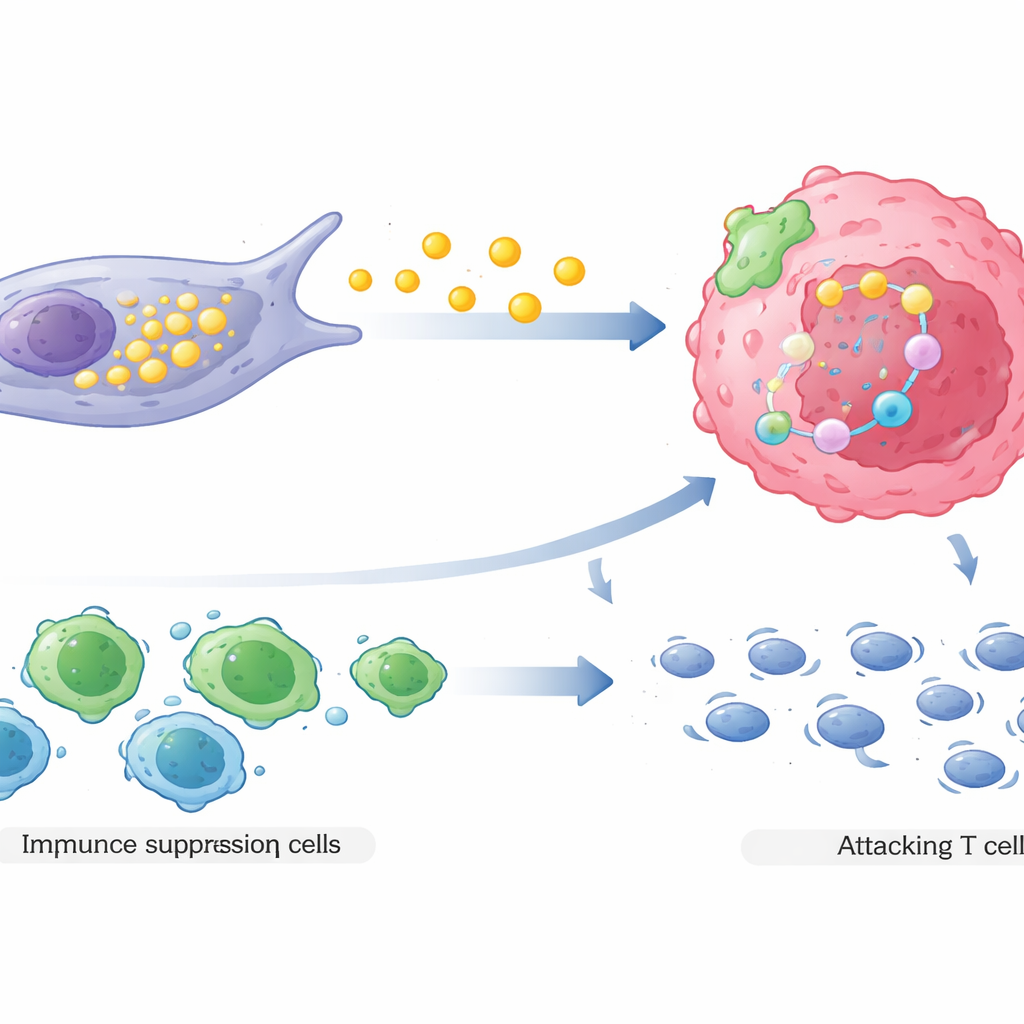
Zweitens formen COL3A1‑reiche CAFs die lokale Immunlandschaft zugunsten des Tumors um. Durch komplexe Signalwechselwirkungen ziehen sie regulatorische T‑Zellen an — eine Immunzellenart, die Immunreaktionen dämpft — und schwächen gleichzeitig oder verdrängen Killer‑T‑Zellen, die normalerweise Krebs angreifen würden. Räumliche Kartierungen realer Patientenproben zeigten, dass diese Fibroblasten dazu neigen, nahe sowohl an medikamentenresistenten Krebszellen als auch an immunsuppressiven Zellen zu sitzen, während wirksame Killer‑T‑Zellen weiter entfernt sind. Diese Anordnung schafft eine geschützte Zone, in der Krebszellen weniger immunen Bedrohungen ausgesetzt sind, gerade während sie auch schwerer durch Medikamente zu töten werden.
Belege aus Zellen, Mäusen und Patienten
Um Kausalität zu prüfen, reduzierten die Forschenden COL3A1 in im Labor gezüchteten CAFs. Wurden Brustkrebszellen neben diesen veränderten Fibroblasten kultiviert, bildeten sie weniger invasive Strukturen, wurden vom Chemotherapeutikum Paclitaxel leichter abgetötet und zeigten stärkeres Anzeichen programmierter Zellsterblichkeit. In Mäusen, die mit Mischungen aus Brustkrebszellen und CAFs transplantiert wurden, verlangsamte das Blockieren von COL3A1 in den Fibroblasten das Tumorwachstum unter Chemotherapie und senkte die Spiegel des fettbildenden Enzyms sowie des an Ölsäure gebundenen Rezeptors der Krebszellen. In einer Kohorte von 72 Patientinnen, die vor einer Operation eine Chemotherapie erhielten, korrespondierten höhere COL3A1‑Level und die zugehörigen Fettstoffwechselpartner stark mit schlechteren Therapieansprechen und kürzerem Wiederauftreten des Krebses.
Was das für zukünftige Behandlungen bedeutet
Kurz gesagt zeigt die Studie, dass eine bestimmte Gruppe von Stützzellen in Brusttumoren wie eine Bodyguard‑Einheit agiert: Sie versorgen Krebszellen mit einer schützenden, fettbasierten Nahrung und rekrutieren Immunverbündete, die die Abwehr des Körpers dämpfen. Zusammen machen diese Mechanismen die Chemotherapie weniger wirksam. Die Messung der Häufigkeit von COL3A1‑reichen Fibroblasten verbessert die Vorhersage, wer auf eine Behandlung ansprechen wird und wer nicht, und die von ihnen genutzten Wege — Fettproduktion, Überlebenssignale in Krebszellen und Immununterdrückung — bieten neue Angriffspunkte für Medikamente. Zukünftig könnten Therapien, die diese Fibroblasten entwaffnen oder umprogrammieren, mit Standardchemotherapie kombiniert werden, um das Entstehen von Resistenzen zu verhindern.
Zitation: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Schlüsselwörter: Brustkrebs, Chemoresistenz, Tumormikroumgebung, krebsassoziierte Fibroblasten, Lipidstoffwechsel