Clear Sky Science · de
Integration von Liquid Biopsy und mutationalen Signaturen zur Förderung der Präzisionsonkologie
Warum ein Bluttest für die „Fingerabdrücke“ des Krebses wichtig ist
Krebs wird oft als Erkrankung der DNA beschrieben, doch jeder Tumor ist genetisch unterschiedlich und kann sich im Laufe der Zeit verändern. Das erschwert es Ärzten, die richtige Behandlung auszuwählen und nachzuverfolgen, ob ein Krebs zurückkehrt oder resistent gegen Therapien wird. Dieser Artikel erklärt einen vielversprechenden Ansatz, der einen einfachen Bluttest — die sogenannte Liquid Biopsy — mit detaillierten Mustern DNA‑Schadens, den mutationalen Signaturen, kombiniert. Zusammengenommen könnten sie es ermöglichen, das Verhalten eines Tumors über den Krankheitsverlauf hinweg zu verfolgen und Therapien präziser denn je anzupassen. 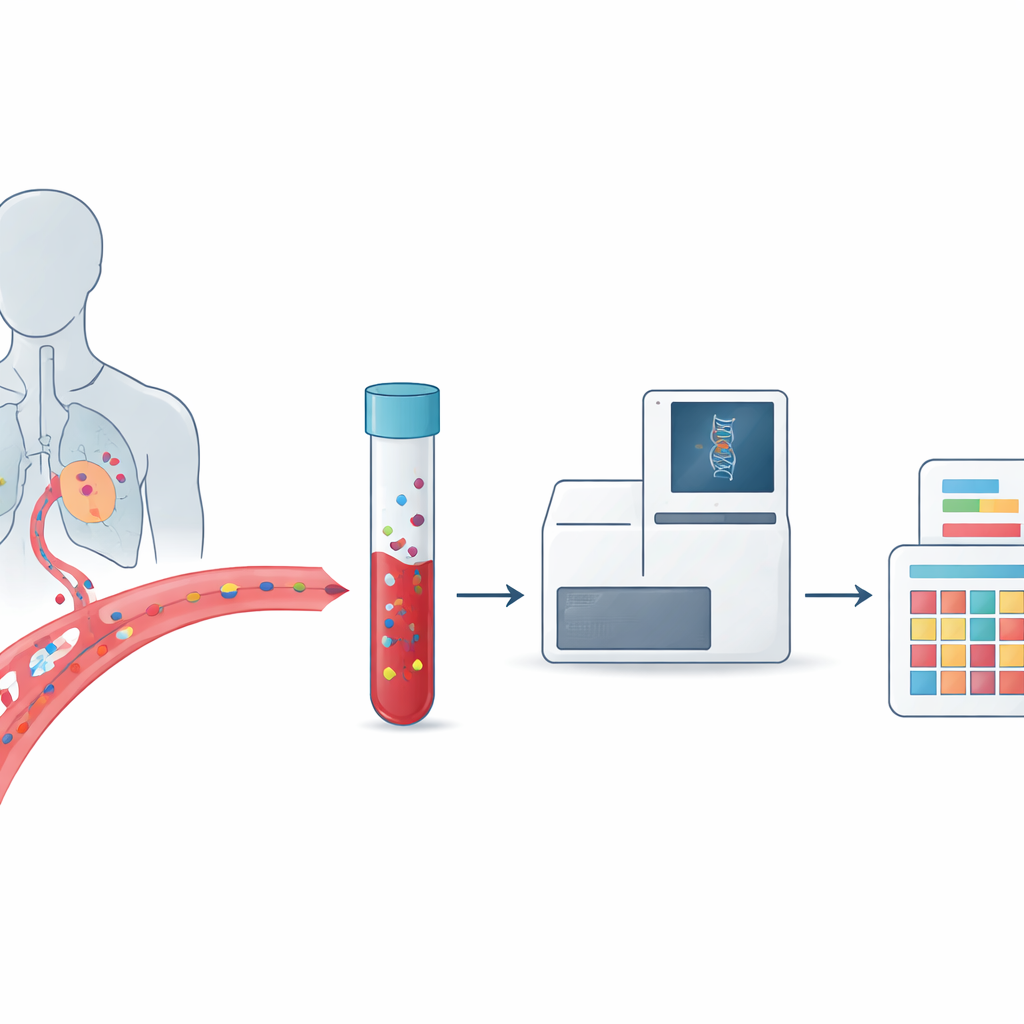
Auf der Suche nach Krebs-Hinweisen in einer Blutprobe
Traditionelle Tumorbiopsien erfordern die Entnahme von Tumorgewebe durch einen chirurgischen Eingriff oder eine Nadel, was schmerzhaft, risikobehaftet und schwer wiederholbar sein kann. Die Liquid Biopsy geht einen anderen Weg: Sie sucht nach Spuren des Tumors, die dieser in Blut und andere Körpersäfte abgibt. Zu diesen Spuren gehören ganze Tumorzellen und kurze DNA‑Fragmente, die freigesetzt werden, wenn Krebszellen absterben. Da Blutproben regelmäßig entnommen werden können und Material von mehreren Tumorherden erfassen, bietet die Liquid Biopsy eher ein bewegtes Bild davon, wie ein Krebs wächst, streut und auf Therapien reagiert, statt nur eine einzelne Momentaufnahme zu liefern.
Von einzelnen Mutationen zu übergreifenden Schadensmustern
Die meisten aktuellen Liquid‑Biopsy‑Tests konzentrieren sich darauf, spezifische Mutationen in einer kurzen Liste von Genen zu erkennen, die den Einsatz zielgerichteter Medikamente steuern. Nicht alle Tumoren tragen jedoch solche „drugbaren“ Veränderungen, und Tumoren mit vielen unterschiedlichen Mutationen entgehen leicht starren Genpanelen. In den letzten zehn Jahren haben leistungsfähige DNA‑Sequenzierungsverfahren gezeigt, dass die Mutationen in einem Krebsgenom nicht zufällig sind: Sie formen wiedererkennbare Muster, die durch Faktoren wie Tabakrauch, ultraviolette Strahlung, fehlerhafte DNA‑Reparatur oder sogar Chemotherapien geprägt werden. Diese wiederkehrenden Muster, mutationale Signaturen genannt, fungieren wie Fingerabdrücke der Prozesse, die die DNA im Verlauf der Tumorentstehung geschädigt haben.
Die Geschichte und Schwachstellen des Tumors lesen
Mutationale Signaturen können Hinweise darauf geben, wo ein Krebs entstanden ist und welche internen Reparatursysteme defekt sind. So zeigen Lungenkrebsarten von Rauchern häufig ein Muster, das mit Tabakexposition verbunden ist, während einige Darmkrebse Signaturen einer Mismatch‑Repair‑Störung tragen — ein Defekt, der sie auch besonders empfindlich gegenüber bestimmten Immuntherapien macht. Andere Signaturen deuten auf Probleme in einem DNA‑Reparaturweg namens homologe Rekombination hin, was Tumoren besonders verwundbar gegenüber Platinmedikamenten und PARP‑Inhibitoren machen kann. Experimentelle Studien in Zell‑ und Tiermodellen haben bestätigt, dass viele Umweltchemikalien und Krebstherapien charakteristische mutationale Fußabdrücke hinterlassen, die denen bei Patienten entsprechen, und damit die Verbindung zwischen Signatur und Ursache stärken. 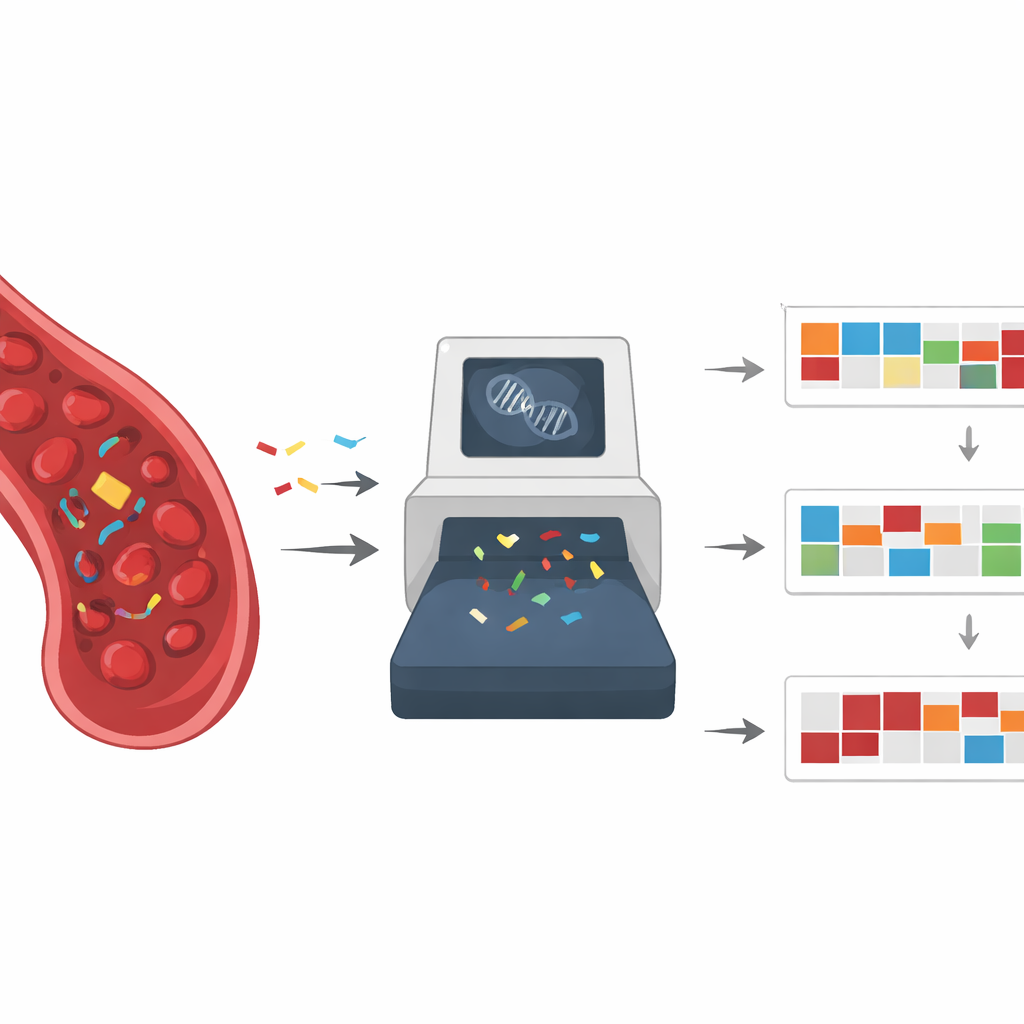
Blutbasiertes Monitoring mit DNA‑Fingerabdrücken kombinieren
Die Kernidee des Artikels ist, Liquid Biopsy und mutationale Signaturen in einem einzigen Rahmen zu verschmelzen. Durch breit angelegte, genomweite Sequenzierung von Tumor‑DNA‑Fragmenten im Blut könnten Ärztinnen und Ärzte gleichzeitig einzelne Mutationen und die übergreifenden Schadensmuster identifizieren, die sie erzeugt haben. Das könnte die Früherkennung von Krebs verbessern, helfen, das Gewebe des Ursprungs in rätselhaften Fällen zu bestimmen, und die Therapieauswahl verfeinern — auch wenn klassische Treibermutationen fehlen. Wiederholte Blutentnahmen über Monate oder Jahre könnten zeigen, wann ein Tumor auf einen neuen mutationalen Prozess umschaltet, etwa durch anhaltende Medikamentenexposition ausgelöst, was auf eine entstehende Resistenz oder das Risiko eines therapiebedingten Zweittumors hinweisen würde.
Hürden auf dem Weg zur routinemäßigen Anwendung
Trotz des Potenzials steht dieser Ansatz vor praktischen Herausforderungen. Manche Tumoren setzen nur sehr wenig DNA ins Blut frei, sodass ihre Signale schwer nachzuweisen sind. Viele bekannte Signaturen haben noch keine klare biologische Erklärung, und einige Muster können teilweise durch technische Eigenheiten unterschiedlicher Sequenzierplattformen geprägt sein. Altersbedingte Veränderungen in blutbildenden Zellen können eigene Mutationen in die zirkulierende DNA einführen und das Bild weiter verwirren. Aktuelle Methoden, um Signaturen aus Plasma zu extrahieren, beruhen häufig auf komplexen Machine‑Learning‑Werkzeugen, die große Trainingsdatensätze benötigen und bislang vornehmlich in retrospektiven Forschungsstudien statt in prospektiven klinischen Studien getestet wurden.
Was dies für die künftige Krebsversorgung bedeuten könnte
Die Autoren kommen zu dem Schluss, dass die Integration von Liquid Biopsy und mutationalen Signaturen die Krebsversorgung langfristig von einer Abfolge einmaliger Entscheidungen zu einem kontinuierlich aktualisierten Prozess transformieren könnte. Anstatt sich allein auf eine zum Zeitpunkt der Diagnose entnommene Gewebeprobe zu stützen, könnten Klinikerinnen und Kliniker eines Tages routinemäßige Bluttests nutzen, um die sich entwickelnde „Handschrift“ der DNA‑Schädigung in einem Tumor zu verfolgen. Das könnte Screening und Diagnose schärfen, die Auswahl und Reihenfolge von Therapien leiten und Resistenz erkennen, noch bevor sie in bildgebenden Verfahren sichtbar wird. Um diese Vision zu verwirklichen, sind standardisierte Methoden, rigorose Validierung und intelligentere Computermodelle erforderlich, doch das Konzept weist auf eine Zukunft, in der Krebsbehandlung nicht nur auf die aktuellen Mutationen des Tumors abzielt, sondern auch von den Kräften informiert wird, die sie hervorgebracht haben.
Zitation: Carrasco, R., Dreij, K. Integrating liquid biopsy and mutational signatures to advance precision oncology. npj Precis. Onc. 10, 114 (2026). https://doi.org/10.1038/s41698-026-01337-w
Schlüsselwörter: Liquid Biopsy, mutationale Signaturen, zellfreie DNA, Präzisionsonkologie, Krebsentwicklung