Clear Sky Science · de
Klinische Validierung eines gewebsunabhängigen, genomweiten Methylom-Anreicherungsassays zur Überwachung der Reaktion auf Pembrolizumab
Krebsbehandlung per einfachem Bluttest beobachten
Menschen mit fortgeschrittenem Krebs und ihre Ärztinnen und Ärzte müssen oft Wochen oder Monate warten, um sicher zu wissen, ob ein Immuntherapeutikum wirklich wirkt. Bildgebende Verfahren können irreführend sein, und wiederholte Gewebebiopsien sind invasiv oder gar nicht durchführbar. Diese Studie untersucht eine neue Art von Bluttest, der winzige chemische Markierungen auf Tumor-DNA im Blut liest und so eine schnellere und weniger invasive Möglichkeit bietet, festzustellen, ob das Medikament Pembrolizumab hilft.
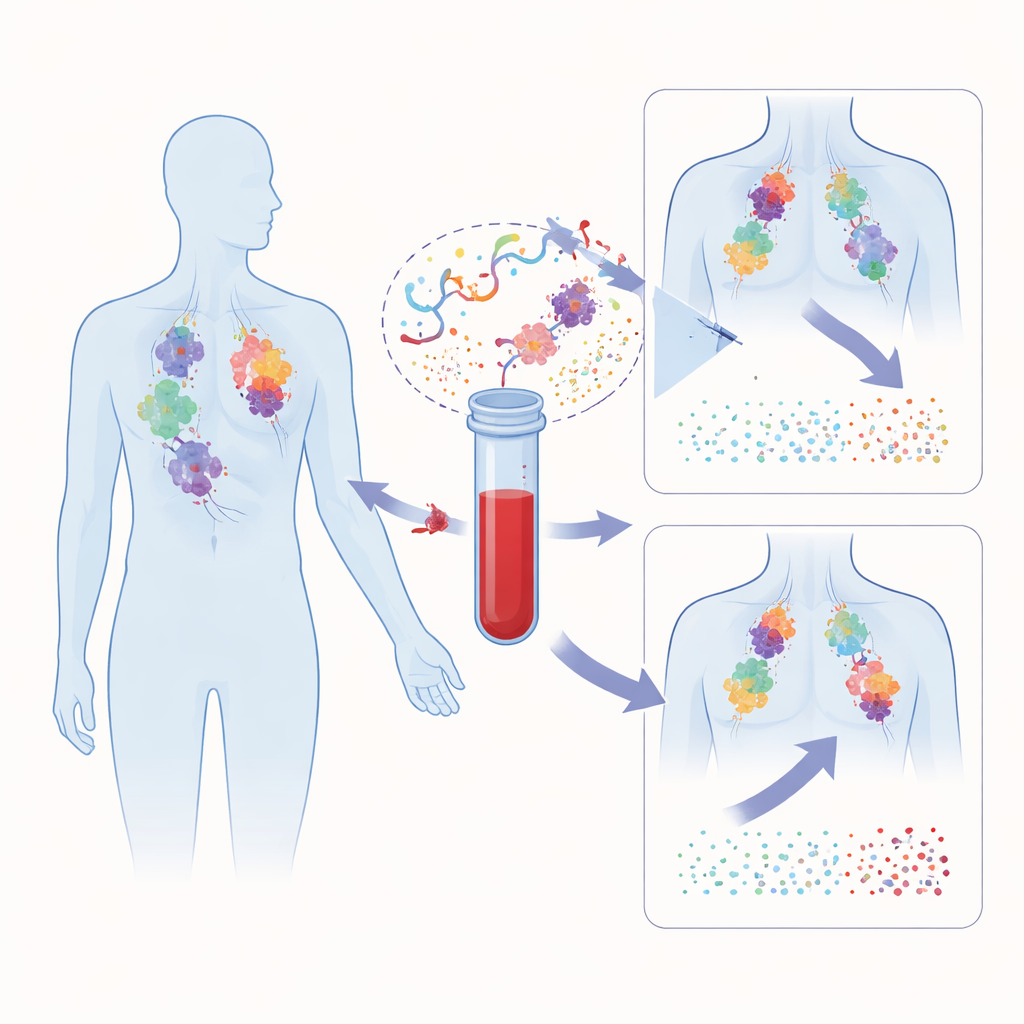
Warum die aktuellen Kontrollen nicht ausreichen
Immuntherapien wie Pembrolizumab können bemerkenswerte und langanhaltende Reaktionen hervorrufen, jedoch nur bei einem Teil der Patientinnen und Patienten. Heute verlassen sich Kliniker auf Tumormerkmale wie PD-L1-Spiegel oder Mutationslast, gemessen an Gewebebiopsien, sowie auf wiederkehrende bildgebende Untersuchungen. Diese Ansätze haben bedeutende Nachteile: Biopsieproben sind nicht immer verfügbar, spiegeln möglicherweise nicht den gesamten Tumor wider und werden meist nur einmal vor Behandlungsbeginn erhoben. Bildgebung kann irreführend sein, weil eindringende Immunzellen den Tumor vorübergehend vergrößern können — ein Phänomen, das als Pseudoprogression bekannt ist. Zusammengenommen können diese Einschränkungen dazu führen, dass Patientinnen und Patienten monatelang unwirksame Therapien fortsetzen, bevor klar wird, dass sie nicht wirken.
Ein universeller Bluttest statt Tumorbiopsien
Die Forschenden testeten einen „gewebsunabhängigen“ Blutassay, der keine vorherige Tumorprobe des Patienten benötigt. Stattdessen konzentriert er sich auf DNA-Methylierung — stabile chemische Markierungen an der DNA, die sich zwischen gesunden und Krebszellen unterscheiden. Tumore geben kontinuierlich DNA-Fragmente ins Blut ab und erzeugen so zirkulierende Tumor-DNA (ctDNA). Mit einer Technik namens cfMeDIP-seq reichert das Team nur methylierte Fragmente aus Plasma an und sequenziert diese, bevor ein auf großen Krebs- und Nicht-Krebs-Datensätzen trainierter Klassifikator angewendet wird. Das Ergebnis ist ein numerischer ctDNA-Score, der widerspiegelt, wie viel tumorabgeleitete DNA im Blut vorhanden ist, unabhängig davon, wo der Krebs im Körper entstanden ist.
Verfolgung der Pembrolizumab-Reaktion über viele Krebsarten hinweg
Um zu prüfen, ob dieser Test die Reaktion auf eine Immuntherapie überwachen kann, analysierten die Wissenschaftlerinnen und Wissenschaftler 241 Blutproben von 69 Personen mit verschiedenen fortgeschrittenen soliden Tumoren, die in die INSPIRE-Studie eingeschlossen waren. Die Teilnehmenden, die zuvor keine Immuntherapie erhalten hatten, wurden allein mit Pembrolizumab behandelt und hatten Blutentnahmen vor Behandlungsbeginn sowie dann alle drei Zyklen, beginnend etwa beim dritten Therapiezyklus. Die zentrale Frage war einfach: Steigt oder fällt der ctDNA-Score vom Behandlungsbeginn bis zum dritten Zyklus? Entsprechend wurden die Patienten gruppiert und hinsichtlich Tumoransprechen, progressionsfreiem Intervall und Gesamtüberleben verfolgt.
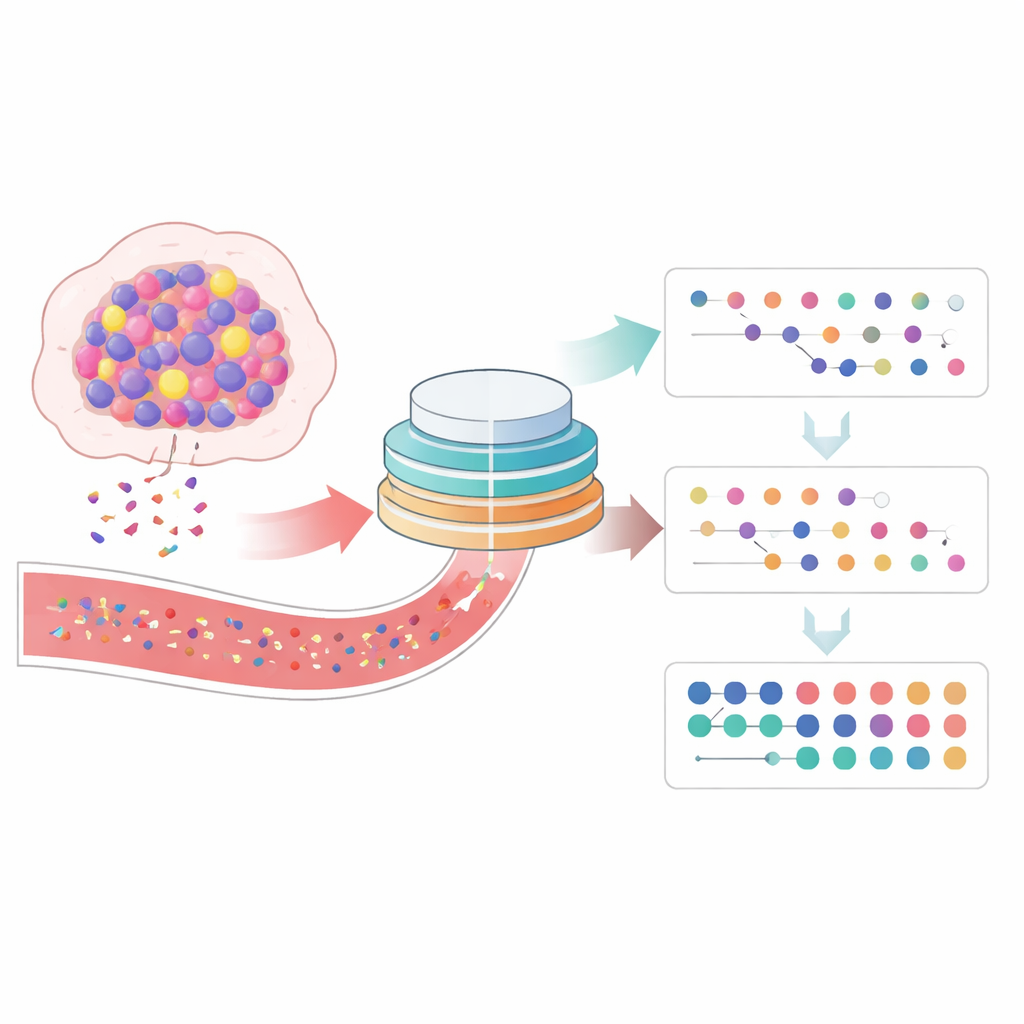
Was Veränderungen in der Tumor‑DNA offenbarten
Die Hälfte der Patienten zeigte bis zum dritten Zyklus einen Rückgang des ctDNA-Scores, die andere Hälfte einen Anstieg. Das frühe Muster war auffällig: Keiner der Patientinnen und Patienten mit steigendem ctDNA zeigte eine relevante Tumorverkleinerung, und fast alle profitierten nicht von der Therapie. Im Gegensatz dazu wiesen nahezu alle klinisch ansprechenden Patientinnen und Patienten einen Abfall der ctDNA auf. Ein sinkender Score war stark mit höheren Chancen auf Tumorschrumpfung, längeren Intervallen bis zur Erkrankungsverschlechterung und in einfacheren Analysen mit längerem Gesamtüberleben verknüpft. Betrachtete das Team nicht nur diesen einzelnen frühen Zeitpunkt, fanden sie, dass Patientinnen und Patienten, deren ctDNA-Werte während der gesamten Behandlung unter dem Ausgangsbaseline blieben, tendenziell länger lebten und längere progressionsfreie Intervalle aufwiesen als diejenigen, deren ctDNA irgendwann über die Ausgangsbasis anstieg.
Wie sich dieser Test im Vergleich zu anderen Signalen schlägt
Das Team verglich die ctDNA-Veränderungen auch mit bekannteren Markern wie PD-L1-Expression und Tumormutationslast, gemessen aus Gewebeproben. Während höhere PD-L1-Werte in einfachen Analysen eine gewisse Beziehung zum Nutzen zeigten, verloren diese Gewebemarker an Bedeutung, sobald die ctDNA-Dynamik in komplexere Modelle einbezogen wurde. Im Gegensatz dazu blieben frühe Veränderungen der ctDNA ein starker, unabhängiger Indikator für das Patientenoutcome, insbesondere für das progressionsfreie Überleben. Wichtig ist, dass diese Leistung mit dem übereinstimmte, was zuvor mit personalisierten, tumorinformierten ctDNA-Tests erreicht worden war, die eine vorherige Sequenzierung des Tumors jedes Patienten erfordern — der neue Assay funktioniert jedoch allein aus Blutproben und kann über viele Krebsarten hinweg angewendet werden.
Was das für Patientinnen und Patienten bedeuten könnte
Praktisch deutet diese Studie darauf hin, dass ein spezialisierter Bluttest innerhalb weniger Behandlungszyklen anzeigen kann, ob Pembrolizumab wahrscheinlich bei einer Patientin oder einem Patienten wirkt. Ein anhaltender Rückgang der Tumor‑DNA im Blut signalisiert eine höhere Chance auf Nutzen, während steigende Werte warnen, dass der Tumor gegen die Therapie resistent sein könnte. Da die Methode nicht von Tumorgewebe abhängt und wiederholt angewendet werden kann, könnte sie Ärzten erlauben, früher und fundierter über das Fortsetzen, Ändern oder Intensivieren einer Behandlung zu entscheiden. Größere prospektive Studien sind erforderlich, doch diese Arbeit liefert starke Hinweise darauf, dass das Lesen von Methylierungsmustern in im Blut zirkulierender Tumor‑DNA zu einem leistungsfähigen, breit einsetzbaren Werkzeug zur Steuerung der Immuntherapie werden könnte.
Zitation: Stutheit-Zhao, E.Y., Zhong, Y., Melton, C.A. et al. Clinical validation of a tissue-agnostic genome-wide methylome enrichment assay to monitor response to pembrolizumab. npj Precis. Onc. 10, 129 (2026). https://doi.org/10.1038/s41698-026-01327-y
Schlüsselwörter: zirkulierende Tumor-DNA, Überwachung der Immuntherapie, Liquid Biopsy, DNA-Methylierung, Pembrolizumab