Clear Sky Science · de
Vorhersage von homologer Rekombinationsdefizienz und Behandlungsergebnissen mittels eines CT-basierten Foundation-Modells: eine präklinische Studie
Warum das für Patientinnen, Patienten und Ärztinnen wichtig ist
Behandlungen, die DNA schädigen — etwa bestimmte Chemotherapien und neue zielgerichtete Wirkstoffe — können bei Tumoren, deren Reparatursysteme bereits gestört sind, außerordentlich wirksam sein. Die Herausforderung besteht darin, welche Tumoren diese verborgenen Schwachstellen besitzen, ohne auf wiederholte, invasive Biopsien angewiesen zu sein. Diese Studie untersucht, ob routinemäßige medizinische Scans von Mäusen, interpretiert durch ein leistungsfähiges künstliches Intelligenzmodell, die Verwundbarkeit eines Tumors und seine Ansprechrate auf ein neues experimentelles Medikament aufdecken können.
Eine verborgene Schwachstelle in Krebszellen
Viele Tumoren weisen Defekte in einem wichtigen DNA-Reparaturweg auf, der als homologe Rekombination bezeichnet wird. Wenn dieser Weg versagt, sammeln sich Schäden im Erbgut an — ein Zustand, der als homologe Rekombinationsdefizienz (HRD) bekannt ist. HRD kann die Entstehung von Krebs begünstigen, stellt aber zugleich eine Achillesferse dar: Wirkstoffe, die zusätzlich DNA schädigen, können diese bereits belasteten Zellen überfordern und sie gezielter abtöten als gesunde Zellen. Heute basiert die Identifikation von HRD meist auf Gentests oder spezialisierten Labortests, die kosten- und zeitaufwändig sind und häufig Tumorproben erfordern. Die Autorinnen und Autoren fragten, ob Bildgebung — dieselben dreidimensionalen Röntgenscans, wie sie in Kliniken weit verbreitet sind — ein schnelles, nicht-invasives Fenster zu HRD bieten könnte.
Intelligente Scans statt weiterer Biopsien
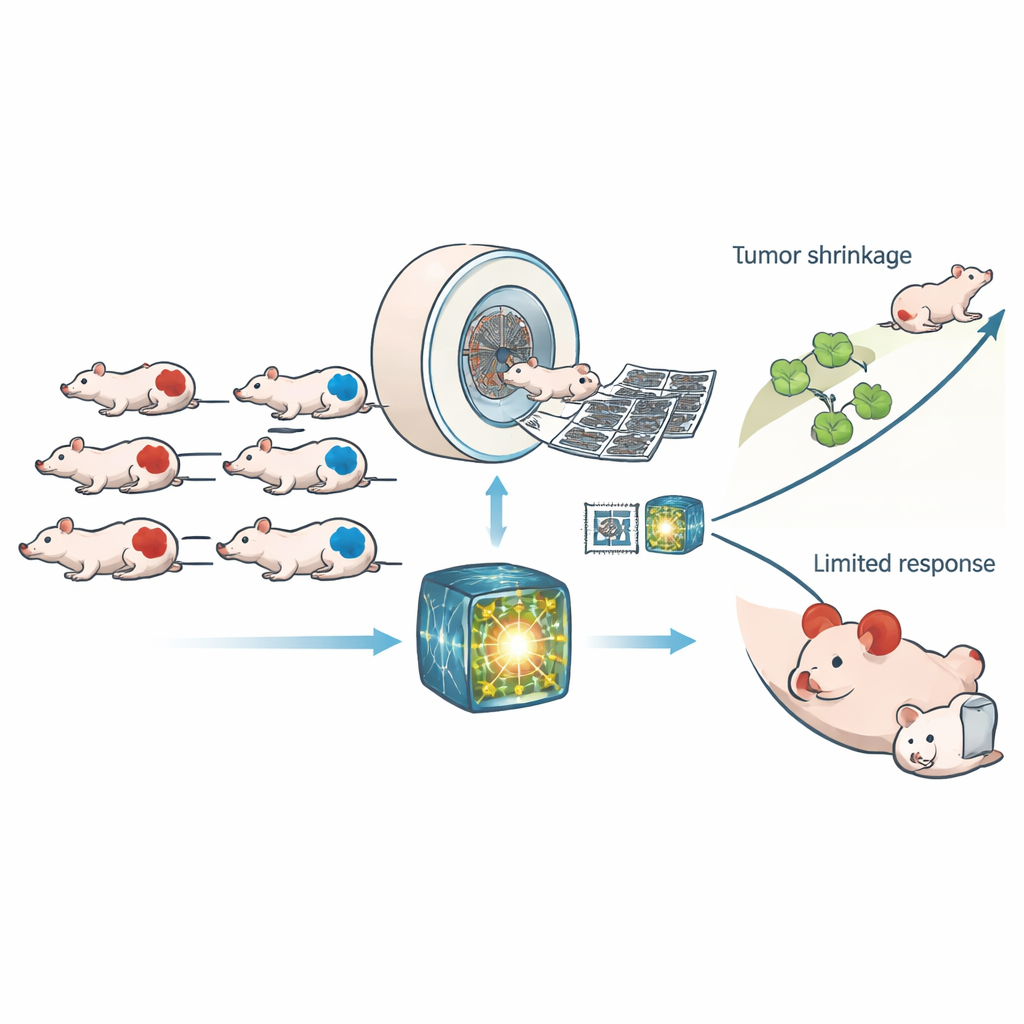
Die Forschenden arbeiteten mit 307 Mäusen, die humane Tumortransplantate trugen, die entweder HRD-positiv oder reparaturmäßig normal waren. Alle Tiere wurden mit hochauflösender Computertomographie (CT) vor und nach der Verabreichung entweder einer Kontrollbehandlung oder CP-506 gescannt — einem experimentellen Wirkstoff, der in sauerstoffarmen Regionen von Tumoren aktiv wird und DNA-Stränge miteinander verknüpft. Anstatt sich auf einige wenige handgefertigte Bildmerkmale zu stützen, nutzte das Team ein modernes „Foundation-Modell“, das an großen menschlichen CT-Datensätzen trainiert worden war, um aus jedem Scan Tausende subtiler Muster zu extrahieren. Auf diesen Mustern wurde dann ein einfacher Klassifikator trainiert, der entscheidet, ob ein Tumor HRD-positiv ist; dieselben gelernten Merkmale wurden außerdem wiederverwendet, um vorherzusagen, wie viel DNA-Schaden und Wachstumspause CP-506 verursachen würde.
Wie gut das Bildgebungsmodell arbeitete
Das Foundation-Modell übertraf deutlich sowohl traditionelle Radiomik-Verfahren als auch ein standardmäßiges Deep-Learning-Netzwerk, das von Grund auf trainiert wurde. Auf neuen Testscans unterschied es HRD- von Nicht-HRD-Tumoren mit einer Fläche unter der Kurve von etwa 0,88 — ein Genauigkeitsniveau, das über verschiedene CT-Energieeinstellungen hinweg stabil blieb. Wenn sich beide KI-Ansätze auf den Tumortyp einigten, stieg die Leistung noch weiter. Der bildbasierte HRD-Score des Modells stimmte in mehreren Prostata- und kolorektalen Tumorlinien eng mit dem tatsächlichen genetischen Status überein, wenngleich eine Linie mit ungewöhnlichem Reparaturverhalten schwerer zu klassifizieren blieb. Wichtig ist, dass die mit HRD verknüpften CT-Merkmale nicht nur statistische Artefakte waren: Sie sagten auch voraus, wie viel anhaltender DNA-Schaden CP-506 48 Stunden nach der Behandlung verursachte und wie lange es in einem parallelen Experiment dauerte, bis Tumoren auf das Vierfache ihrer Größe nachwuchsen.
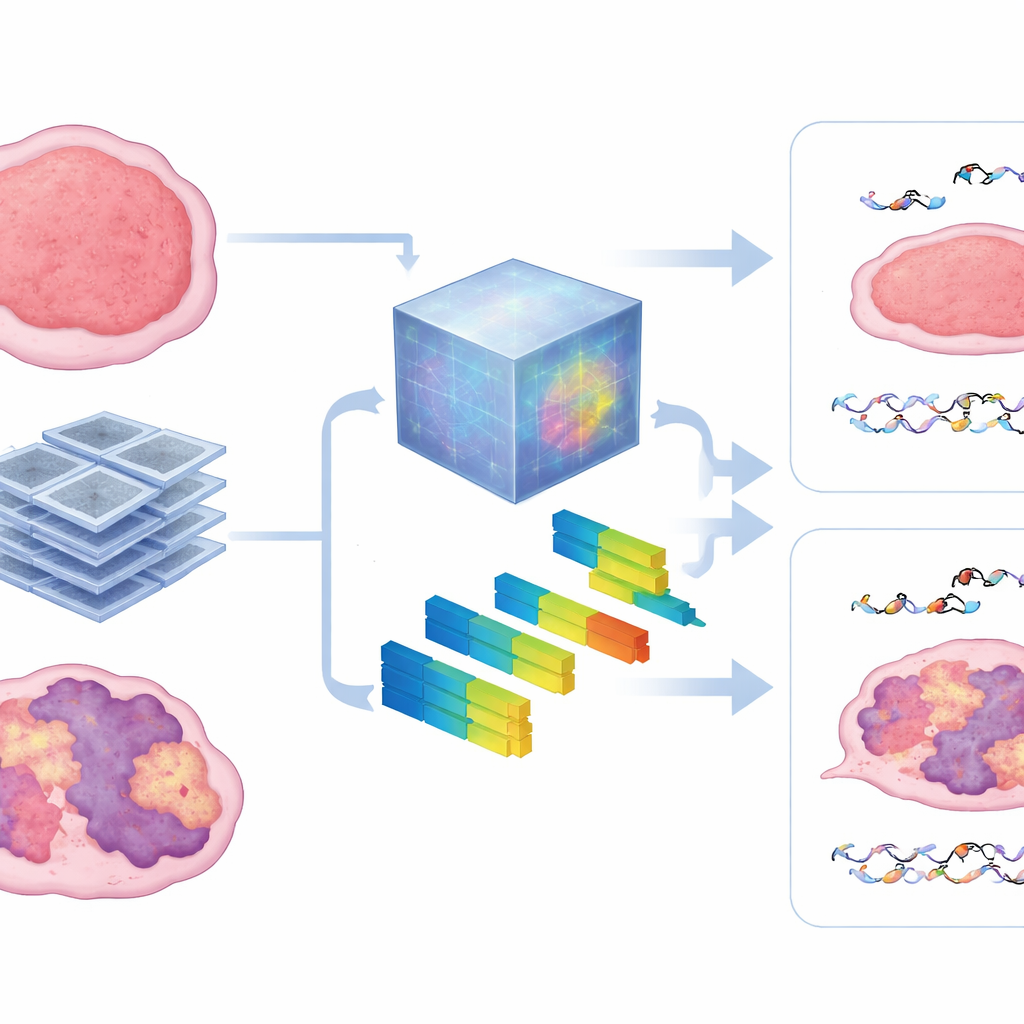
Was die Scans im Inneren des Tumors offenbaren
Um einen Blick in die Blackbox zu werfen, verglichen die Autorinnen und Autoren die vom Foundation-Modell gelernten Muster mit standardmäßigen radiomischen Merkmalen, die Textur und Intensität in Bildern beschreiben. Sie fanden heraus, dass das Modell stark auf Maße der Heterogenität setzte — wie fleckig, grob oder unregelmäßig der Tumor im CT erschien. Tumoren mit stärkeren HRD-Signaturen zeigten tendenziell unorganisiertere Texturen, und dieselben Merkmale halfen, sowohl mikroskopische DNA-Schäden als auch makroskopische Tumorkontrolle vorherzusagen. Der Ansatz blieb robust, wenn weniger Trainingsdaten verfügbar waren, was darauf hindeutet, dass solche vortrainierten Modelle ein großes Hindernis in Tierstudien überwinden können, wo das Sammeln umfangreicher Bilddatensätze schwierig ist.
Von Mausversuchen zur zukünftigen Patientenversorgung
Diese präklinische Arbeit zeigt, dass ein einziger CT-Scan, interpretiert durch eine leistungsfähige, vortrainierte KI, Signale fehlerhafter DNA-Reparatur erfassen und vorhersagen kann, wie stark ein Tumor auf ein DNA-schädigendes Medikament reagiert. Für Laien lautet die Quintessenz: Routinemäßig wirkende Scans könnten bald zweifach genutzt werden — zur Lokalisation eines Tumors und zur Einschätzung seiner Fragilität — ohne zusätzliche Eingriffe. Bevor dies Teil der Routineversorgung wird, muss die Methode jedoch an Patientinnen und Patienten getestet und validiert werden. Gelingt dies, könnten CT-basierte KI-Fingerabdrücke von HRD Ärztinnen und Ärzten helfen, Menschen genauer passenden Behandlungen wie CP-506 und verwandten Therapien zuzuordnen, die Ergebnisse zu verbessern und andere vor unwirksamen, toxischen Medikamenten zu bewahren.
Zitation: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Schlüsselwörter: homologe Rekombinationsdefizienz, Krebsbildgebung, Radiomik, Foundation-Modelle, DNA-schädigende Therapie