Clear Sky Science · de
Entwicklung und Validierung eines KI-basierten Modells zur Diagnose benigner, borderline und maligner Adnexläsionen
Warum das für die Gesundheit von Frauen wichtig ist
Ovarielle und andere Adnexläsionen sind häufige Befunde bei der Beckenultraschalluntersuchung. Dennoch ist es nach wie vor schwierig — selbst für Expertinnen und Experten — zu entscheiden, welche Veränderungen harmlos sind und welche frühe Krebszeichen darstellen. Diese Studie beschreibt ein neues System der künstlichen Intelligenz (KI), genannt Clinical‑OMTA, das Ultraschallbilder auswertet und Ärztinnen und Ärzten hilft, diese Läsionen in drei wichtige Gruppen einzuordnen — benigne, borderline und maligne — damit Frauen die richtige Behandlung erhalten und unnötige Operationen vermieden werden.
Drei Arten von Wucherungen, drei sehr unterschiedliche Entscheidungen
Nicht alle Adnexläsionen sind gleich. Benigne Läsionen können oft beobachtet oder mit einer einfachen Operation entfernt werden. Maligne Tumoren sind lebensbedrohliche Krebserkrankungen, die spezialisierte Operationen und Chemotherapie benötigen. Borderline-Tumoren liegen in einer Grauzone: Sie können wiederkehren, betreffen aber häufig jüngere Frauen, die ihre Fertilität erhalten möchten, sodass Chirurgen versuchen, möglichst schonend zu operieren. Leider können diese drei Kategorien im Ultraschall sehr ähnlich aussehen. Besonders Borderline-Tumoren können entweder eine harmlose Zyste oder einen aggressiven Krebs imitieren, was die Behandlungsentscheidung für Patientinnen und Klinikpersonal belastend macht.
Komplexe Scans in klarere Antworten verwandeln
Der Ultraschall ist in der Regel der erste und am weitesten verbreitete Test bei Adnexläsionen, doch die Interpretation der körnigen, stark variablen Bilder erfordert erhebliche Erfahrung. Bestehende Bewertungssysteme und Risikorechner, wie das weit verbreitete ADNEX-Modell, kombinieren spezifische Ultraschallmerkmale mit einfachen klinischen Angaben wie Alter und einem Blutmarker (CA125), verlassen sich jedoch weiterhin auf menschliche Beobachter, die die Bilder korrekt beschreiben müssen. Jüngste Fortschritte im Deep Learning — einem Zweig der KI, der Muster direkt aus Pixeln lernt — bieten die Möglichkeit, einen Teil dieser Subjektivität zu umgehen, indem Computer darauf trainiert werden, subtile Bildsignaturen unterschiedlicher Tumorarten zu erkennen.
Ein über viele Krankenhäuser trainierter KI-Assistent
Aufbauend auf früheren Arbeiten entwickelten die Autorinnen und Autoren Clinical‑OMTA, ein zweigleisiges KI‑Modell, das zunächst benigne von nicht‑benignen Läsionen trennt und anschließend zwischen borderline und malign unterscheidet. Das System verarbeitet Graustufen‑Ultraschallbilder und kann optional Alter und CA125‑Werte als zusätzliche Eingaben aufnehmen. Zum Trainieren und Testen des Modells stellte das Team einen großen, heterogenen Datensatz zusammen: 2381 Frauen aus 23 Krankenhäusern in China, untersucht mit 38 verschiedenen Ultraschallgeräten. Die meisten Fälle wurden chirurgisch gesichert; eine kleinere Gruppe klar benigner Zysten wurde durch mindestens sechs Monate Ultraschall‑Follow‑up bestätigt. Die Daten wurden in Trainingssets, interne Tests und zwei vollständig unabhängige externe Testkohorten aufgeteilt, die sowohl Standbilder als auch kurze Videosequenzen der Ovarien enthielten. 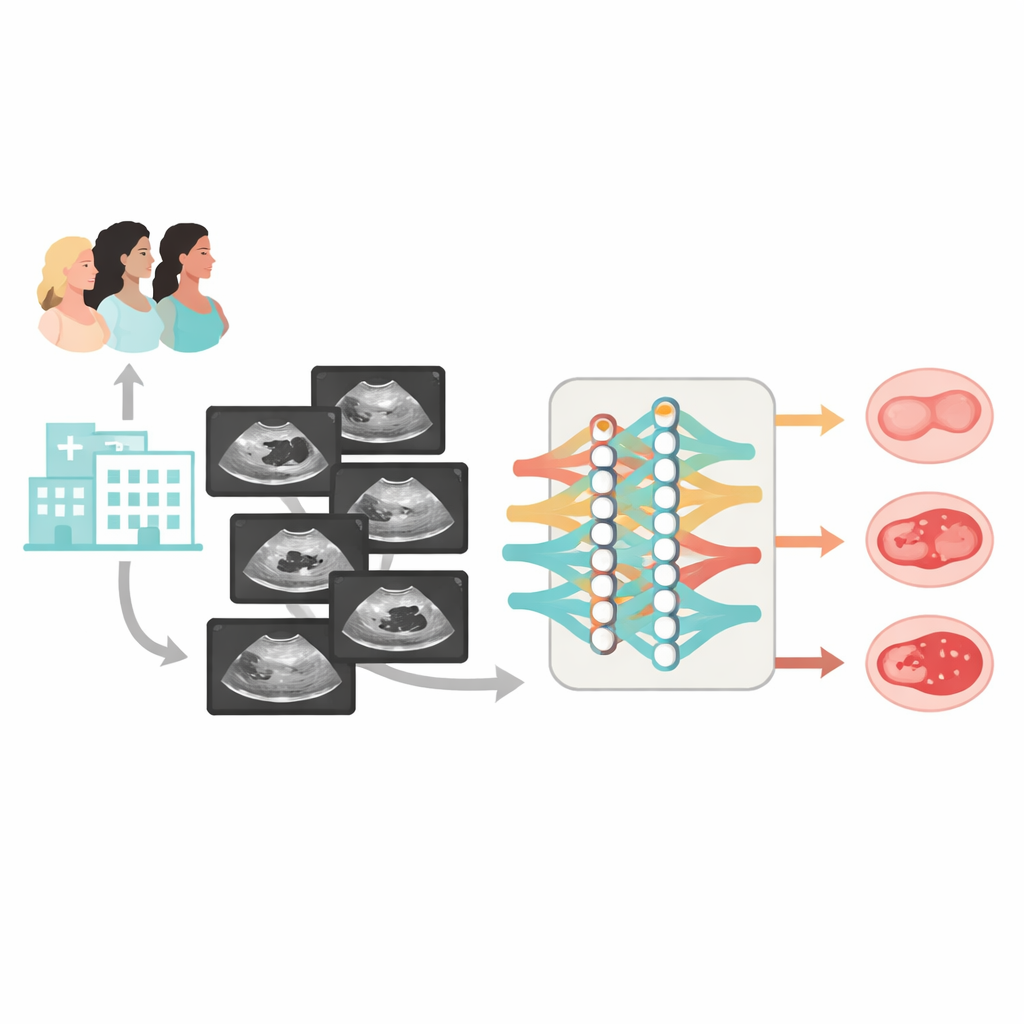
Wie gut die KI in realen Umgebungen abschnitt
An externen Testbildern unterschied Clinical‑OMTA korrekt zwischen benignen, borderline und malignen Läsionen mit einer Genauigkeit, die der des ADNEX‑Modells und dem Urteil eines erfahrenen Ultraschallexperten ähnelte. Die Leistung war über verschiedene Ultraschallmarken, Untersuchungszugänge (abdominal oder vaginal) und die beiden externen Krankenhäuser hinweg stabil, was darauf hindeutet, dass das Modell nicht übermäßig auf ein bestimmtes Gerät oder Zentrum abgestimmt ist. Das System funktionierte zudem gut bei Videoclips, nicht nur bei Einzelbildern. Interessanterweise verbesserte die Zugabe von Alter und CA125 die Entscheidungen nicht gegenüber der ausschließlichen Nutzung von Ultraschallbildern — ein Ergebnis, das frühere Studien bestätigt, wonach dieser Blutmarker wenig zusätzlichen Nutzen bringt, wenn hochwertige Bildgebung vorliegt. 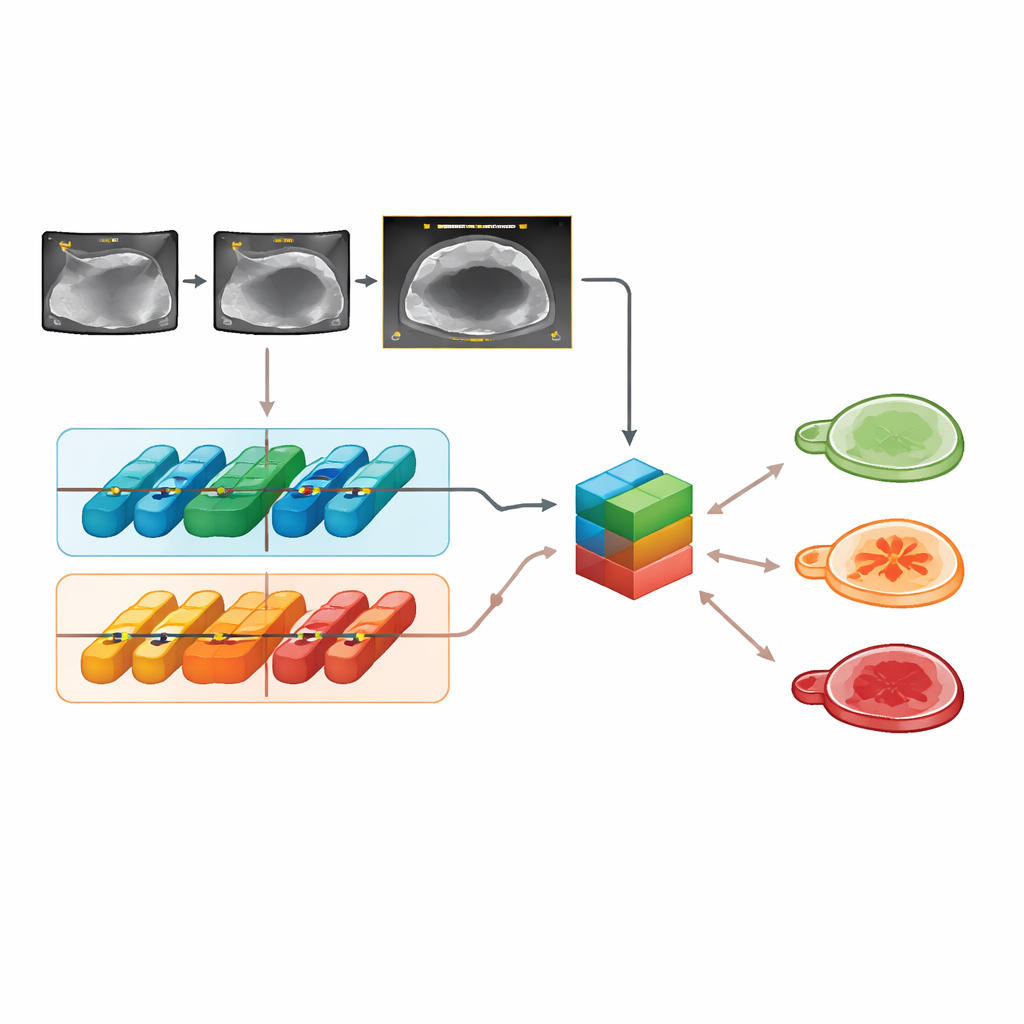
Unterstützung für weniger erfahrene Ärztinnen und Ärzte — und die Grenzen
Die Forschenden baten anschließend 11 Radiologinnen und Radiologen — junior, mittleres Erfahrungslevel und sehr erfahren — dieselben Fälle zu klassifizieren, zunächst ohne Hilfe und danach mit der Ausgabe der KI sowie Heatmap‑Overlays, die Bildbereiche hervorheben, die das Modell als wichtig erachtet. Mit Clinical‑OMTA stieg die Genauigkeit der Junior‑Ärztinnen und -Ärzte um etwa 18–20 Prozentpunkte, und auch die mittleren Leser verbesserten sich deutlich und erreichten nahezu Expertenniveau. Die Übereinstimmung zwischen den Leserinnen und Lesern, die zuvor nur von fair bis moderat reichte, erhöhte sich durch die Nutzung des Werkzeugs auf sehr hohe Werte. Gleichzeitig weisen die Autorinnen und Autoren darauf hin, dass diese starke Angleichung „Automationsbias“ widerspiegeln kann, also eine übermäßige Verlass auf die KI, insbesondere bei den am stärksten uneindeutigen Borderline‑Fällen. Sie betonen deshalb, dass Heatmaps Forschungswerkzeuge und keine eigenständigen Erklärungen sind und dass KI‑Leitlinien sorgfältig in Ausbildung und klinische Entscheidungsprozesse integriert werden müssen.
Was das für Patientinnen bedeutet
Insgesamt zeigt Clinical‑OMTA, dass ein auf vielfältigen Ultraschalldaten trainiertes KI‑System die Leistung von Expertinnen und Experten bei der Einordnung von Adnexläsionen in benigne, borderline und maligne Kategorien erreichen kann, während es gleichzeitig die Fähigkeiten und die Konsistenz weniger erfahrener Radiologinnen und Radiologen deutlich verbessert. Da das Modell über verschiedene Geräte und Zentren hinweg funktioniert, könnte es künftig in Ultraschallgeräte integriert oder als eigenständige Software eingesetzt werden, um Ärztinnen und Ärzten in stark ausgelasteten oder unterversorgten Kliniken Unterstützung zu bieten. Die Autorinnen und Autoren warnen, dass vor einer routinemäßigen Anwendung weitere prospektive und internationale Studien nötig sind, insbesondere in Umgebungen mit einfacherer Ausstattung oder nicht‑spezialisierten Anwendern. Dennoch deutet ihre Arbeit auf eine Zukunft hin, in der mehr Frauen — unabhängig davon, wo sie behandelt werden — von expertengleichen Interpretationen von Ovarialultraschallaufnahmen und besser zugeschnittener, zeitnaher Versorgung profitieren können.
Zitation: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Schlüsselwörter: Ovarialsonographie, künstliche Intelligenz, Adnexläsionen, borderline Ovarialtumoren, klinische Entscheidungsunterstützung