Clear Sky Science · de
Deletion des Y‑chromosom‑gebundenen EIF1AY treibt Geschlechtsunterschiede beim Multiplen Myelom
Warum einige Blutkrebserkrankungen Männer stärker treffen
Das multiple Myelom ist ein Krebs der antikörperproduzierenden Zellen im Knochenmark. Weltweit erkranken und sterben Männer häufiger daran als Frauen, doch die Gründe dafür waren lange unklar. Diese Studie richtet den Blick auf einen überraschenden Verdächtigen: das Y‑Chromosom. Die Autoren zeigen, wie der Verlust eines einzigen Y‑verknüpften Gens, EIF1AY, das immunologische Umfeld bei Männern in eine tumorfördernde Richtung verschiebt und damit ein mögliches neues Ziel für präzisere Therapien offenlegt.
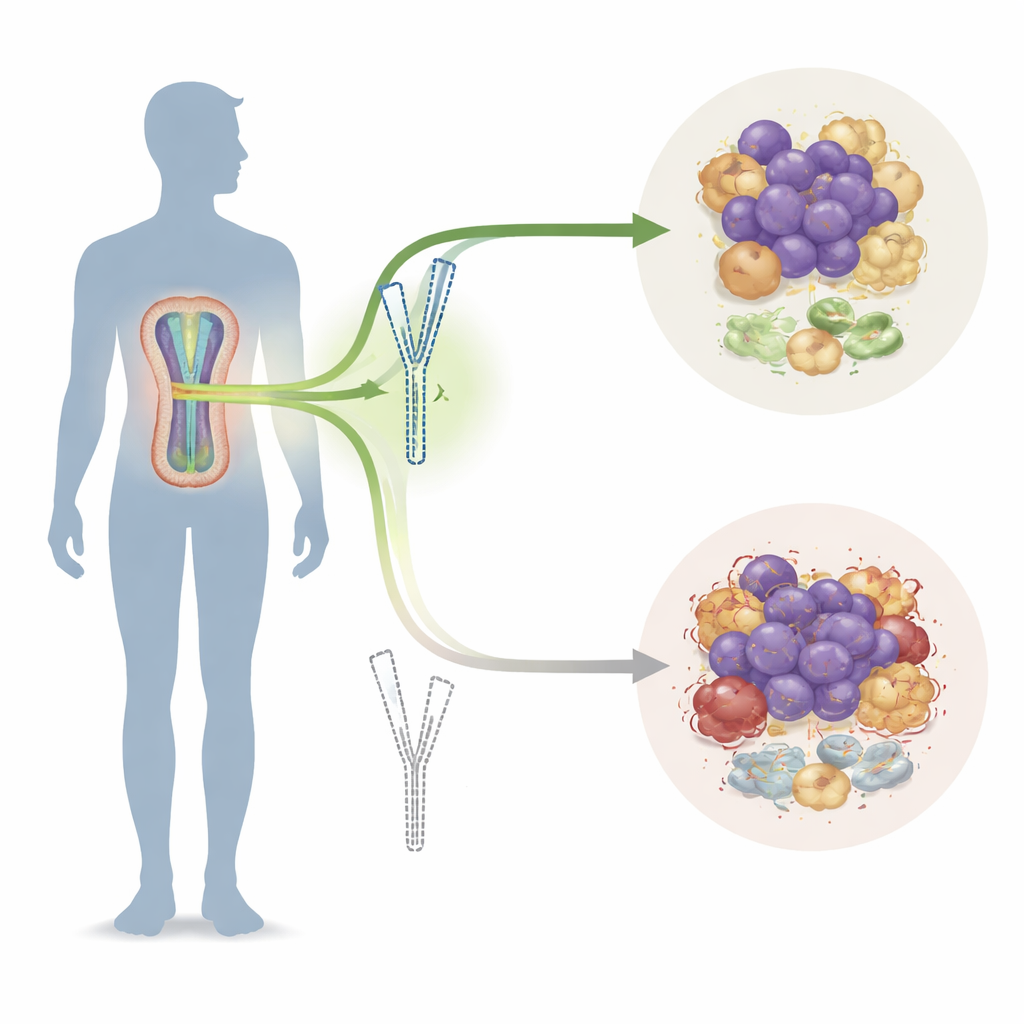
Ein geschlechtsgebundenes Indiz im Tumor‑DNA
Die Forschenden bestätigten zunächst, dass Männer mit multiplem Myelom tendenziell schlechter abschneiden als Frauen: höhere Inzidenz, weiter fortgeschrittene Krankheit bei Diagnose und kürzere Überlebenszeiten. Anschließend durchsuchten sie große genetische und klinische Datenbanken nach Genen, die sich zwischen männlichen und weiblichen Patientinnen und Patienten unterscheiden. Unter vielen Kandidaten fielen drei Y‑verknüpfte Gene durch geringere Expression bei aggressiver Krankheit auf, wobei EIF1AY als stärkster Prädiktor für ein schlechtes Ergebnis hervorging. In Blut‑ und Knochenmarkproben männlicher Patienten war EIF1AY häufig partiell vom Y‑Chromosom deletiert, besonders bei älteren Männern und bei Patienten mit fortgeschrittenem Myelom und komplexen chromosomalen Schäden. Patienten mit niedrigen EIF1AY‑Werten wiesen eine höhere Tumorlast und schlechtere Therapieansprechen auf, was dieses Gen als wichtigen Schutzfaktor kennzeichnet, den manche Tumoren zu verlieren versuchen.
Wie Immunzellen zu Helfern des Krebses gemacht werden können
Das Team untersuchte anschließend, wie EIF1AY das Tumorumfeld beeinflusst, insbesondere Makrophagen—Immunzellen, die entweder Krebs angreifen (der M1‑Zustand) oder ihn unterstützen (der M2‑Zustand). Analysen von Patientendatensätzen zeigten, dass männliche Myelomproben reicher an M2‑ähnlichen Makrophagen waren als weibliche Proben. In Laborversuchen wuchsen Myelomzellen, die mehr EIF1AY exprimierten, langsamer in Kultur und in Mäusen. Die umgebenden Makrophagen neigten weniger dazu, das tumorfördernde M2‑Programm anzunehmen, und wurden schlechter in Tumore rekrutiert. Wurde EIF1AY verringert oder verloren, geschah das Gegenteil: Mehr M2‑polarisierte Makrophagen sammelten sich an Tumorrändern und im Tumorgewebe, und diese konditionierten Makrophagen setzten wiederum Faktoren frei, die die Proliferation der Myelomzellen förderten. Im Kern wirkt EIF1AY als Bremse für diese gegenseitig verstärkende Partnerschaft zwischen Krebszellen und Makrophagen.
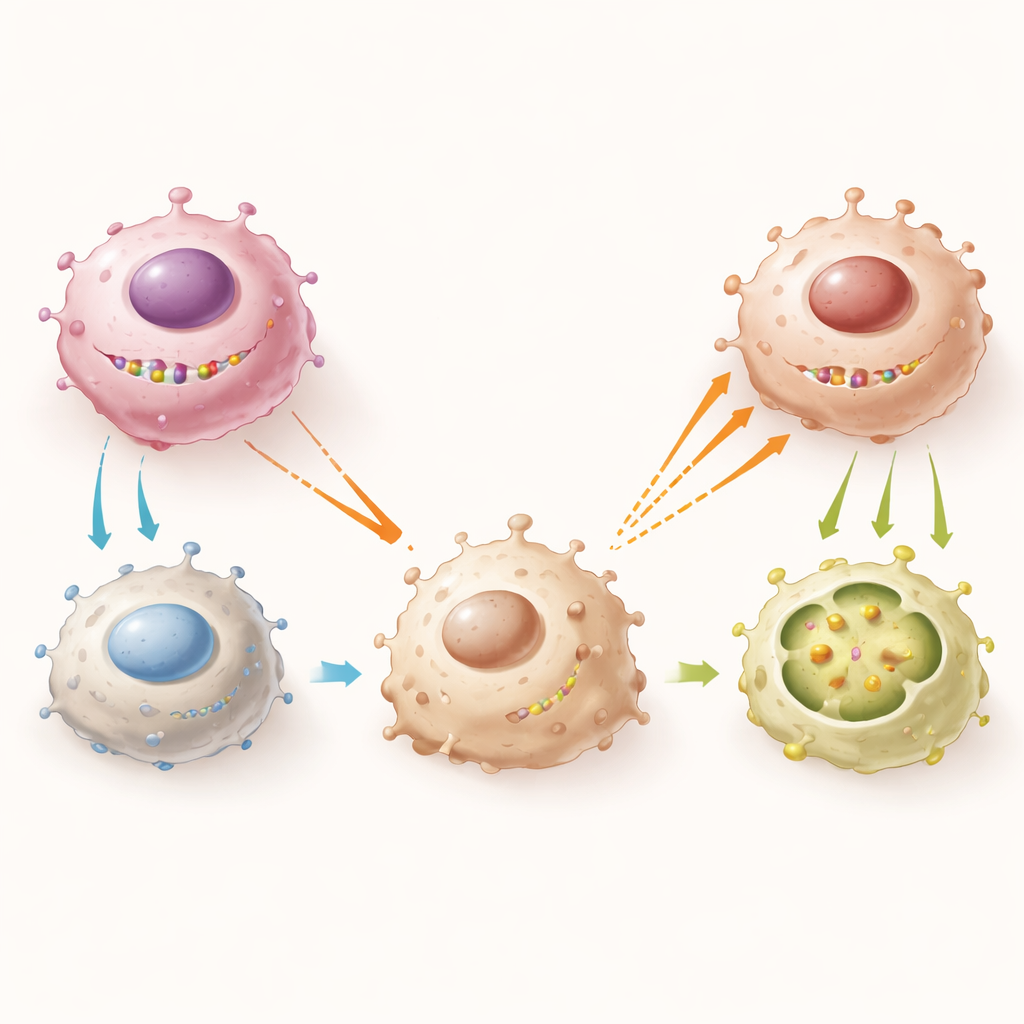
Eine molekulare Kettenreaktion von Tumorzelle zu Makrophage
Vertiefte Untersuchungen kartierten die molekulare Kette, die ein Y‑chromosomal verankertes Gen in einer Tumorzelle mit dem Verhalten benachbarter Immunzellen verbindet. EIF1AY arbeitet mit einem weiteren Y‑verknüpften Protein, RPS4Y1, zusammen und bildet einen Komplex, der physisch an die Boten‑RNA eines Oberflächenrezeptors namens CD134 in Myelomzellen bindet und diese stabilisiert. Wenn EIF1AY und RPS4Y1 vorhanden sind, bleibt CD134 auf höheren Niveaus erhalten. Das verhindert wiederum die Freisetzung großer Mengen der Signalmoleküle IL‑4 und IL‑13 durch die Tumorzellen. Niedrige IL‑4‑ und IL‑13‑Spiegel bedeuten, dass Makrophagen weniger des kollagenerkennenden Rezeptors DDR1 exprimieren, seltener M2‑ähnlich werden und weniger in den Tumor hineingezogen werden. Bei Deletion von EIF1AY bricht diese Achse zusammen: CD134‑Spiegel fallen, IL‑4 und IL‑13 steigen, DDR1 auf Makrophagen nimmt zu, und mehr M2‑Makrophagen strömen hinein, um den Tumor zu unterstützen.
Verknüpfung männlicher und weiblicher Versionen desselben Schutzmechanismus
Interessanterweise besitzen Frauen EIF1AY oder RPS4Y1 nicht, wohl aber enge Gegenstücke auf dem X‑Chromosom—EIF1AX und RPS4X. Die Studie zeigte, dass hohe Spiegel dieser X‑verknüpften Entsprechungen bei weiblichen Myelompatientinnen ebenfalls mit besseren Ergebnissen assoziiert waren. Reduzierten die Forschenden experimentell EIF1AX oder RPS4X in aus Frauen stammenden Myelomzelllinien, wuchsen die Zellen schneller—analog zu dem, was bei Männern passiert, wenn EIF1AY und RPS4Y1 verloren gehen. Das spricht dafür, dass beide Geschlechter über einen ähnlichen Schutzweg verfügen, Männer jedoch besonders verwundbar sind, weil das Y‑Chromosom in alternden Blutzellen partiell verloren gehen kann, wodurch EIF1AY und RPS4Y1 komplett entfernt werden, während die X‑verknüpften Gene bei Frauen stabiler erhalten bleiben.
Was das für Patienten und zukünftige Therapien bedeutet
Konkret zeigt diese Arbeit, dass viele männliche Myelompatienten einen schützenden Schaltkreis verlieren, der Tumorzellen dazu bringt, bestimmte Signale niedrig zu halten und benachbarte Makrophagen davon abhält, zu Komplizen des Krebses zu werden. Ist die EIF1AY–RPS4Y1–CD134‑Achse intakt, hält sie bestimmte Immun‑Signale gering, verhindert eine tumorfördernde Identität der Makrophagen und verlangsamt das Myelomwachstum. Gehen Teile des Y‑Chromosoms—insbesondere EIF1AY—verloren, fällt diese Bremse weg, wodurch eine sich selbst verstärkende Schleife aus pro‑inflammatorischen Signalen und unterstützenden Makrophagen entsteht, die die Krankheit beschleunigt. Diese Befunde helfen zu erklären, warum Männer beim multiplen Myelom schlechter abschneiden als Frauen, und legen nahe, dass die Bestimmung des EIF1AY‑Status oder die Wiederherstellung des downstream liegenden Wegs dabei helfen könnte, gezieltere Immuntherapien für männliche Patienten zu entwickeln.
Zitation: Feng, Z., Bai, J., Li, Y. et al. Y chromosome-linked EIF1AY deletion drives sex differences in multiple myeloma. npj Precis. Onc. 10, 131 (2026). https://doi.org/10.1038/s41698-026-01317-0
Schlüsselwörter: multiples Myelom, Y‑Chromosom, Tumormikroumgebung, Makrophagenpolarisation, Geschlechtsunterschiede bei Krebs