Clear Sky Science · de
Groß angelegte Einzelzellanalyse und In-silico-Perturbation enthüllen die dynamische Evolution von HCC: von der Initiation bis zur therapeutischen Zielausrichtung
Warum das Innenleben von Leberkrebs wichtig ist
Das hepatozelluläre Karzinom, die häufigste Form von Leberkrebs, ist bekanntermaßen schwer zu behandeln. Viele Patientinnen und Patienten sprechen nicht gut auf die heutigen Medikamente an, und Tumoren kommen oft zurück oder breiten sich aus. Ein wesentlicher Grund ist, dass jeder Tumor ein chaotisches Gemisch unterschiedlicher Zellen ist, die sich im Zeitverlauf verändern und kontinuierlich mit ihrer Umgebung kommunizieren. Diese Studie nutzt leistungsfähige Einzelzell- und räumliche Genexpressionsmethoden, um diese Evolution Zelle für Zelle zu verfolgen — von frühem Tumorwachstum bis zur fortgeschrittenen, therapieresistenten Erkrankung — und Schwachstellen zu identifizieren, die neue Therapien ausnutzen könnten.
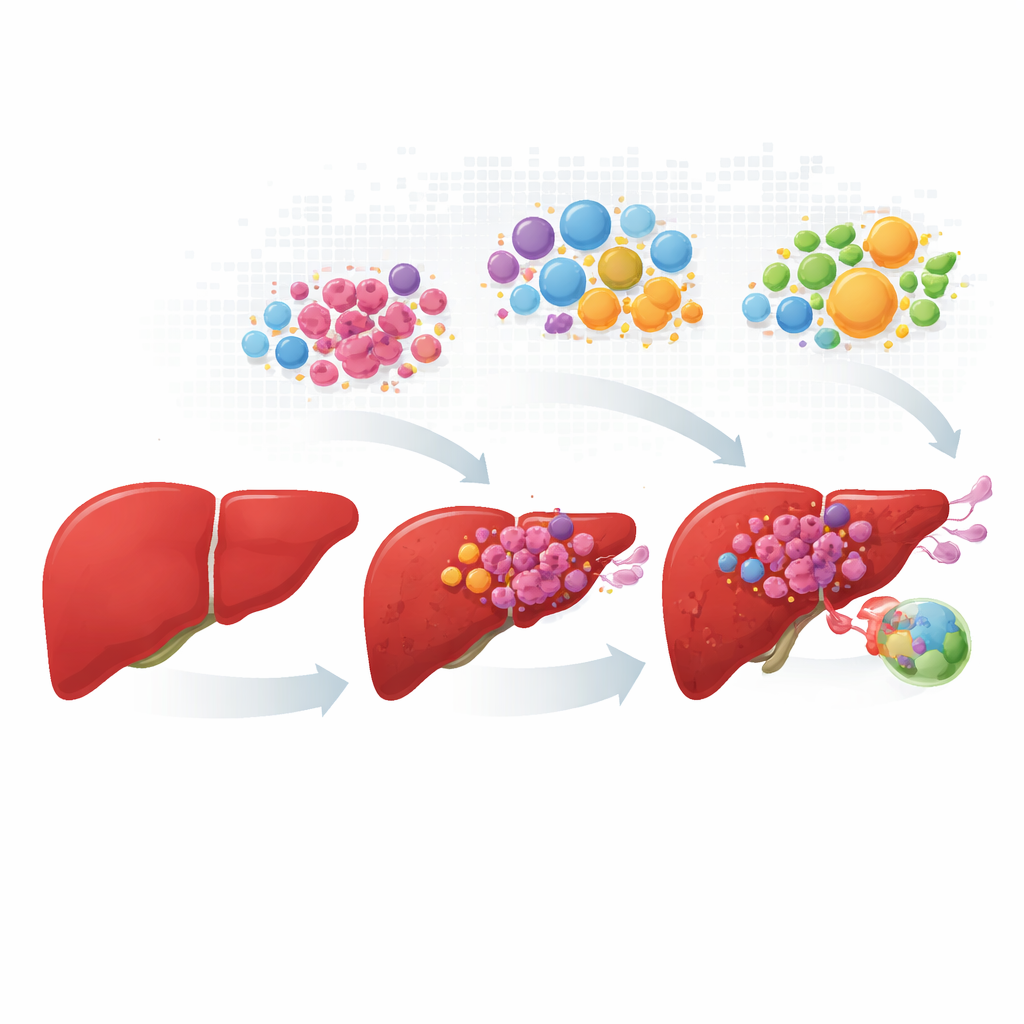
Krebszellen von frühem Umbau bis zur Ausbreitung verfolgen
Die Forschenden haben Daten von mehr als hundert Patientinnen und Patienten zusammengetragen und harmonisiert, die normales Lebergewebe, Primärtumoren, Wucherungen in Blutgefäßen und Lymphknotenmetastasen abdeckten. Anstatt jeden Tumor als einheitliche Masse zu betrachten, profilierten sie hunderte Tausende einzelner Zellen und kartierten dann, wo diese Zellen in tatsächlichen Gewebeschnitten liegen. Krebsartige Leberzellen fielen in vier wiederkehrende „Persönlichkeiten“. Eine Gruppe behielt viele normale Leberfunktionen und Stoffwechselaufgaben bei; die anderen drei zeigten stressgetriebenes Wachstum, hohe Aktivität des MYC-Wachstumswegs oder invasives, entzündungsassoziiertes Verhalten. Diese vier Zustände traten in unterschiedlichen Anteilen auf, während die Erkrankung voranschritt; schnell wachsende und invasive Zellen dominierten in Gefäß- und Lymphknotenläsionen.
Vier Tumorpersönlichkeiten mit unterschiedlichen Aussichten
Die vier Krebszellzustände waren nicht nur theoretische Kategorien, sondern korrelierten mit dem Verlauf der Patientinnen und Patienten. Tumoren, die reich an dem leberähnlichen, stoffwechselaktiven Zustand waren, gingen mit besserem Überleben einher, während Tumoren, die von den drei anderen aggressiven Zuständen dominiert wurden, tendenziell schlechtere Ergebnisse zeigten. Doch selbst der „gute“ Zustand hatte einen Haken: Er war stark angereichert bei Patientinnen und Patienten, die keinen Nutzen von dem Leberkrebsmedikament Sorafenib hatten — vermutlich, weil diese Zellen Entgiftungsmechanismen bewahren, die Arzneimittel inaktivieren können. Indem das Team Rekonstruktionen der Entwicklungsverläufe vorlegte, zeigte es, dass invasive, entzündliche Zellen sich in Richtung stärker differenzierter oder stärker proliferierender Zustände verzweigen können, was darauf hindeutet, dass Tumorzellen Identitäten wechseln und so Therapien entkommen können, die auf einen einzelnen Zustand abzielen.
Die Begleittruppe: immun- und stromale Komplizen
Krebszellen agieren nicht allein. Die Studie entdeckte spezialisierte Immunzellen und Stütz-Zellen, die entweder gegen Tumoren kämpfen oder sie stillschweigend unterstützen. Unter den Makrophagen, den „Müllsammlern“ und Wächterzellen des Gewebes, produzierten einige Typen entzündliche Signale, die die Anti-Tumor-Immunität fördern können, während andere metabolisch umprogrammiert waren, hilfreiche Signale unterdrückten und Gefäßwachstum sowie Invasion begünstigten. Diese „schlechten“ Makrophagen vermehrten sich in fortgeschrittenen Proben. Ebenso bildeten bestimmte Endothelzellen, die Blutgefäße auskleiden, und Fibroblasten, die das Bindegewebe formen, klar abgegrenzte Subsets, die mit schlechter Prognose verbunden waren. In fortgeschrittener Erkrankung schufen ein bestimmter Endotheltyp und zwei Fibroblasten-Typen eng vernetzte Knotenpunkte, die die extrazelluläre Matrix umgestalteten, neues Gefäßwachstum antrieben und mit den aggressivsten Krebszellzuständen korrelierten.
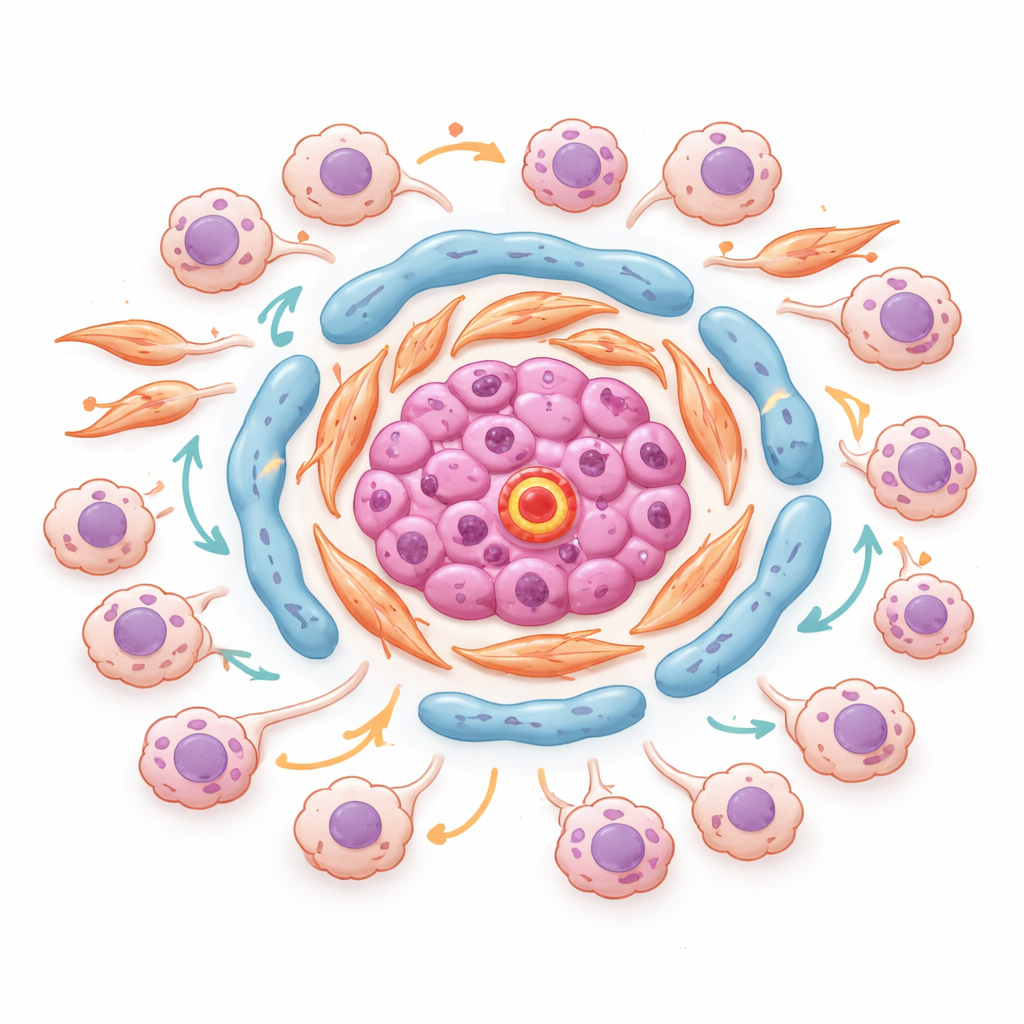
Gefährliche Nachbarschaften in Tumoren erkennen
Mithilfe räumlicher Transkriptomik, die Genaktivität misst, ohne die räumliche Anordnung der Messpunkte im Gewebe zu verlieren, identifizierten die Autorinnen und Autoren organisierte „Nachbarschaften“ innerhalb von Tumoren. In einem repräsentativen Tumor gruppierten sich Endothelzellen mit hohem Gehalt an einem Molekül namens ESM1 zusammen mit lipidhungrigen und matrixproduzierenden Fibroblasten im Kern stromaler Inseln. Um diese Kerne häuften sich stressgetriebene und invasive Krebszellen in Regionen mit starken TGF‑beta- und Niedrig-Sauerstoff-Signalen. Wichtige Transkriptionsfaktoren, die steuern, wie Zellen auf Stress und Entzündung reagieren, wurden zwischen diesen Krebszuständen geteilt und waren genau dort am aktivsten, wo Tumorzellen auf diese stromalen Knoten trafen. Das deutet darauf hin, dass spezifische Mikronischen an Tumor–Stroma-Grenzen aktiv dazu beitragen, Krebszellen in einen aggressiveren, therapieresistenteren Zustand zu drängen.
Eine geteilte Schwachstelle für neue Behandlungen finden
Um von der Beschreibung zur Intervention zu gelangen, nutzte das Team ein Machine‑Learning-Modell, das an Millionen von Zellen trainiert wurde, um „virtuelle Knockouts“ von Genen zu simulieren und vorherzusagen, welche Veränderungen schädliche Zellen wieder in gesündere Zustände zurückdrängen könnten. Beim Vergleich von Makrophagen, Endothelzellen und Krebszellen fanden sie eine kleine Gruppe von Genen, deren Abschaltung dazu beitrug, alle drei zu normalisieren. Dabei fiel HSP90B1 besonders auf: Krebszelllinien sind stark von diesem Gen abhängig, es wird in Lebertumoren überproduziert — insbesondere in solchen, die gegen zielgerichtete Therapien und Immuntherapien resistent sind — und hohe Werte sagen ein schlechteres Überleben voraus. HSP90B1 codiert für eine Stress‑bewältigende Chaperon‑Protein im zellulären Proteinfaltungsapparat, das viele Oberflächenrezeptoren und Signalwege stützt. Da selektive Wirkstoffe gegen dieses Chaperon bereits existieren und zudem das Immunumfeld umgestalten können, schlagen die Forschenden HSP90B1 als vielversprechendes Ziel vor, um Resistenzen zu überwinden — insbesondere in Kombination mit aktuellen Leberkrebsbehandlungen.
Was das für Patientinnen, Patienten und Therapien bedeutet
In der Summe zeigt diese Arbeit, dass Leberkrebs nicht eine einzelne Krankheit ist, sondern ein dynamisches Ökosystem aus Zellzuständen und Nischen, die sich verändern, während der Tumor wächst und sich ausbreitet. Indem spezifische Krebszellpersönlichkeiten, Stützzellen und räumliche Nachbarschaften mit Patientenoutcome und Medikamentenansprechen verknüpft werden, bietet die Studie eine Route zu präziseren Behandlungen: Therapien an dominante Zellzustände anpassen, stromale Knotenpunkte stören, die aggressives Verhalten fördern, und gemeinsame Abhängigkeiten wie HSP90B1 angreifen, auf die viele Tumor- und Mikroumgebungszellen angewiesen sind. Zwar sind weitere Labor‑ und klinische Tests notwendig, aber der Atlas, den das Team erstellt hat, liefert einen detaillierten Bauplan, um die interne Komplexität des Tumors von einem Hindernis in eine Chance für klügere, dauerhaftere Leberkrebsbehandlungen zu verwandeln.
Zitation: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Schlüsselwörter: hepatozelluläres Karzinom, Einzelzellanalyse, tumormikroumgebung, räumliche Transkriptomik, HSP90B1