Clear Sky Science · de
Übersetzung räumlicher transkriptomischer Signaturen in adenosquamöses Karzinom zu prognostischen Bulk-Biomarkern beim Lungenadenokarzinom: ein Bottom-up-Ansatz
Versteckte Warnsignale in Lungentumoren
Lungenkrebs gehört weiterhin zu den tödlichsten Krebsarten, teilweise weil Tumoren aus einer Mischung vieler verschiedener Zelltypen bestehen. Einige dieser Zellen können unbemerkt das Fortschreiten der Krankheit antreiben oder Therapien widerstehen, sind aber zu selten oder zu stark vermischt, um mit Standardtests erkannt zu werden. Diese Studie zeigt, wie ultra-detailreiche "Karten" der Genaktivität innerhalb von Tumoren solche verborgenen Übeltäter aufdecken und in einfache Labormarker übersetzen können, die helfen vorherzusagen, wie Patientinnen und Patienten mit Lungenkrebs abschneiden werden.
Genauerer Blick auf einen seltenen, gemischten Tumor
Die Forschenden konzentrierten sich auf einen seltenen Lungenkrebs, das adenosquamöse Karzinom, das zwei Haupttypen von nicht‑kleinzelligem Lungenkrebs in einer einzigen Masse vereint: drüsenartige Adenokarzinome und flachere, hautähnliche Plattenepithelkarzinome. Da beide Komponenten nebeneinander im selben Tumor wachsen, ist dieser Krebs ein ideales Modell, um zu untersuchen, wie Tumorzellen ihre Identität verändern können, wenn sie maligner werden. Mithilfe einer Bildgebungsmethode namens räumliche Transkriptomik erfasste das Team, welche Gene in Tausenden einzelner Zellen aktiviert sind, während deren exakte Positionen in dünnen Tumorscheiben erhalten blieben. Gleichzeitig setzten sie Standardfärbungen für zwei gängige diagnostische Marker ein, TTF‑1 (für Adenokarzinom) und p40 (für Plattenepithelzellen), um ihre High‑tech‑Karten in die Routinepathologie zu verankern. 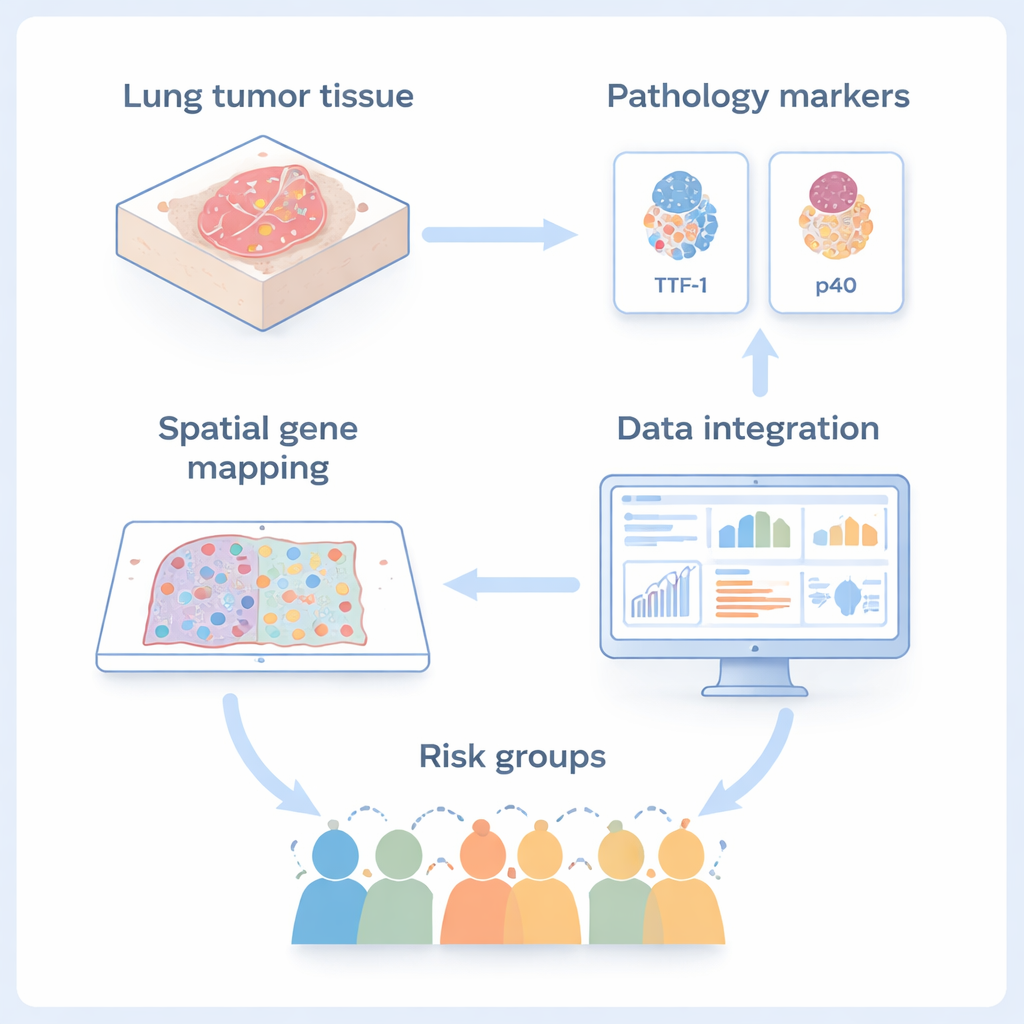
Zellen farblich kodieren, um Ausreißer zu finden
Allein das Gruppieren von Zellen nach ihren Genmustern reichte nicht aus, denn normale Lungenzellen und Tumorzellen können in Genexpressionsdaten manchmal ähnlich aussehen. Um ihren Blick zu schärfen, nutzte das Team einen Visualisierungstrick, den sie RGB‑UMAP nennen. Dabei wird das Gesamt‑Genaktivitätsmuster jeder Zelle auf drei Zahlen komprimiert und in eine Rot‑Grün‑Blau‑Farbe übersetzt. Zellen mit ähnlichem Verhalten erscheinen in ähnlichen Farben, wenn sie wieder in das Gewebebild projiziert werden. So konnten die Wissenschaftlerinnen und Wissenschaftler Inseln normaler Zellen zwischen Tumorzellen erkennen und aus der Analyse ausschließen, wodurch sichergestellt wurde, dass sie echte Krebszellen und nicht gesunde Begleitzellen untersuchten.
Entdeckung eines hybriden Zellzustands und eines wichtigen Zucker‑Tors
Nachdem normale Zellen herausgefiltert waren, suchten die Forschenden nach Genen, die stark und konsistent nur in Tumorzellen aktiv waren. Unter diesen entdeckten sie eine Gruppe von Tumorzellen, die sowohl für TTF‑1 als auch für p40 negativ waren, aber ein gemischtes Genmuster zeigten und Merkmale sowohl des Adenokarzinoms als auch des Plattenepithelkarzinoms teilten. Ein Gen stach in dieser hybriden Gruppe hervor: SLC2A1, das ein Protein namens GLUT1 codiert. GLUT1 fungiert als Tor, das Glukose, den Brennstoff der Zelle, aus dem Blutkreislauf hereinlässt. In mehreren Tumoren war SLC2A1 in den squamösen Bereichen und in den TTF‑1/p40‑negativen Zonen reichlich vorhanden, in normalem Lungengewebe dagegen fast nicht exprimiert. Das Team bestätigte dieses Muster in mehreren Patientenproben, was darauf hindeutet, dass hohe SLC2A1‑Werte eine squamöse, stoffwechselaktivere Untergruppe von Krebszellen markieren.
Von mikroskopischen Karten zu Patientenergebnissen
Um zu prüfen, ob dieser mikroskopische Befund für reale Patientinnen und Patienten relevant ist, nutzten die Forschenden große vorhandene Datensätze, in denen Bulk‑Genexpressionsdaten (gemittelt über ganze Tumorproben), DNA‑Veränderungen und klinische Verläufe für Hunderte von Personen mit Lungenadenokarzinom verfügbar waren. Als sie diese Patientinnen und Patienten nach SLC2A1‑Spiegeln in ihren Tumoren gruppierten, zeigte sich: Bei höheren SLC2A1‑Werten traten mehr Genveränderungen auf, die typischerweise bei squamösen Tumoren gesehen werden, eine stärkere Signatur eines zuckerverbrauchenden Stoffwechsels und eine signifikant schlechtere Überlebensrate. Dieser Zusammenhang hielt auch nach Berücksichtigung von Faktoren wie Alter, Tumorstadium, Rauchgeschichte und Geschlecht stand und wurde in einem unabhängigen öffentlichen Datensatz bestätigt. Im Gegensatz dazu trennten SLC2A1‑Spiegel in reinen squamösen Tumoren die Patientinnen und Patienten nicht eindeutig nach Outcome, was betont, dass dieser Marker besonders innerhalb des Adenokarzinoms aussagekräftig ist. 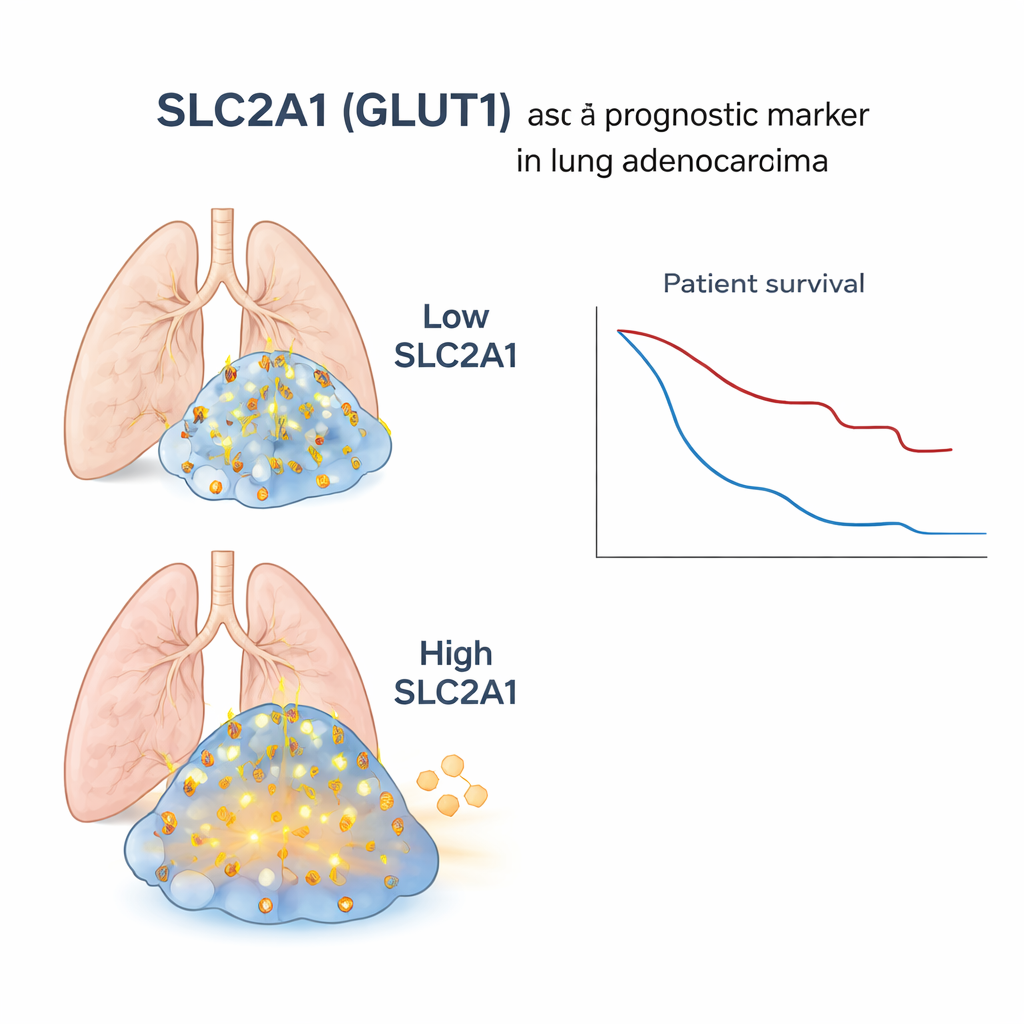
Was das für Patientinnen und Patienten mit Lungenadenokarzinom bedeutet
Für Nicht‑Fachleute lautet die Kernaussage: Innerhalb dessen, was unter dem Mikroskop wie ein einziger Lungenkrebstyp aussieht, können sich verborgene Zellnester verbergen, die sich wie ein anderer, aggressiverer Typ verhalten. Durch hochauflösende Genkartierung identifizierten die Forschenden SLC2A1 als ein einfach messbares Zeichen dieser squamös‑ähnlichen, kraftstoffhungrigen Zellen, die in Adenokarzinomen lauern. Hohe Werte dieses Gens in Routinegewebeproben markieren Patientinnen und Patienten, deren Tumoren wahrscheinlich aggressiver sind und die möglicherweise engmaschiger überwacht oder anders behandelt werden sollten. Allgemeiner zeigt die Studie einen "Bottom‑up"‑Weg — von einzelnen Zellen in einer Gewebescheibe zu Ganz‑Tumor‑Tests — der auf andere Krebsarten angewendet werden könnte, um gefährliche Zellzustände aufzudecken, die von üblichen Methoden derzeit übersehen werden.
Zitation: Hatakeyama, K., Kawata, T., Muramatsu, K. et al. Translating spatial transcriptomic signatures in adenosquamous carcinoma into bulk prognostic biomarkers in lung adenocarcinoma: a bottom-up approach. npj Precis. Onc. 10, 77 (2026). https://doi.org/10.1038/s41698-026-01297-1
Schlüsselwörter: Lungenadenokarzinom, räumliche Transkriptomik, adenosquamöses Karzinom, SLC2A1 GLUT1, Krebs-Biomarker