Clear Sky Science · de
Klonspezifische Vielfalt und Spezialisierung von T‑Zell‑Rezeptoren bei Krebserkrankungen des Verdauungssystems
Warum diese Forschung für Krebspatienten wichtig ist
Die Krebsimmuntherapie hat die Behandlung für viele Menschen revolutioniert, wirkt jedoch nicht bei allen gleichermaßen gut. Diese Studie blickt tief in die „Barcode“-Muster der Immunzellen — T‑Zell‑Rezeptoren — in Tumoren des Verdauungssystems, darunter kolorektale und Magenkarzinome. Durch das groß angelegte Auslesen dieser Barcodes zeigen die Forschenden, wie das Immunsystem Tumoren erkennt, wie sich diese Erkennung zwischen Krebsarten unterscheidet und wie sie sich verändert, wenn kolorektaler Krebs metastasiert. Diese Erkenntnisse könnten Ärzten helfen, Prognosen besser zu stellen und präzisere, personalisierte Immuntherapien zu entwickeln.
Der Fingerabdruck des Immunsystems in Tumoren
T‑Zellen sind die gezielten Verteidiger des Körpers; jede trägt einen einzigartigen Rezeptor, mit dem sie bestimmte abnorme Zellen, einschließlich Krebszellen, erkennt. Das Team sequenzierte T‑Zell‑Rezeptoren aus 415 Tumorproben von 145 Patientinnen und Patienten mit kolorektalen, Magen‑ und Lebertumoren und kombinierte diese Daten mit detaillierten klinischen Informationen. Sie untersuchten mehrere Rezeptorketten, die zwei zentrale T‑Zell‑Familien definieren: konventionelle αβ‑T‑Zellen, die den Großteil adaptiver Immunantworten antreiben, und γδ‑T‑Zellen, die eher als Schnellreaktions‑Wächter fungieren. Sie fanden, dass αβ‑T‑Zellen dazu neigen, große, sehr variable Klone zu bilden, während γδ‑T‑Zellen kleinere, stärker spezialisierte Gruppen bilden. Patientinnen und Patienten mit fortgeschrittenerem Krankheitsstadium, Gefäßinvasion oder Fernmetastasen wiesen komplexere T‑Zell‑Rezeptormuster auf, was darauf hindeutet, dass Tumorprogression das Immunsystem in eine breitere, kompliziertere Auseinandersetzung treibt.
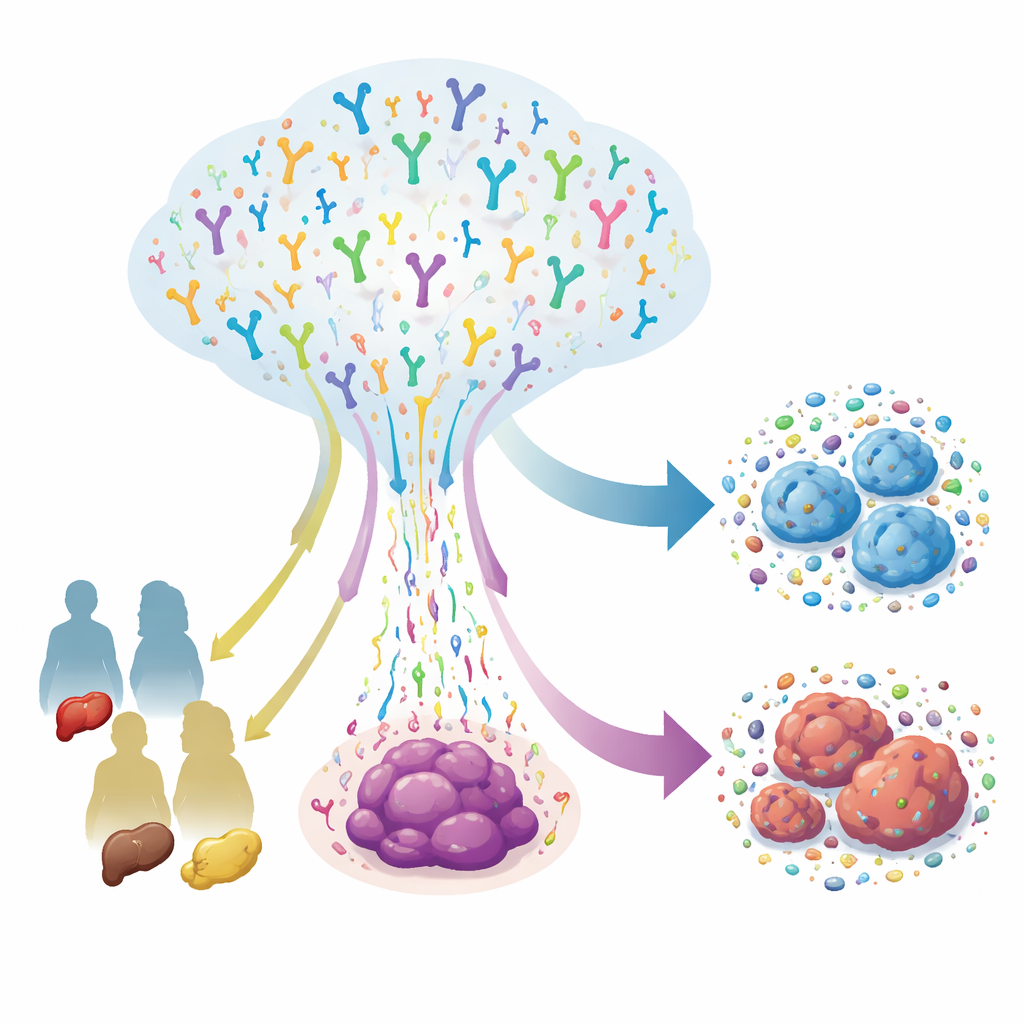
Verschiedene Krebsarten, verschiedene Immunstrategien
Obwohl diese Tumoren alle im Verdauungssystem entstehen, ziehen sie T‑Zellen nicht in gleicher Weise an oder formen sie unterschiedlich. Kolorektale Karzinome zeigten eine Anreicherung bestimmter Kombinationen von Rezeptorgen‑Segmenten in der klassischen β‑Kette, was auf eine starke Rolle konventioneller T‑Zellen hinweist. Magenkarzinome dagegen nutzten stärker γδ‑T‑Zell‑Rezeptoren, was andeutet, dass diese weniger untersuchten Wächter bei Magen Tumoren eine besondere Rolle spielen könnten. Beim Hineinzoomen auf den kritischsten Teil des Rezeptors — die kurze Schleife, die tatsächlich Kontakt zu Zielen aufnimmt — fanden die Forschenden über die Krebsarten hinweg gemeinsame Sequenzmuster, Hinweise darauf, dass T‑Zellen durch gemeinsame Selektionsdrücke gelenkt werden. Gleichzeitig gab es deutlich unterschiedliche Längen, Aminosäurezusammensetzungen und kleine wiederkehrende „Motife“, die darauf hindeuten, dass jede Tumorart die T‑Zellen vor leicht unterschiedliche Erkennungsaufgaben stellt.
Geteilte und einzigartige Ziele für Immunangriffe
Mithilfe einer globalen Datenbank bekannter T‑Zell‑Antigen‑Paare verknüpften die Autorinnen und Autoren spezifische Rezepturmuster mit ihren wahrscheinlichen Zielantigenen. Einige Antigene traten sowohl bei kolorektalen als auch bei Magenkarzinomen auf, darunter bekannte Treiber und immunrelevante Proteine wie KRAS, SF3B1, BST2 sowie mehrere klassische Cancer‑Testis‑Antigene. Diese geteilten Ziele könnten „pan‑cancer“ Strategien unterstützen, die dieselben Immunwerkzeuge über mehrere Tumortypen hinweg einsetzen. Zugleich zeigte jede Krebsart auch eigene, private Ziele. Kolorektale Tumoren waren mit Antigenen wie MAGEA10, WT1 und einem nur in Krebszellen gefundenen Fusionsgen assoziiert, während Magenkarzinome spezifisch das Protein PABPC1 hervorhoben, das an der Kontrolle von mRNA beteiligt ist. Solche tumor‑spezifischen Antigene sind vielversprechende Kandidaten für hochselektive Impfstoffe oder gentechnisch veränderte T‑Zell‑Therapien, die gesundes Gewebe schonen.
Wie sich Immunsignaturen verändern, wenn Krebs streut
Die Studie widmete besonderes Augenmerk kolorektalem Krebs mit bereits erfolgter Metastasierung und verglich Tumoren von Patientinnen und Patienten mit und ohne Fernmetastasen. Metastasierte Tumoren waren größer, neigten stärker zur Gefäßinvasion und zeigten höhere Blutspiegel gängiger Tumormarker. Ihre T‑Zell‑Rezeptor‑Repertoires waren ebenfalls reicher und komplexer, insbesondere in der β‑Kette, was zu einem härteren und vielfältigeren immunologischen Wettstreit passt. Durch das Nachverfolgen von Klonen, die zwischen nicht‑metastatischen und metastatischen Kontexten geteilt wurden, gruppierten die Forschenden diese in stabile, schrumpfende oder expandierende Populationen. Auffällig war, dass einige γδ‑T‑Zell‑Klone, die in Primärtumoren zunächst selten waren, in metastasierten Tumoren stark expandierten und mit wachsendem Tumorvolumen häufiger wurden. Bei den konventionellen T‑Zellen trug eine besonders expandierte Klonengruppe ein spezifisches Sequenzmotiv in der β‑Kette und zielte häufig auf MLANA, ein tumorassoziiertes Antigen. Hohe MLANA‑Expression in kolorektalen Tumoren war mit besserem Überleben der Patientinnen und Patienten verbunden, was darauf hindeutet, dass dieses Antigen Tumoren markieren könnte, die für das Immunsystem sichtbar bleiben und auf immunbasierte Therapien ansprechen.
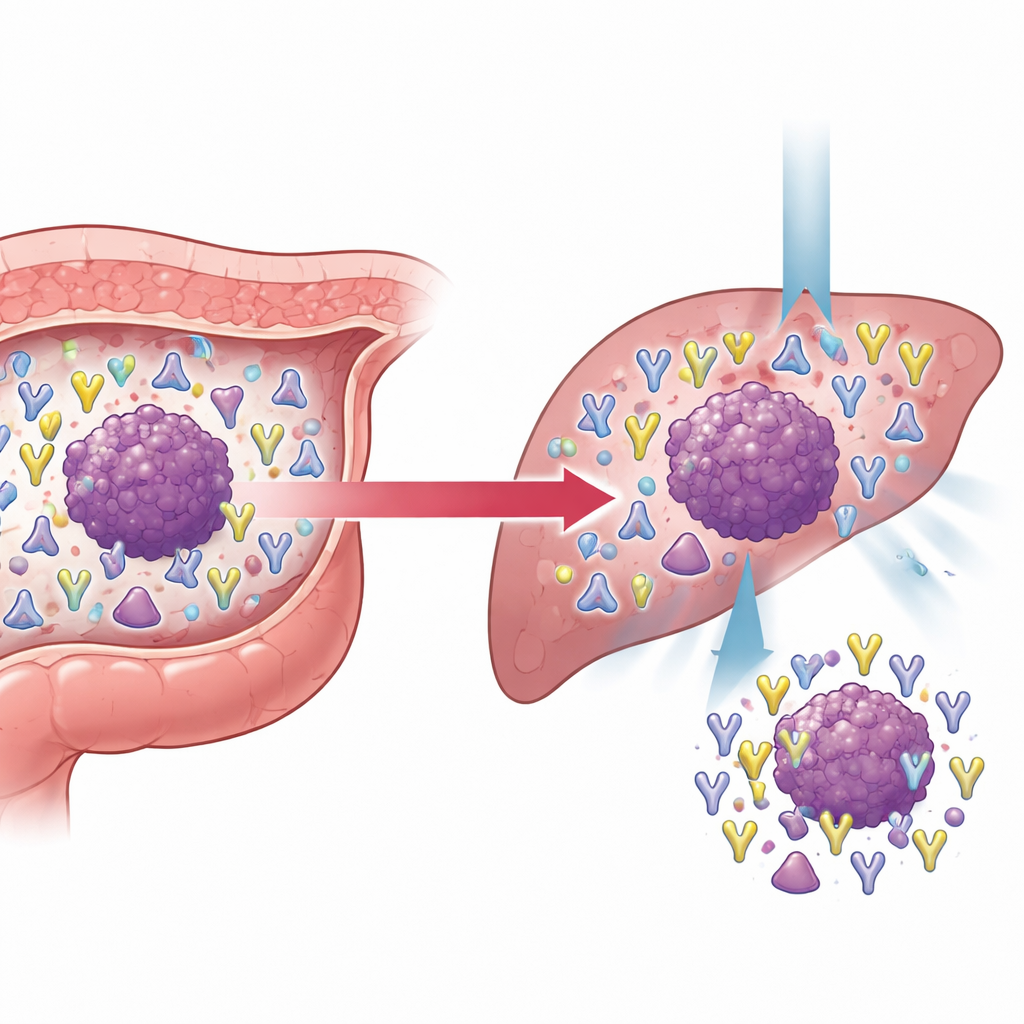
Was das für die künftige Krebsversorgung bedeutet
Insgesamt zeigt die Arbeit, dass die immunologische Landschaft in Tumoren des Verdauungssystems nicht zufällig ist, sondern durch Krebsart, Stadium und Ausbreitung geformt wird. Bestimmte Muster von T‑Zell‑Rezeptoren fungieren als ablesbare Fingerabdrücke dafür, wie das Immunsystem den Tumor angeht, und heben sowohl gemeinsame als auch krebsartspezifische Antigene hervor. Für Patientinnen und Patienten deutet das auf eine Zukunft hin, in der Ärztinnen und Ärzte T‑Zell‑Rezeptor‑Repertoires aus einer Tumorprobe analysieren könnten, um Prognosen zu verfeinern, Immuntherapien gezielter auszuwählen und sogar maßgeschneiderte Behandlungen zu entwerfen, die auf die effektivsten T‑Zell‑Klone setzen. Bei kolorektalen und Magenkarzinomen liefern die hier identifizierten Rezeptorsignaturen und Antigene eine Landkarte für solche präzisen Immuntherapie‑Ansätze.
Zitation: Li, L., Li, J., Wang, F. et al. T-cell receptor clonotypic diversity and specialization in digestive system cancers. npj Precis. Onc. 10, 91 (2026). https://doi.org/10.1038/s41698-026-01294-4
Schlüsselwörter: T‑Zell‑Rezeptoren, kolorektaler Krebs, Magenkrebs, Tumorimmunität, Biomarker für Immuntherapie