Clear Sky Science · de
Multimodale Einzelzell-Analyse enthüllt Kommunikation zwischen Makrophagen und Stromazellen bei Cholangiokarzinom-Patienten mit schlechter Prognose
Das verborgene Umfeld des Krebses
Das Cholangiokarzinom, ein Krebs der Gallengänge in der Leber, ist selten, aber häufig tödlich, und es gibt nur wenige wirksame Therapien. Viele Patientinnen und Patienten sprechen nicht auf moderne Immuntherapien an, die das Immunsystem gegen Tumore aktivieren. Diese Studie stellt eine einfache, aber entscheidende Frage: Was geschieht im „Umfeld“ des Tumors, das die Abwehrzellen des Körpers daran hindert, ihre Arbeit zu tun — und warum haben manche Patientinnen und Patienten ein deutlich schlechteres Ergebnis?
Warum Immunzellen am Tor hängen bleiben
Das Cholangiokarzinom ist nicht bloß ein lockeres Bündel von Krebszellen, sondern reich an Stützgewebe, dem Stroma, und an verschiedenen Immunzellen. Durch die Analyse einzelner Zellen aus Tumoren, benachbartem Lebergewebe und Blut zeigen die Forschenden, dass im Tumorzentrum genau jene T‑Zellen, die am wirksamsten Krebszellen töten, selten sind. Diese sogenannten Effektor‑Gedächtnis-T‑Zellen bleiben überwiegend in der umliegenden Leber und dringen kaum in den Tumor ein. Im Gegensatz dazu häufen sich regulatorische T‑Zellen — Immunzellen, die bremsen — im Tumorinneren. Viele der T‑Zellen, die es hinein schaffen, tragen mehrere „Aus‑Schalter“ an ihrer Oberfläche, ein Hinweis darauf, dass sie erschöpft und kampfunfähig sind.
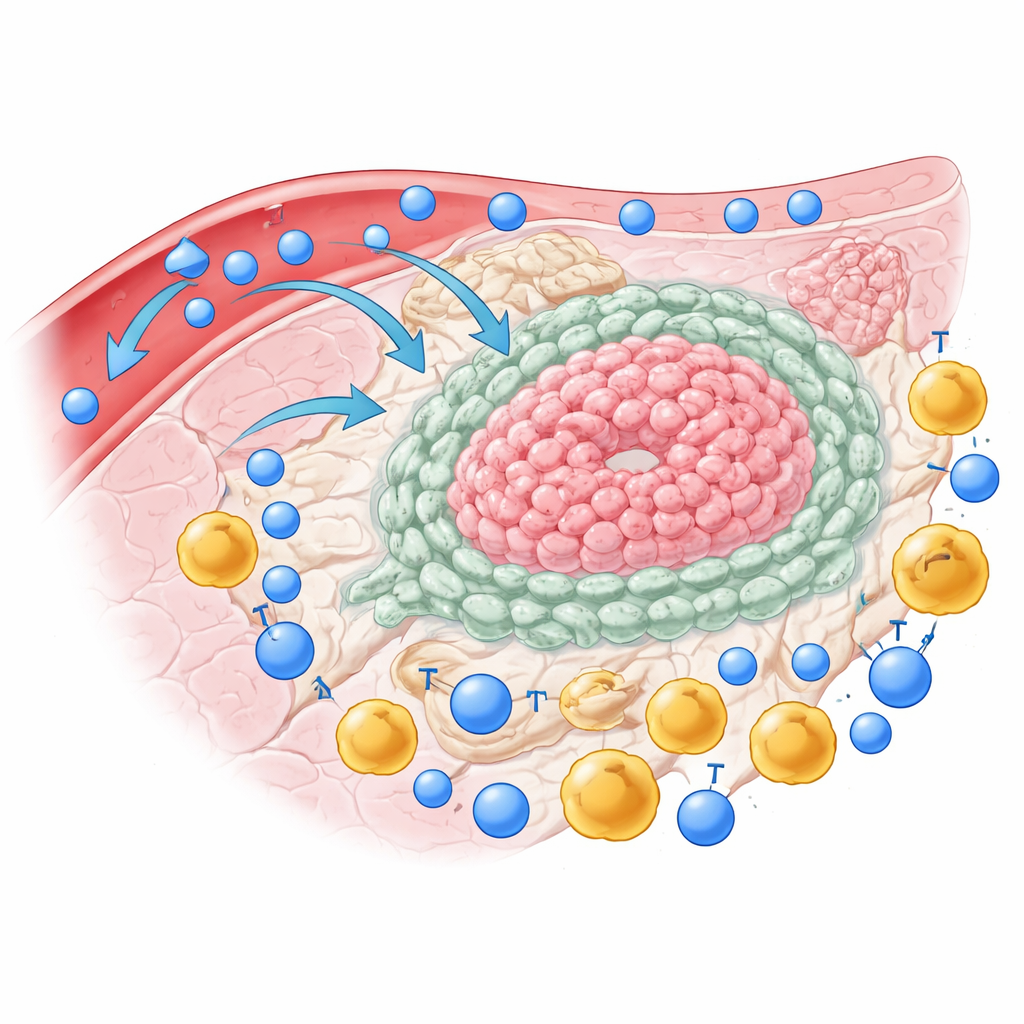
Die unterdrückende Allianz des Tumors
Um über T‑Zellen hinauszublicken, kartierte das Team tausende Einzelzellen aus Patiententumoren auf Ebene der Genaktivität. Sie fanden nicht nur mehrere Varianten von Krebszellen, sondern auch unterschiedliche Gruppen von Stützzellen wie tumorausgezeichnete Fibroblasten, Lebersternzellen, Endothelzellen der Blutgefäße und Makrophagen — Immunzellen, die entweder angreifen oder den Tumor unterstützen können. Bei Patientinnen und Patienten mit besonders schlechter Prognose zeigte eine bestimmte Untergruppe von Krebszellen stärkere Kommunikationswege mit Stromazellen und Makrophagen. Diese Zelltypen agierten nicht isoliert, sondern bildeten ein enges Netzwerk, das offenbar darauf ausgelegt ist, angreifende T‑Zellen fernzuhalten und zu deaktivieren.
Stille Signale, die die Abwehr abschalten
Bei der Untersuchung dieser zellulären „Gespräche“ identifizierten die Forschenden zentrale molekulare „Handschläge“, die von einer Zelle zur anderen weitergegeben werden. Krebszellen produzierten Versican, ein klebriges Matrixprotein, das mit Sensoren auf Makrophagen und Wachstumsrezeptoren auf Stromazellen interagiert und das Gewebe so umgestaltet, dass Tumorwachstum begünstigt und die Immunantwort abgeschwächt wird. Makrophagen setzten TGF‑beta frei, ein starkes Signal, das sowohl die Bildung regulatorischer T‑Zellen fördert als auch krebsabweisende T‑Zellen schwächt. Ein weiterer Weg involvierte GAS6, das an den AXL‑Rezeptor auf Makrophagen, Fibroblasten und Krebszellen bindet — eine Kombination, die auch in anderen Krebsarten mit aggressivem Verhalten und Immunflucht verbunden ist. Zusammen erzeugen diese Signale eine Rückkopplungsschleife: Stroma und Makrophagen remodeln die Umgebung, verstärken die Immunbremsen und unterstützen das Gedeihen der Krebszellen.
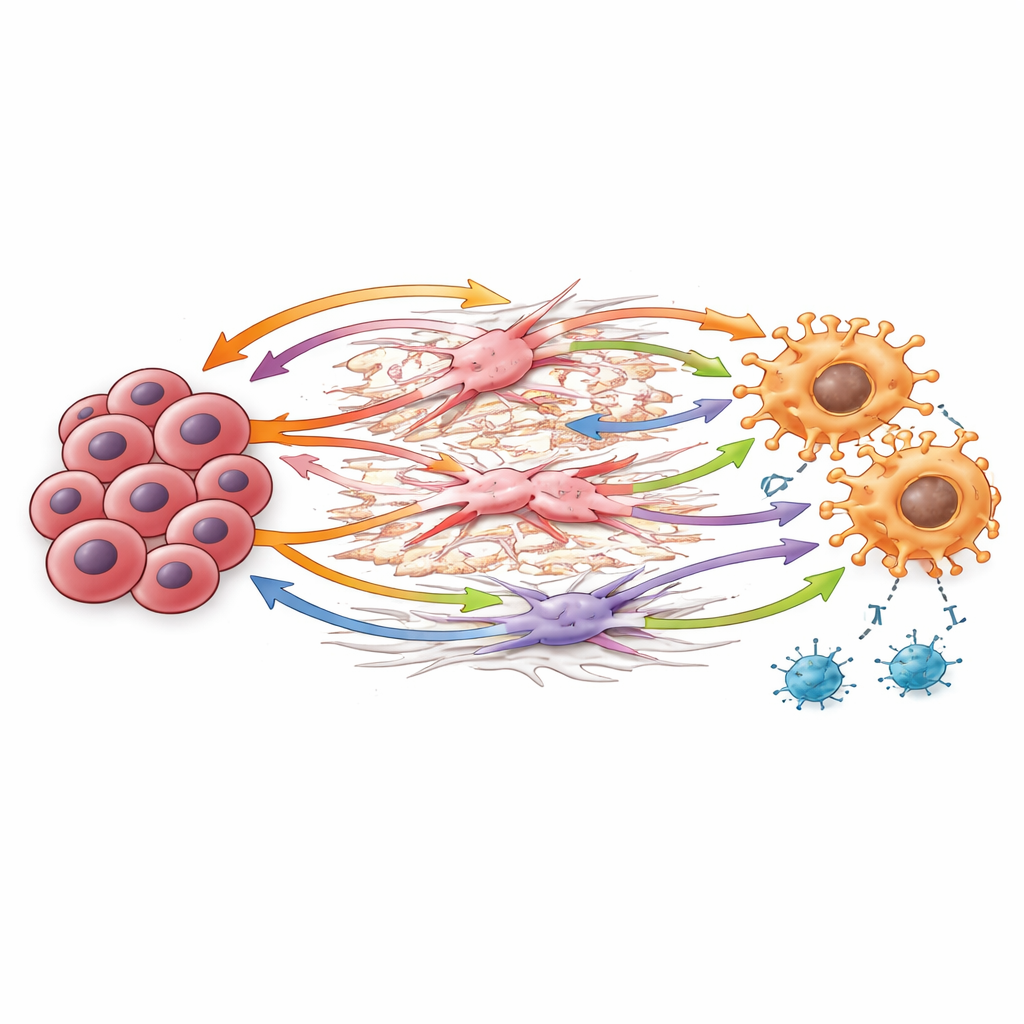
Ein Muster, das über eine kleine Gruppe hinausreicht
Obwohl die Einzelzell-Analysen an einer überschaubaren Zahl von Patientinnen und Patienten durchgeführt wurden, prüfte das Team seine Befunde anhand eines deutlich größeren öffentlichen Datensatzes von extrahepatischen Cholangiokarzinomproben. Durch mathematische Abschätzung, welche Zelltypen in jedem Tumor vorhanden waren, entdeckten sie eine beträchtliche Patientengruppe, deren Tumore reich an Stromazellen und Makrophagen waren und hohe Expression derselben Schlüsselmoleküle zeigten — Versican, GAS6, AXL und den Wachstumsrezeptor EGFR. Das legt nahe, dass das in der kleinen Studie beschriebene unterdrückende Netzwerk keine seltene Besonderheit ist, sondern eine klinisch relevante Untergruppe von Patientinnen und Patienten mit besonders aggressiver Krankheitsbiologie definieren könnte.
Was das für zukünftige Behandlungen bedeutet
Für Menschen mit Cholangiokarzinom helfen diese Befunde zu erklären, warum Standard‑Checkpoint‑Inhibitoren oft nicht ausreichen: Das Problem ist nicht nur eine einzelne Bremse auf T‑Zellen, sondern ein ganzes Zellumfeld, das zusammenarbeitet, um das Immunsystem zu dämpfen. Die Studie hebt mehrere Signalwege hervor — etwa die GAS6–AXL‑, Versican–TLR2‑ und TGF‑beta–EGFR‑Achsen — die neben Checkpoint‑Inhibitoren angegriffen werden könnten, um den Schutzschild des Tumors zu schwächen. Sie unterstreicht außerdem den Bedarf an Tests, die nicht nur Tumorzellen, sondern auch das umliegende Lebergewebe untersuchen, um festzustellen, ob aggressive T‑Zellen vorhanden sind, aber am Zutritt gehindert werden. Langfristig könnte die Entschlüsselung dieses komplexen zellulären Austauschs zu präziseren Verfahren führen, um Patientinnen und Patienten für Immuntherapien auszuwählen und Kombinationstherapien zu entwickeln, die dem Immunsystem eine echte Chance geben, zurückzuschlagen.
Zitation: Heij, L., Hayat, S., Reichel, K. et al. Multimodal single-cell profiling reveals crosstalk between macrophages and stromal cells in poor prognostic cholangiocarcinoma patients. npj Precis. Onc. 10, 105 (2026). https://doi.org/10.1038/s41698-026-01292-6
Schlüsselwörter: Cholangiokarzinom, Tumormikroumgebung, Einzelzell-Analysen, Immunerschöpfung, tumorassoziierte Makrophagen