Clear Sky Science · de
Verlust von MicroRNA-29b fördert eine DNMT3b-vermindert vermittelte STING-Downregulation und schwächt so die durch Radiotherapie ausgelöste antitumorale Immunität bei KRAS-mutiertem kolorektalem Krebs
Warum diese Forschung wichtig ist
Für viele Menschen mit Rektum- oder Dickdarmkrebs ist Strahlentherapie ein zentraler Bestandteil der Behandlung vor einer Operation. Dennoch schrumpfen manche Tumoren kaum, und der Krebs tritt häufig zurück oder streut. Diese Studie blickt auf eine häufige genetische Veränderung im kolorektalen Krebs—eine KRAS-Mutation—um zu erklären, warum diese Tumoren oft gegenüber Radiotherapie und neuen Immuntherapien resistent sind, und sie schlägt eine Strategie vor, das körpereigene Immunsystem wieder gegen sie zu aktivieren.
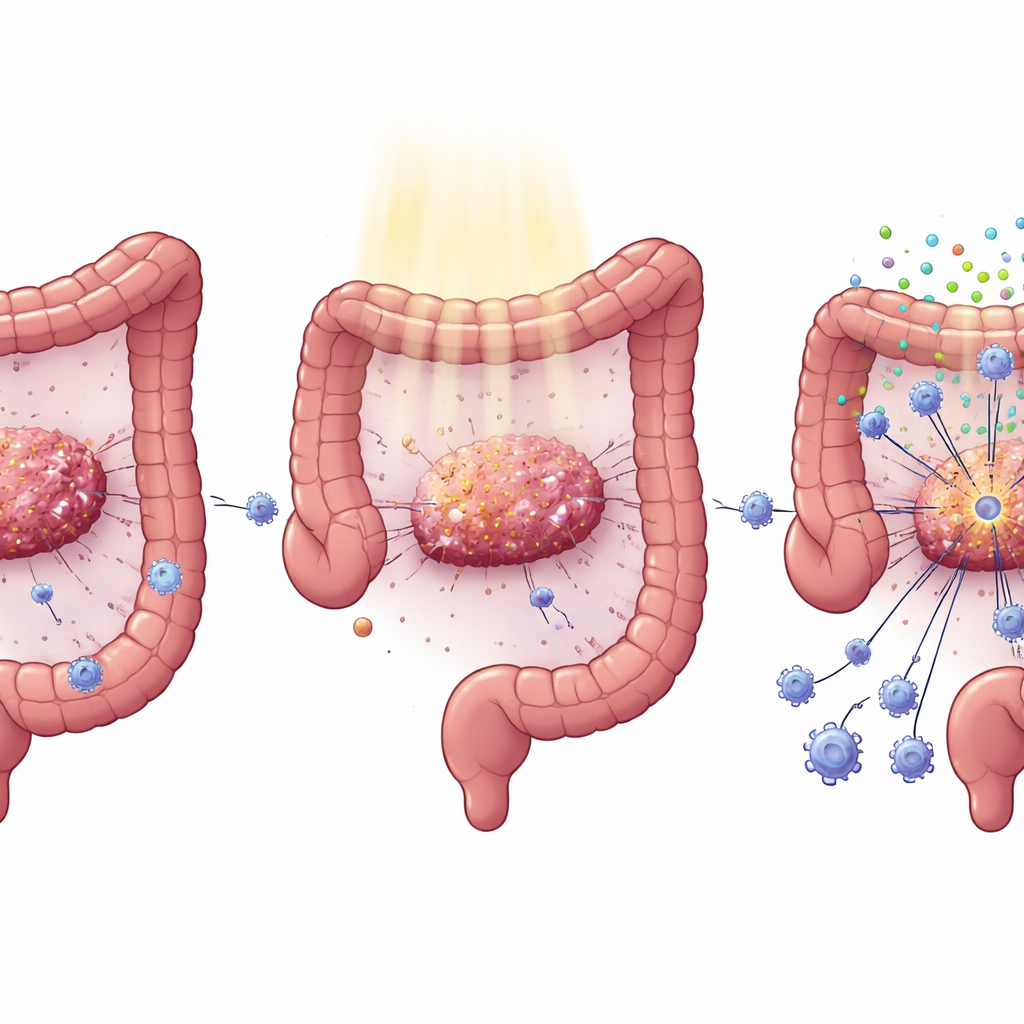
Eine häufige Mutation, die Tumoren vor Immunangriffen verbirgt
Kolorektaler Krebs trägt häufig Mutationen im KRAS-Gen, einem treibenden Faktor für Tumorwachstum und -ausbreitung. Kliniker hatten bereits beobachtet, dass KRAS-mutierte Tumoren tendenziell schlecht auf sowohl zielgerichtete Medikamente als auch auf Strahlentherapie ansprechen. Durch Auswertung großer Krebsdatenbanken und Untersuchung von Patientenproben fanden die Autorinnen und Autoren heraus, dass Tumoren mit mutiertem KRAS weniger krebsabtötende CD8-T-Zellen und eine abgeschwächte Aktivität interferon-vermittelter Immunantworten aufweisen. Bei Patientinnen und Patienten, die vor einer Rektumoperation eine standardmäßige Chemoradiotherapie erhielten, gewannen diejenigen mit normalem KRAS nach der Behandlung deutlich mehr CD8-T-Zellen in ihren Tumoren als die mit KRAS-Mutationen—was ihre besseren Ergebnisse mit erklärt.
Das fehlende Alarmsystem innerhalb der Krebszellen
Strahlentherapie schädigt nicht nur die Tumor-DNA; sie kann auch wie ein Leuchtfeuer wirken, indem Krebszellen DNA-Fragmente freisetzen, die einen internen Alarmweg namens cGAS–STING auslösen. Wenn STING aktiv ist, produzieren Zellen Typ-I-Interferone und andere Signale, die Immunzellen, darunter T-Zellen und dendritische Zellen, anlocken und aktivieren. Die Forschenden zeigten, dass dieses Alarmsystem in kolorektalen Krebszellen mit eingeführter KRAS-Mutation gedämpft ist: Nach Bestrahlung produzierten diese Zellen deutlich weniger Interferon und verwandte Moleküle. In Mäusen stellte das Abschalten von KRAS in Tumoren die STING-Spiegel wieder her, verstärkte Interferonsignale und führte zu mehr CD4- und CD8-T-Zellen, weniger regulatorischen T-Zellen und besserer Tumorkontrolle—nicht nur in bestrahlten Tumoren, sondern auch in weit entfernten, nicht bestrahlten „abscopalen“ Tumoren.
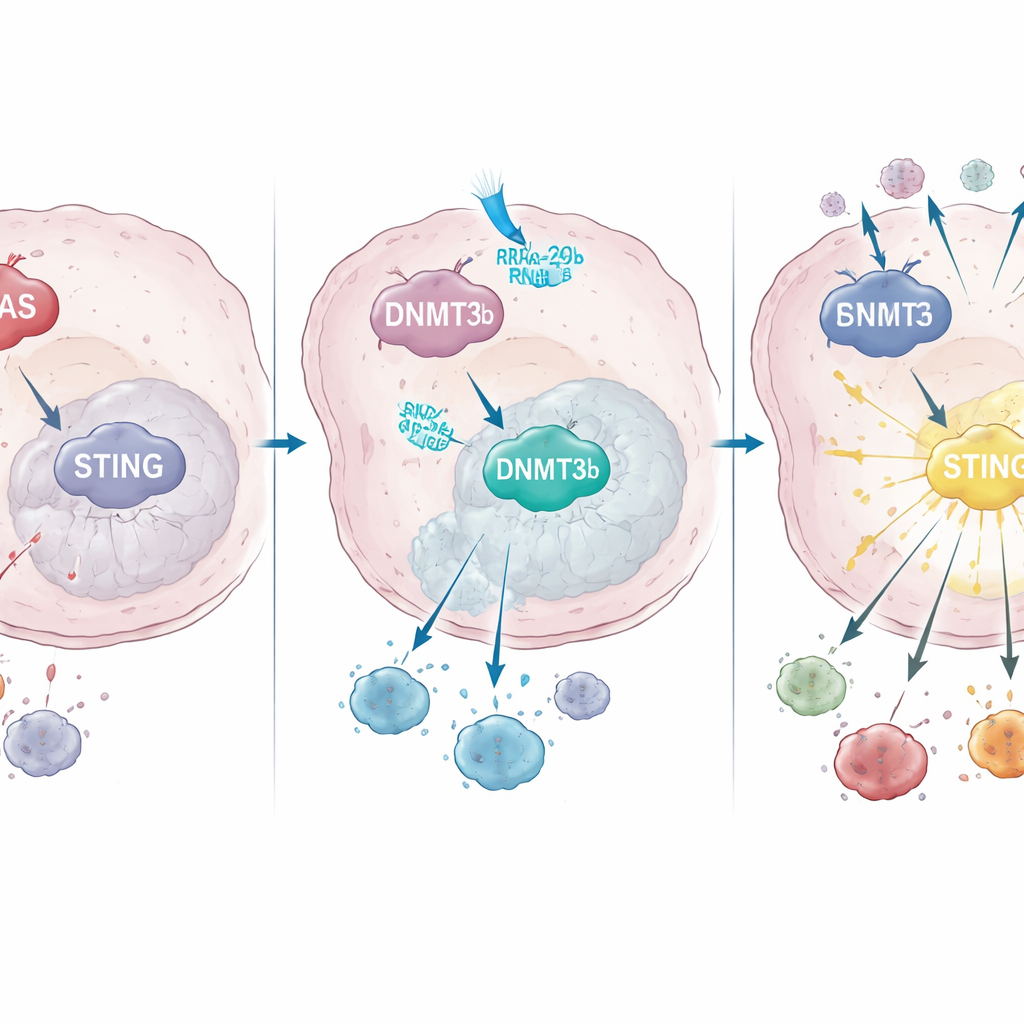
Wie KRAS die Genkontrolle umschaltet, um STING auszuschalten
Bei tiefergehender Untersuchung entdeckte das Team, dass mutiertes KRAS die Aktivität eines DNA-modifizierenden Enzyms namens DNMT3b erhöht, das Methylgruppen an bestimmte DNA-Regionen anhängt und benachbarte Gene abschaltet. Sowohl in Krebszelllinien als auch in Patientenproben ging hoher DNMT3b-Spiegel mit niedrigem STING einher. Ein entscheidender Abschnitt des STING-Promoters—die DNA-„An“-Schalter-Region—war in KRAS-mutierten Tumoren stark methyliert, nicht aber in Tumoren mit normalem KRAS. Patientinnen und Patienten, deren Tumoren nach Chemoradiotherapie STING noch hochregulieren konnten, zeigten mehr CD8-T-Zell-Infiltration und ein besseres Überleben, was unterstreicht, wie wichtig dieser Signalweg für einen erfolgreichen Therapieerfolg ist.
Eine kleine RNA, die den Alarm wieder wecken kann
Die Autorinnen und Autoren fragten dann, was DNMT3b in KRAS-mutierten Tumoren so reichlich macht. Mithilfe von microRNA-Sequenzierung identifizierten sie eine kleine regulatorische RNA, microRNA‑29b‑3p, die normalerweise DNMT3b in Schach hält, aber durch mutiertes KRAS stark unterdrückt wird. Die Wiederherstellung dieser microRNA in im Labor gezüchteten KRAS-mutierten Zellen senkte DNMT3b, belebte STING wieder und steigerte nach Bestrahlung die Interferonproduktion; ihre Blockade hatte den gegenteiligen Effekt. In Tumorproben wiesen KRAS-mutierte Patienten tendenziell niedrige microRNA‑29b‑3p-Werte, hohe DNMT3b- und niedrige STING-Spiegel auf, und jene mit höheren microRNA‑29b‑3p-Werten lebten länger—eine direkte Verknüpfung dieser molekularen Kette mit klinischen Ergebnissen.
Ein zielgerichteter Genlieferansatz, der Strahlentherapie und Immuntherapie verstärkt
Um diese Befunde in eine potenzielle Behandlung zu überführen, konstruierten die Forschenden ein harmloses Virus (AAV), das microRNA‑29b‑3p unter der Kontrolle eines hauptsächlich in kolorektalen Krebszellen aktiven Promoters liefert. In Mausmodellen mit KRAS-mutierten kolorektalen Tumoren führte die Gabe dieses AAV in Kombination mit lokalisierter Strahlentherapie zu einer dramatischen Schrumpfung sowohl der bestrahlten Tumoren als auch entfernter Tumoren, die keine Strahlung erhalten hatten. Die Tumoren zeigten geringere DNMT3b-Spiegel, mehr STING, verstärkte Interferonsignale und eine starke Infiltration durch T-Zellen und andere Immunzellen. Als dieselbe microRNA‑29b‑3p-Behandlung mit einem Immun-Checkpoint-Inhibitor gegen PD‑1 kombiniert wurde, verbesserte sich das Überleben weiter—und dieser Nutzen hing von CD8-T-Zellen ab, was bestätigt, dass das Immunsystem den Hauptanteil der Wirkung trägt.
Was das für Patientinnen und Patienten bedeuten könnte
Vereinfacht gesagt zeigt diese Studie, wie KRAS-mutierte kolorektale Tumoren die „Verkabelung“ zu einem internen Alarmsystem durchtrennen, das Strahlung normalerweise auslöst, und sich so der Immunabwehr entziehen. Durch die Wiederherstellung einer einzigen kleinen RNA, microRNA‑29b‑3p, konnten die Forschenden DNMT3b senken, STING reaktivieren und immunologisch „kalte“ Tumoren in „heiße“ verwandeln, die besser auf sowohl Strahlentherapie als auch Checkpoint-Blockade ansprechen. Obwohl diese Arbeit noch präklinisch ist, weist sie auf künftige Therapien hin, die Strahlung mit tumorzielgerichteter Gentherapie kombinieren, um die Resistenz von KRAS‑mutierten kolorektalen Tumoren zu überwinden und bestehende Behandlungen für deutlich mehr Patientinnen und Patienten wirksam zu machen.
Zitation: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Schlüsselwörter: KRAS-mutierter kolorektaler Krebs, Strahlentherapie-Resistenz, STING-Signalweg, microRNA-29b, Tumorimmunologie