Clear Sky Science · de
Hochsensitive ctDNA-Überwachung enthüllt frühe Prädiktoren für die Immuntherapieantwort bei fortgeschrittenem Krebs
Warum ein einfacher Bluttest die Krebsimmuntherapie leiten könnte
Die Immuntherapie hat die Krebsbehandlung revolutioniert, doch nur ein Teil der Patienten erfährt langanhaltenden Nutzen, und oft dauert es Monate, bis eindeutig feststeht, ob eine Behandlung tatsächlich wirkt. Diese Studie untersucht einen neuartigen Bluttest, der nach Spuren von Tumor-DNA im Blutkreislauf sucht. Indem diese winzigen Fragmente mit extrem hoher Sensitivität verfolgt werden, könnten Ärztinnen und Ärzte bereits innerhalb von Wochen erkennen, ob der Tumor eines Patienten schrumpft oder stillschweigend gegen die Behandlung resistent ist — lange bevor bildgebende Verfahren das ganze Bild zeigen.
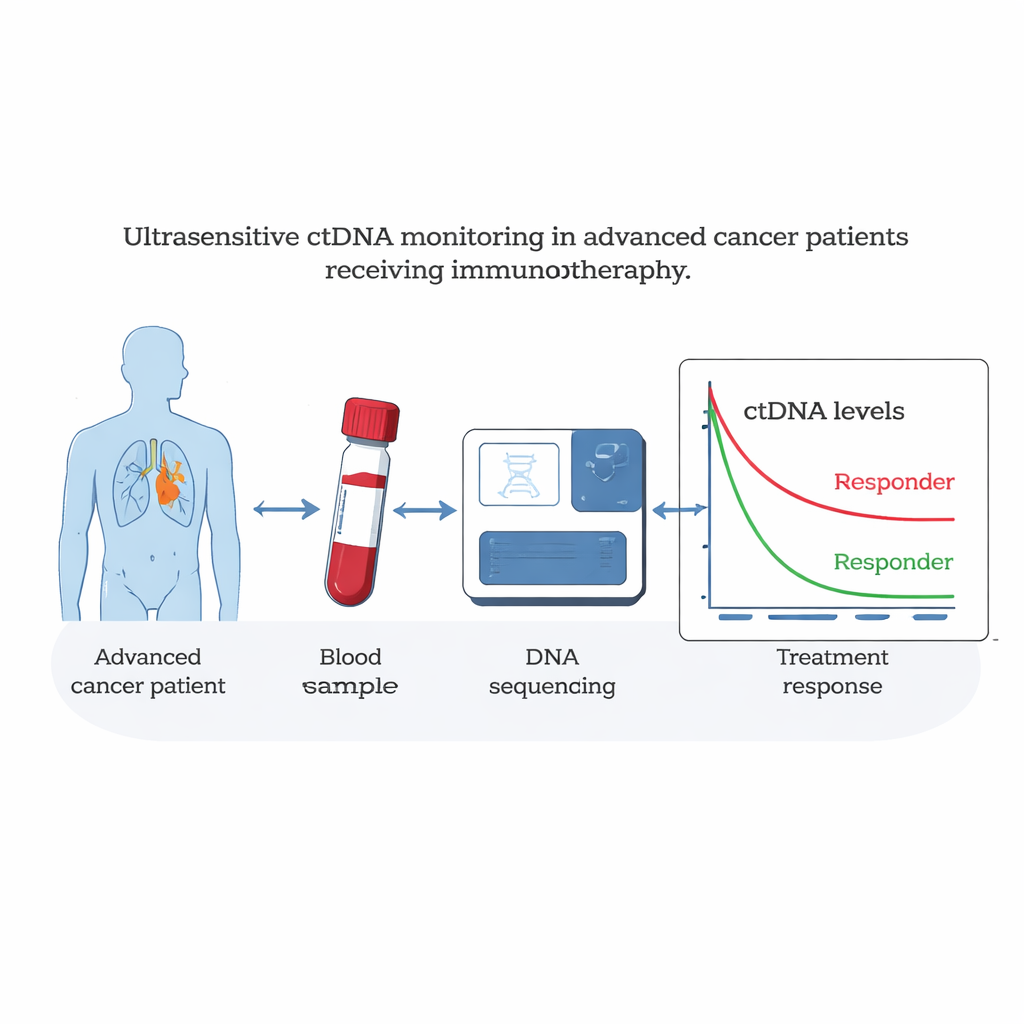
Tumoren anhand einer Blutabnahme lesen
Wenn Krebszellen absterben, geben sie Bruchstücke ihrer DNA ins Blut ab, die als zirkulierende Tumor-DNA oder ctDNA bezeichnet werden. Die Forschenden nutzten einen hochgradig personalisierten Test, der zunächst das gesamte Erbgut des Tumors und des normalen Gewebes eines Patienten sequenziert, um rund 1.800 einzigartige Tumormutationen zu identifizieren. Anschließend erstellten sie für jede Person ein individuelles Panel und nutzten tiefgehende Sequenzierung, um zu zählen, wie viele dieser tumor-spezifischen DNA-Fragmente in wiederholten Blutproben erschienen. Weil diese Methode ctDNA bis auf wenige Teile pro Million nachweisen kann, erkennt sie extrem kleine Veränderungen der Tumorlast, die Standardmethoden entgehen könnten.
Eine vielfältige Patientengruppe unter der Lupe
Das Team begleitete 39 Personen mit fortgeschrittenen oder metastasierten Krebserkrankungen, darunter Tumoren des Magen-Darm-Trakts, gynäkologische, Lungen-, Brust-, Haut-, Kopf- und Hals- sowie andere Tumorarten. Alle erhielten Checkpoint-Inhibitoren, entweder allein oder kombiniert mit Chemotherapie oder zielgerichteten Medikamenten. Im Verlauf wurden 227 Blutproben gesammelt; typischerweise gab ein Patient etwa fünf Proben während der Behandlung ab. Die meisten Patienten hatten bereits beim ersten on‑treatment-Zeitpunkt messbare ctDNA im Blut, wobei die Menge je nach Krebsart stark variierte — von sehr niedrigen Werten bei einigen Brustkrebserkrankungen bis zu sehr hohen Werten bei einigen gynäkologischen Tumoren.
Frühe Abnahmen der Tumor-DNA deuten auf bessere Ergebnisse hin
Zentrale Frage war, ob frühe Veränderungen der ctDNA vorhersagen können, wer von der Immuntherapie profitiert. Die Forschenden konzentrierten sich auf die Verschiebung der ctDNA zwischen der Ausgangsprobe und der ersten Kontrollblutentnahme, die etwa drei Wochen nach Behandlungsbeginn erfolgte. Patienten, deren ctDNA um mehr als die Hälfte sank — oder die weiterhin nicht nachweisbar blieb —, wurden als „frühe molekulare Responder“ bezeichnet. Diese Gruppe hatte deutlich längere Zeiträume ohne Krankheitsprogression als jene, deren ctDNA nicht sank, und dieser Zusammenhang blieb bestehen, selbst nachdem andere gängige Marker wie Tumormutationslast und Mikrosatelliteninstabilität berücksichtigt wurden. Wichtig ist: Selbst unter Patienten, deren Bildgebung nur eine „stabile Erkrankung“ zeigte, teilten ctDNA-Veränderungen sie in solche mit guter Prognose und solche mit hohem Progressionsrisiko auf.
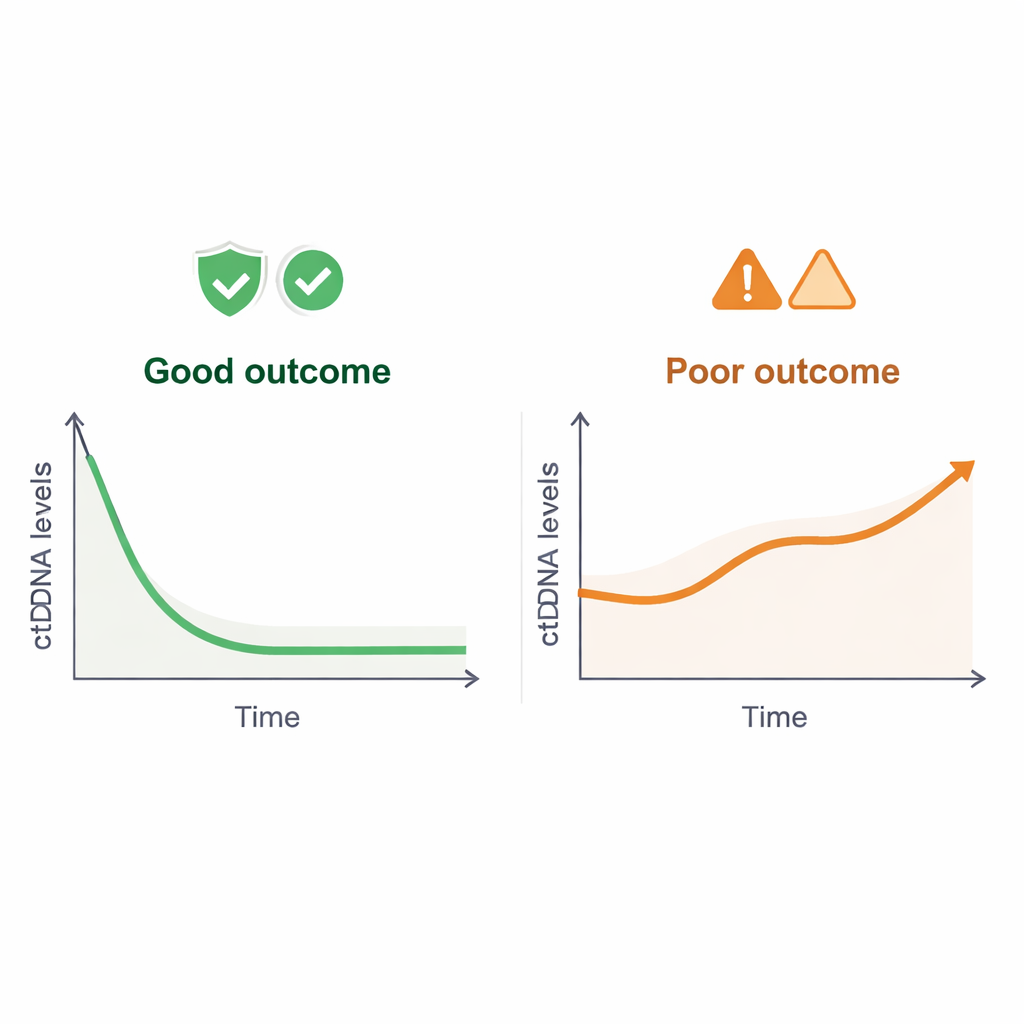
Clearing und Wiederauftreten: Was Langzeitmuster verraten
Über den gesamten Behandlungszeitraum hinweg zeigte sich, dass Patienten, bei denen die ctDNA zu irgendeinem Zeitpunkt verschwand — eine sogenannte molekulare Komplettremission —, eine deutlich bessere Gesamtüberlebensrate hatten als jene, deren ctDNA nie verschwand. Andererseits signalisierte ein anhaltender Anstieg der ctDNA um mindestens 30 Prozent eine molekulare Progression und trat oft Monate früher auf als das Tumorwachstum in der bildgebenden Diagnostik. Durch das Clustern von Patienten nach ihren ctDNA-Verlaufsmustern identifizierte die Studie eine „Niedrigrisiko“-Gruppe mit frühen Abfällen und dauerhaft niedrigen Werten sowie eine „Hochrisiko“-Gruppe mit persistierend hohen oder steigenden ctDNA-Werten. Diese Cluster korrelierten eng mit den Langzeitergebnissen, wobei die prädiktive Aussagekraft verlorenging, wenn die Analyse auf weniger empfindliche ctDNA-Schwellen beschränkt wurde.
Was das für Patienten und Ärztinnen bedeuten könnte
Für Menschen mit fortgeschrittenem Krebs kann das monatelange Warten darauf, ob eine neue Immuntherapie wirkt, qualvoll und riskant sein. Diese Studie legt nahe, dass ein hochsensitiver ctDNA-Bluttest früher und klarer Aufschluss geben könnte: Ein starker Rückgang oder das Verschwinden der Tumor-DNA deutet auf einen bedeutsamen Nutzen hin, während hartnäckige oder steigende Werte warnen, dass ein Strategiewechsel nötig sein könnte. Obwohl die Studie relativ klein war und viele Krebsarten einschloss, unterstützt sie die Vorstellung, dass das Beobachten von Anstieg oder Abfall der Tumor-DNA im Blut zu einem mächtigen Instrument werden könnte, um Immuntherapien gezielter einzusetzen, unnötige Nebenwirkungen zu reduzieren und Patienten schneller zu Behandlungen zu führen, die ihnen wirklich helfen.
Zitation: Nishizaki, D., Law, A., Li, B. et al. Ultrasensitive ctDNA monitoring reveals early predictors of immunotherapy response in advanced cancer. npj Precis. Onc. 10, 79 (2026). https://doi.org/10.1038/s41698-026-01287-3
Schlüsselwörter: zirkulierende Tumor-DNA, Immuntherapieantwort, Liquid Biopsy, fortgeschrittener Krebs, Therapiemonitoring