Clear Sky Science · de
Ein interpretierbares Deep‑Learning‑Modell zur Vorhersage molekularer Subtypen des Endometriumkarzinoms aus H&E‑gefärbten Präparaten
Warum das für die Frauengesundheit wichtig ist
Das Endometriumkarzinom, das in der Gebärmutterschleimhaut entsteht, gehört zu den häufigsten Krebserkrankungen bei Frauen, und die Sterberate steigt weltweit. Ärztinnen und Ärzte wissen inzwischen, dass dieser Krebs in mehrere molekulare „Varianten“ vorkommt, die unterschiedlich auf Operation, Strahlentherapie, Chemotherapie und neuere Immuntherapien reagieren. Heute erfordert die Bestimmung dieser molekularen Subtypen in der Regel teure und zeitaufwändige Gentests, die viele Krankenhäuser nicht ohne Weiteres anbieten können. Die vorliegende Studie untersucht, ob ein sorgfältig entwickeltes System der künstlichen Intelligenz (KI) routinemäßig erstellte Pathologie‑Präparate – die rosa‑violetten Gewebebilder, die bereits für jede Patientin angefertigt werden – lesen und diese molekularen Subtypen zuverlässig inferieren kann, um so präzisere Versorgung breiter verfügbar zu machen.
Ein genauerer Blick auf die Tumorvielfalt
Nicht alle Endometriumkarzinome verhalten sich gleich. Manche wachsen langsam und bleiben auf die Gebärmutter beschränkt; andere breiten sich früh aus und sind schwerer zu behandeln. Moderne Leitlinien teilen diese Tumoren in vier molekulare Subtypen ein, basierend auf DNA‑Veränderungen und auf der Art, wie die Zellen genetische Schäden reparieren. Diese Kategorien helfen, den Verlauf vorherzusagen und Entscheidungen zu treffen, etwa wie umfangreich eine Operation sein sollte und ob eine Patientin von einer Immuntherapie profitieren könnte. Die dafür nötigen Gentests und Spezialfärbungen sind jedoch teuer, erfordern Experteninterpretation und sind in kleineren oder ressourcenarmen Krankenhäusern oft nicht verfügbar. Pathologinnen und Pathologen vermuteten schon lange, dass viele dieser molekularen Unterschiede visuelle Hinweise in der Erscheinung von Zellen und dem Stützgewebe unter dem Mikroskop hinterlassen – doch diese Hinweise sind häufig zu subtil und komplex, als dass das menschliche Auge sie konsistent erkennen könnte.
Computern das Lesen von Pathologiepräparaten beibringen
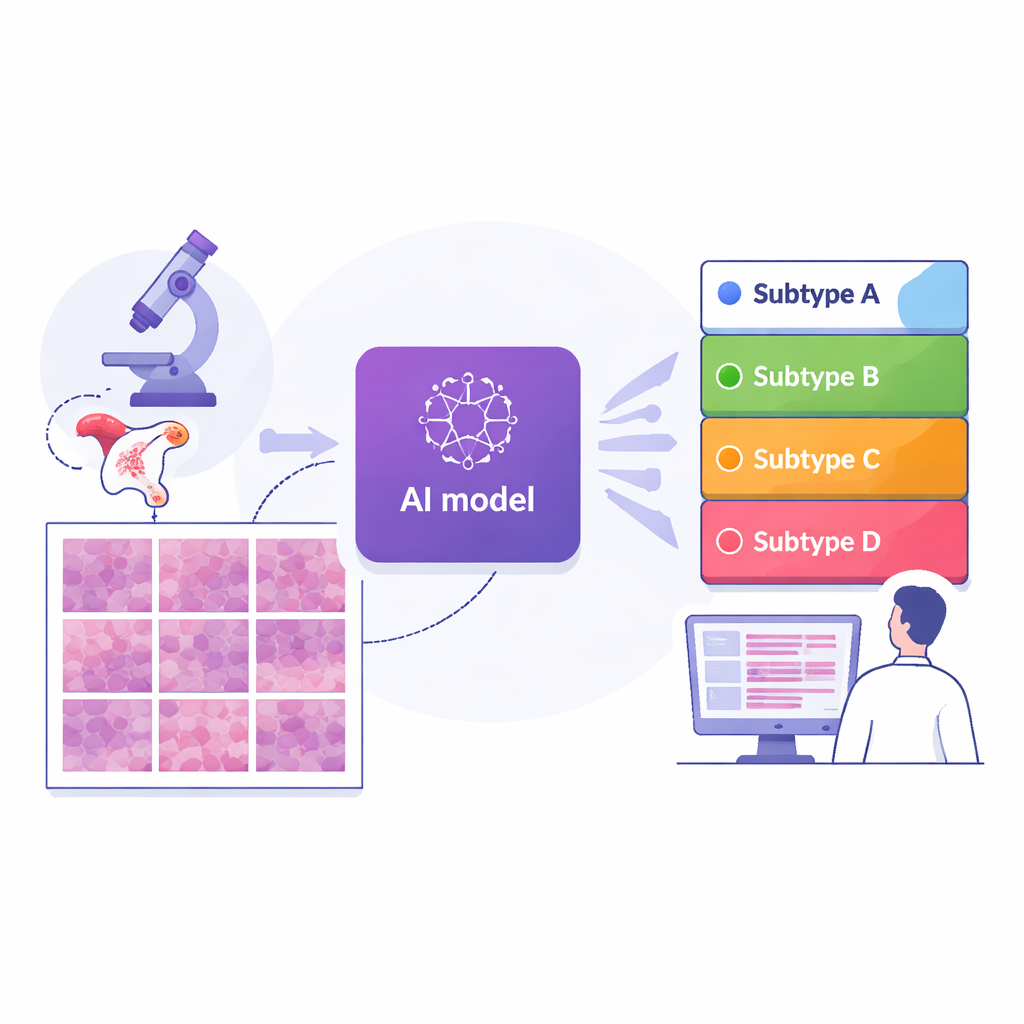
Die Forschenden stellten digitale Bilder von 364 Präparaten von 324 Patientinnen zusammen, die an einem großen Krebszentrum in Shanghai behandelt wurden, sowie zwei unabhängige Vergleichsgruppen: 296 Präparate aus einem internationalen öffentlichen Datensatz und 36 aus einem weiteren Krankenhaus in Suzhou. Jeder Fall war bereits mittels fortgeschrittener Gentests einem der vier molekularen Subtypen zugeordnet worden. Das Team teilte dann jedes Ganzschnittbild in Tausende von kleinen Kacheln und trainierte ein Deep‑Learning‑Modell – eine Form von KI, die in der Bilderkennung eingesetzt wird –, jede Kachel zu betrachten und abzuschätzen, wie wahrscheinlich sie zu jedem Subtyp gehört. Durch Mittelung der Kachel‑Vorhersagen über das gesamte Präparat erzeugte das System eine einzelne Subtyp‑Vorhersage pro Patientin, was dem klinischen Blick auf den Tumor als Ganzes ähnelt.
Wie gut das System abgeschnitten hat
In der Hauptkohorte aus Shanghai erreichte die KI ein hohes Genauigkeitsniveau: ihr Gesamtwert zur Unterscheidung der vier Subtypen (gemessen an einer standardisierten Kennzahl, die von 0,5 für reines Raten bis 1,0 für perfekte Trennung reicht) lag bei etwa 0,87. Die Leistung blieb robust – um etwa 0,84 – als das Modell an den beiden externen Gruppen aus anderen Krankenhäusern und mit unterschiedlichen Slide‑Scanner‑Systemen getestet wurde, was auf eine gewisse Robustheit der Methode hindeutet. Im Vergleich zu mehreren führenden KI‑Strategien, die komplexere Attention‑ oder Pooling‑Schemen verwenden, schnitt dieses End‑to‑End‑Modell, aufgebaut auf einem modernen Bildanalyse‑Backbone, allgemein besser ab. Wichtig ist, dass die Autorinnen und Autoren das System interpretierbar gestaltet haben: Sie nutzten Visualisierungstools, um genau hervorzuheben, welche Bereiche jeder Kachel die KI für ihre Entscheidungen heranzog.
Was die KI im Tumormikroumfeld „sah“
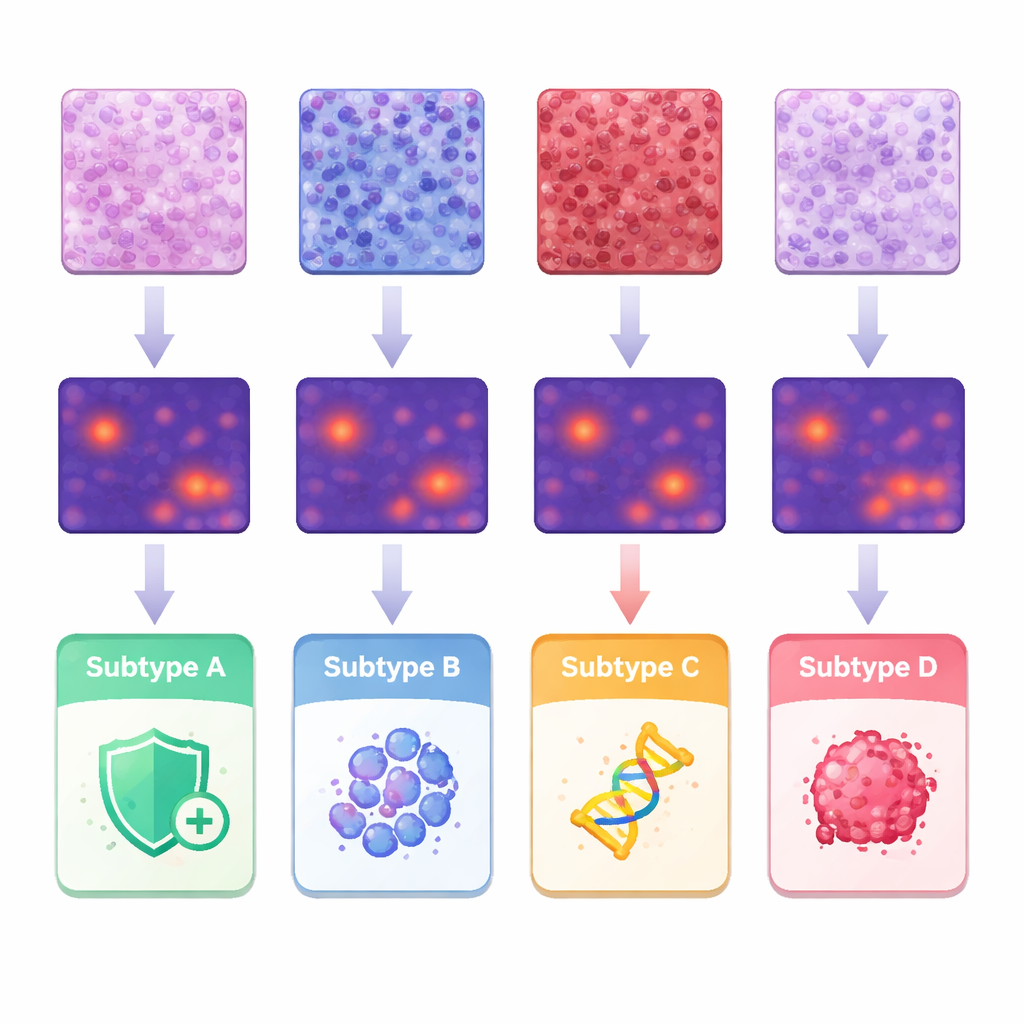
Um zu verstehen, welche Merkmale die Vorhersagen antrieben, verband das Team die Hitze‑Karten der KI mit klassischen pathologischen Beobachtungen und mit detaillierten Messungen individueller Zellformen und -anordnungen. Tumoren eines Subtyps zeigten eine dichte Infiltration von Immunzellen im Stroma, während ein anderer Subtyp dazu neigte, eng gepackte strukturelle Zellen aufzuweisen. Eine dritte Gruppe präsentierte mehr geschlossene Platten hochgradig abnormaler Tumorzellen, und der Subtyp, der mit aggressiverem Verhalten assoziiert ist, zeigte papilläre, fingerartige Strukturen und sehr unregelmäßige Zellkerne. Durch Segmentierung und Analyse von etwa 245 Millionen Zellen quantifizierten die Forschenden Unterschiede in Zellgröße, -variabilität und -abständen und zeigten, wie bestimmte Kombinationen mit spezifischen Subtypen korrespondieren. Diese Ergebnisse stützen die Idee, dass molekulare Unterschiede einen erkennbaren Abdruck in der Gewebearchitektur hinterlassen, den Maschinen systematisch detektieren können.
Vom Proof of Concept zur klinischen Unterstützung
Diese Arbeit zielt nicht darauf ab, Gentests zu ersetzen; vielmehr schlägt sie ein „H&E‑first“‑Triage‑Tool vor, das die standardmäßig für jede Biopsie angefertigte Färbung nutzt. In der Praxis könnte eine KI‑generierte Subtyp‑Wahrscheinlichkeitskarte Pathologinnen und Pathologen helfen, zu entscheiden, welche Bestätigungstests zuerst angeordnet werden sollten, begrenztes Gewebe für die aussagekräftigsten Assays zu priorisieren und Behandlungsentscheidungen zu beschleunigen – besonders in Krankenhäusern, in denen eine vollständige molekulare Charakterisierung schwer zu erhalten ist. Die Studie hebt auch aktuelle Grenzen hervor, etwa eine schwächere Leistung beim seltensten Subtyp und den Bedarf an größeren, diverseren Datensätzen vor einem Einsatz in der Routine. Dennoch liefert sie eine überzeugende Demonstration, dass routinemäßige Mikroskopbilder hinreichend verborgene Informationen enthalten, damit KI komplexe molekulare Labels annähernd ableiten kann, und ebnet so einen Weg zu gerechterer, datengetriebener Versorgung für Frauen mit Endometriumkarzinom.
Zitation: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
Schlüsselwörter: Endometriumkarzinom, digitale Pathologie, Deep Learning, molekulare Subtypen, präzisionsonkologie