Clear Sky Science · de
Ein integriertes Einzelzell-Lungenkrebs-Atlas enthüllt unterschiedliche Fibroblasten-Phänotypen zwischen Adenokarzinomen und Plattenepithelkarzinomen
Warum die Umgebung eines Tumors wichtig ist
Lungenkrebs besteht nicht nur aus Krebszellen. Er ähnelt eher einer dicht besiedelten Stadt, in der Krebszellen neben Blutgefäßen, Immunzellen und Stütz- bzw. Hilfszellen leben. Diese Studie stellt eine überraschend einfache Frage mit weitreichenden Konsequenzen: Bauen die beiden wichtigsten Formen des nicht-kleinzelligen Lungenkrebses — Adenokarzinom und Plattenepithelkarzinom — unterschiedliche „Nachbarschaften“ in der Lunge auf, und könnten diese Unterschiede helfen zu erklären, warum Patienten unterschiedlich gut abschneiden? Mithilfe leistungsfähiger Einzelzell-Analysewerkzeuge kartieren die Forschenden Hunderttausende einzelner Zellen, um zu zeigen, wie eine wichtige Gruppe von Stützzellen, die Fibroblasten, in diesen beiden Krebsarten sehr unterschiedlich agiert.
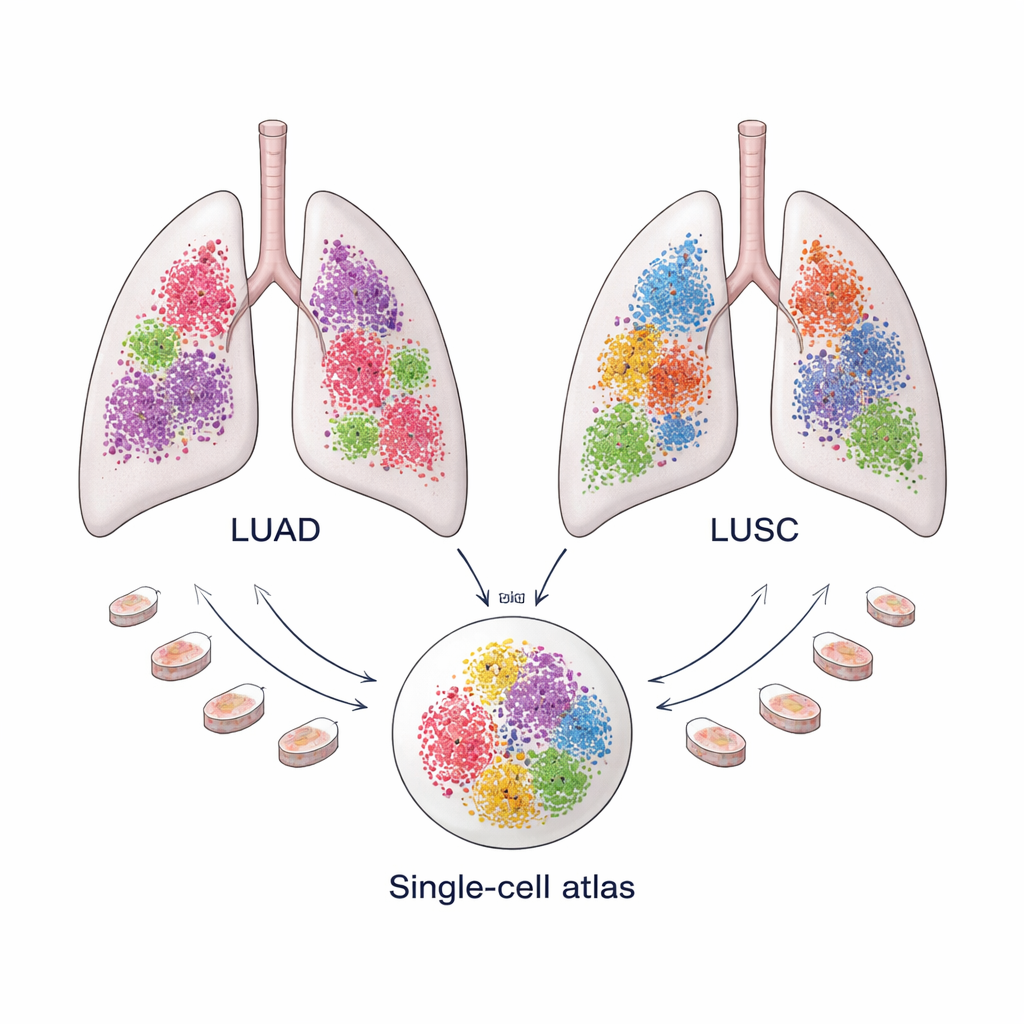
Zwei häufige Lungenkrebse, zwei unterschiedliche Ökosysteme
Das nicht-kleinzellige Lungenkarzinom macht etwa 85 Prozent der Lungenkrebserkrankungen aus und wird von zwei Typen dominiert: das Lungenadenokarzinom (LUAD), das häufig in den peripheren Bereichen der Lunge entsteht, und das Lungenplattenepithelkarzinom (LUSC), das tendenziell zentraler auftritt. Obwohl beide heute unter demselben breiten Label behandelt werden, sprechen sie unterschiedlich auf Therapien an und haben unterschiedliche Langzeitergebnisse. Zunehmende Hinweise deuten darauf hin, dass diese Unterschiede nicht nur durch die Krebszellen selbst erklärt werden, sondern auch durch die „Tumormikroumgebung“ — das Gemisch aus Immunzellen, Blutgefäßen und strukturellen Zellen, das den Tumor umgibt und mit ihm interagiert.
Aufbau eines Einzelzell-Atlas für Lungenkrebs
Um diese Mikroumgebungen im Detail zu verstehen, stellten die Forschenden einen großen „Atlas“ aus Einzelzell-RNA-Sequenzierungsdaten zusammen: 366.652 Zellen aus 175 LUAD-Proben und 125.238 Zellen aus 74 LUSC-Proben, entnommen aus zehn öffentlichen Datensätzen. Das Muster der Genaktivität jeder Zelle diente als Fingerabdruck, der es ermöglichte, Zellen in Hauptgruppen wie Immunzellen, Gefäßzellen, Krebszellen und strukturelle oder „stromale“ Zellen zu sortieren. Ausgereifte computationale Methoden entfernten technische Störungen und alignierten die Proben, sodass Zellen unterschiedlicher Patienten direkt verglichen werden konnten. Diese Größenordnung ist entscheidend, weil einige Zelltypen — besonders Fibroblasten — selten sind und in einzelnen Studien schwer in ausreichender Zahl isoliert werden können.
Fibroblasten: Die Gestalter der Tumorlandschaft
Fibroblasten sind Stützzellen, die Bindegewebe aufbauen und umgestalten. In Tumoren werden sie zu krebsassoziierten Fibroblasten (CAFs), die je nach Zustand entweder das Tumorwachstum hemmen oder fördern können. Durch die Fokussierung auf über 8.700 Fibroblasten identifizierten die Autorinnen und Autoren fünf Haupt-CAF-Subtypen: myofibroblastische CAFs (mCAFs), inflammatorische CAFs (iCAFs), gefäßassoziierte CAFs (vCAFs), teilende CAFs (cCAFs) und antigenpräsentierende CAFs (apCAFs). Das Verhältnis dieser Subtypen unterschied sich auffallend zwischen LUAD und LUSC. LUAD-Tumoren wiesen tendenziell mehr iCAFs auf, die hohe Mengen entzündlicher Moleküle sezernieren, während LUSC-Tumoren reichlicher an mCAFs waren, die steifes, faseriges Gewebe produzieren und das physische Gerüst des Tumors mitgestalten.
Krebszellen lehren Fibroblasten ihre Rollen
Um zu prüfen, ob Krebszellen die Fibroblasten dazu anleiten, diese Identitäten anzunehmen, kultivierten die Forschenden normale Lungenfibroblasten in der Nähe von LUAD- oder LUSC-Zelllinien. Unter dem Einfluss von LUAD-Zellen schalteten Fibroblasten Gene ein, die typisch für iCAFs sind, einschließlich bekannter entzündlicher Signale wie IL-6 und bestimmter Chemokine. Wurden sie mit LUSC-Zellen zusammengebracht, aktivierten dieselben Fibroblasten stattdessen mCAF-Gene, die an muskelähnlicher Kontraktion und Kollagenproduktion beteiligt sind. Analysen der Zell-zu-Zell-Kommunikation deuteten darauf hin, dass LUAD-Zellen Zytokine wie IL-1, LIF und OSM nutzen, um den inflammatorischen iCAF-Zustand zu fördern, während LUSC-Zellen stärker auf mechanische Hinweise und nicht-kanonische WNT-Signalgebung setzen, um Fibroblasten in Richtung des matrixbildenden mCAF-Zustands zu treiben.
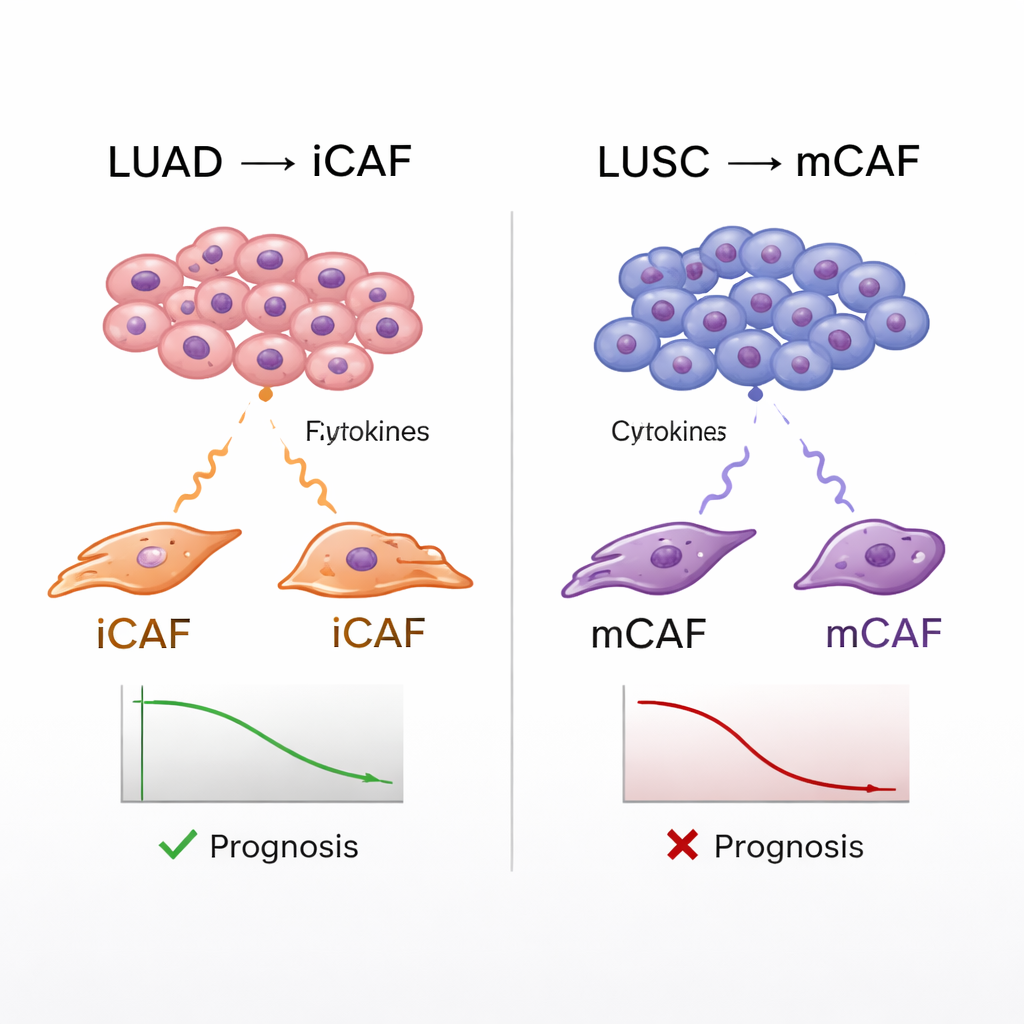
Verknüpfung von Fibroblasten-Typen mit Patientenverläufen
Der Atlas ermöglichte es dem Team auch, CAF-Subtypen mit realen Patientendaten zu verbinden. Mit großen Krebsdatenbanken schätzten sie, wie stark der Tumor jedes Patienten Expressionssignaturen für die verschiedenen Fibroblasten-Typen aufwies, und verglichen diese Werte mit dem Überleben. Sowohl bei LUAD als auch bei LUSC standen Tumoren mit Anreicherungen an mCAFs mit schlechteren Verläufen in Verbindung, was mit der Vorstellung übereinstimmt, dass eine dichte, faserige Kapsel Tumoren beim Fortschreiten helfen und Immunangriffe blockieren kann. iCAFs zeigten jedoch eine gespaltene Rolle: Bei LUSC sagten hohe iCAF-Signaturen ebenfalls ein schlechteres Überleben voraus, während sie bei LUAD mit besseren Ergebnissen assoziiert waren. Weitere Analysen ließen vermuten, dass iCAFs bei LUSC Neutrophile anziehen — Immunzellen, die in diesem Kontext offenbar hilfreiche T‑Zellen unterdrücken — und so eine besonders feindliche Umgebung für effektive Immunantworten schaffen.
Was das für die künftige Lungenkrebsbehandlung bedeutet
Für Laien lautet die Kernbotschaft: Nicht alle Stützzellen in Lungentumoren sind gleich, und derselbe Fibroblasten‑Subtyp kann je nach Tumorkontext gegensätzliche Bedeutungen haben. LUAD und LUSC unterscheiden sich nicht nur in der DNA ihrer Krebszellen; sie bauen unterschiedliche mikroskopische Ökosysteme auf, die beeinflussen, wie Tumoren wachsen und wie Patienten abschneiden. Indem diese Ökosysteme Zelle für Zelle kartiert werden, identifiziert die Studie spezifische Fibroblasten‑Populationen, die als Prognosemarker oder als Ziele zukünftiger Therapien dienen könnten — idealerweise um Behandlungen nicht nur nach dem Krebstyp, sondern auch nach der Zusammensetzung der Zellen zu gestalten, die den Tumor umgeben und erhalten.
Zitation: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Schlüsselwörter: Lungenkrebs, Tumormikroumgebung, Fibroblasten, Einzelzell-RNA-Sequenzierung, Krebsprognose