Clear Sky Science · de
TheraMind: ein Multi-LLM-Ensemble zur Beschleunigung des Drug Repurposing bei Lungenkrebs durch Auswertung von Fallberichten
Warum das für Patientinnen, Patienten und Ärztinnen wichtig ist
Für Menschen mit fortgeschrittenem Lungenkrebs ist Zeit kostbar und die Behandlungsmöglichkeiten sind oft schnell erschöpft. Die Entwicklung völlig neuer Medikamente kann mehr als ein Jahrzehnt dauern, doch verstreute Hinweise auf hilfreiche Therapien können bereits in veröffentlichten Patientenberichten — sogenannten Fallberichten — verborgen sein. Dieser Artikel stellt TheraMind vor, ein künstliches Intelligenzsystem, das Tausende solcher Berichte durchsucht, um bestehende Medikamente zu identifizieren, die möglicherweise sicher wiederverwendet werden könnten, um Menschen mit schwer behandelbarem Lungenkrebs zu helfen.
Die Herausforderung, alten Medikamenten neue Anwendungen zu geben
Das nicht-kleinzellige Lungenkarzinom ist die tödlichste Krebsart weltweit; die Überlebensraten bleiben sehr niedrig, sobald sich die Erkrankung ausgebreitet hat. Neuentwicklungen von Arzneimitteln sind langsam, teuer und riskant. Im Gegensatz dazu sind „repurposete“ Medikamente bereits für andere Indikationen zugelassen, sodass deren Sicherheit wesentlich besser bekannt ist. Onkologinnen und Onkologen interessieren sich für solche Mittel, insbesondere für Patientinnen und Patienten, die alle Standardtherapien ausgeschöpft haben, benötigen jedoch reale klinische Hinweise darauf, dass ein Medikament tatsächlich jemandem mit Lungenkrebs geholfen hat — und nicht nur vielversprechende Laborergebnisse. Diese klinischen Hinweise tauchen oft in einzelnen Fallberichten auf, die tief in der medizinischen Literatur vergraben sind und sich nur schwer und zeitaufwendig manuell finden lassen.
Ein digitaler Leser für Tausende Patientenberichte
Die Forschenden entwickelten TheraMind als unermüdlichen, sorgfältigen Leser von Fallberichten. Ausgehend von 18 Wirkstoffkandidaten, die frühere genomische und laborbasierte Studien vorgeschlagen hatten, zog das System automatisch 10.023 Fallberichte aus PubMed, der größten medizinischen Artikeldatenbank. Es übergab dann den Text jedes Berichts an drei separate Sprachmodelle — unterschiedliche KI‑„Leser“, die darauf trainiert sind, medizinische Texte zu verstehen. Für jeden Bericht beantworteten diese Modelle dieselben vier einfachen Fragen: Wird der Patient bzw. die Patientin als Träger eines nicht-kleinzelligen Lungenkarzinoms beschrieben? Wurde das Prüfmedikament speziell zur Behandlung desselben verabreicht? Wurde die Behandlung vorzeitig abgebrochen? Und erlebte der Patient bzw. die Patientin einen guten klinischen Ausgang?
Wie das KI‑Team zu einer gemeinsamen Entscheidung kommt
Sobald TheraMind jeden Bericht in eine Reihe von Ja‑/Nein‑Antworten überführt hat, greifen mehrere Entscheidungsstufen. Eine Methode verwendet einen handkodierten Entscheidungsbaum, der verlangt, dass alle vier Bedingungen erfüllt sind, bevor ein Fall als relevant für Drug Repurposing eingestuft wird. Eine andere erlaubt einem einzelnen Modell, die Evidenz flexibler abzuwägen, indem es sowohl die Ja‑/Nein‑Antworten als auch die kurzen Begründungen berücksichtigt, die es erzeugte. Die leistungsfähigste Methode kombiniert drei separate Klassifizierer, die jeweils auf einem anderen Modell basieren, und akzeptiert einen Bericht nur, wenn mindestens zwei der drei zustimmen, dass er relevant ist. Dieser „Mehrheitsentscheid“-Ansatz hilft, individuelle Fehler auszugleichen — ähnlich wie mehrere unabhängige Ärztinnen und Ärzte, die denselben Befund überprüfen.
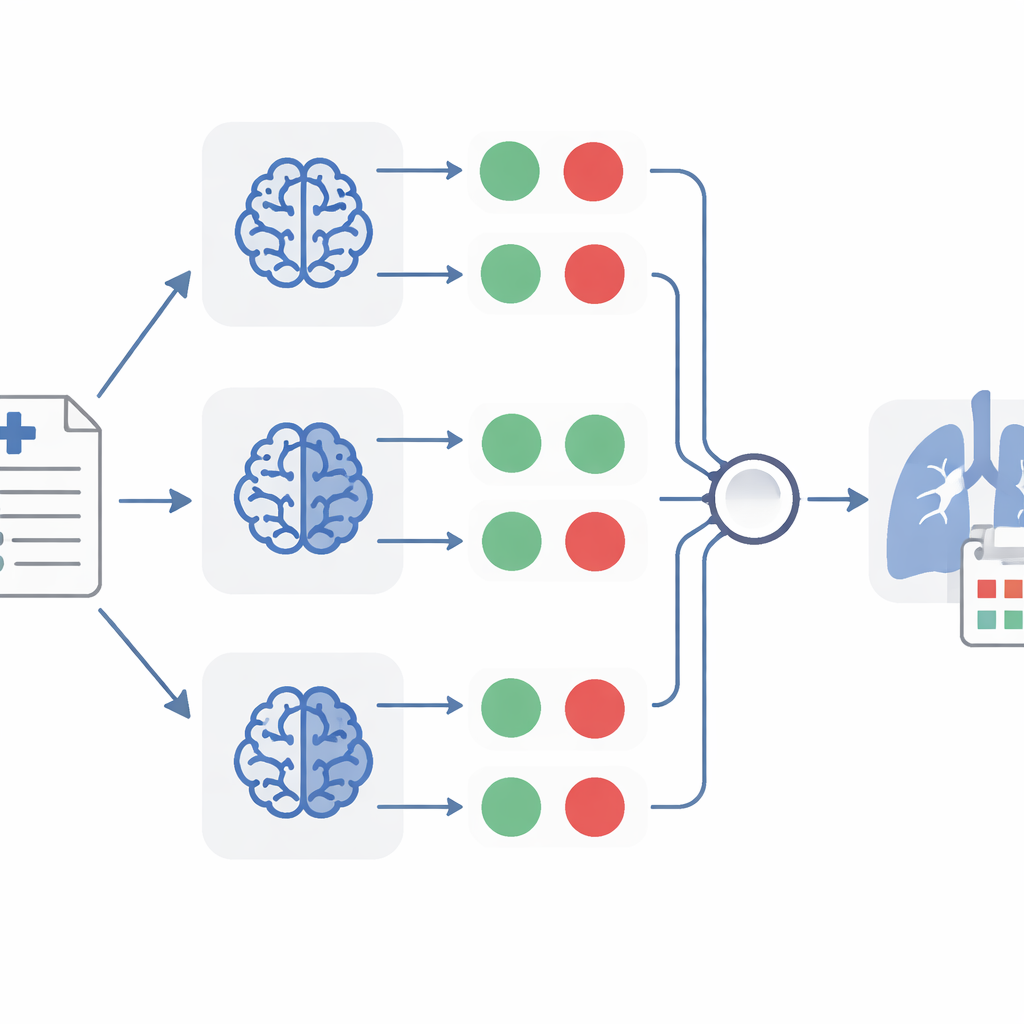
Was TheraMind in Lungenkrebsberichten fand
Angewendet auf die große Sammlung von Fallberichten markierte TheraMind 26 Berichte als starke Unterstützung für den Einsatz von zehn verschiedenen Wirkstoffen beim nicht-kleinzelligen Lungenkarzinom. Die Ensemble‑Methode erreichte eine Sensitivität (Recall) von etwa 92 Prozent, das heißt, sie erfasste nahezu alle tatsächlich relevanten Berichte, während sie eine sehr hohe Spezifität von 99,7 Prozent beibehielt, sodass nur sehr wenige irrelevante Berichte durchrutschten. Für jeden ausgewählten Bericht extrahierte das System außerdem zentrale Patientendaten — wie Alter, Geschlecht, medizinische Vorgeschichte, Zustand und das verdächtige Medikament — in ein einheitliches Datenformat und erzeugte eine kurze, verständliche Zusammenfassung des Falls. Menschliche Gutachter mit Hintergründen in Biologie und Informatik prüften diese Ausgaben und bestätigten, dass insbesondere eines der Modelle sehr genaue und vollständige Extraktionen lieferte.
Über Lungenkrebs hinaus und auf dem Weg in die Klinik
Um die Flexibilität des Systems zu testen, richtete das Team TheraMind auch auf Brustkrebs und mehrere Wirkstoffkandidaten, die zuvor in ihrer eigenen Forschung identifiziert worden waren. In diesem Setting meldete das System keine passenden Fallberichte und spiegelte damit akkurat den aktuellen wissenschaftlichen Stand wider, anstatt Evidenz zu erfinden. Die Autorinnen und Autoren argumentieren, dass eine solche strukturierte, transparente Pipeline — die regelbasierte Logik mit mehreren KI‑Lesern kombiniert — helfen kann, die Lücke zwischen Laborbefunden und für klinische Studien geeigneten Therapien zu schließen. Sie heben sowohl das Potenzial hervor, ähnliche Methoden auf andere Krebsarten anzuwenden, als auch die Notwendigkeit, den Datenschutz der Patientinnen und Patienten sorgfältig zu wahren, falls zukünftige Versionen direkt mit elektronischen Gesundheitsakten verknüpft werden.
Was das für zukünftige Behandlungen bedeutet
Einfach gesagt verwandelt TheraMind verstreute, unstrukturierte Patientenberichte in organisierte Evidenz, auf die Ärztinnen, Ärzte und Forschende reagieren können. Indem es schnell Berichte sichtbar macht, in denen bestehende Medikamente scheinbar Menschen mit Lungenkrebs geholfen haben, kann es lenken, welche repurposeten Arzneimittel eine nähere Untersuchung in klinischen Studien verdienen. Zwar ersetzt das System nicht die medizinische Urteilskraft, doch dieser multi‑modelle KI‑Leser bietet eine Möglichkeit, Berge medizinischer Texte zu sichten und eine kurze, verlässliche Liste vielversprechender Optionen für Patientinnen und Patienten zu liefern, die dringend neue Wahlmöglichkeiten brauchen.
Zitation: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Schlüsselwörter: Drug Repurposing, Lungenkrebs, Fallberichte, große Sprachmodelle, klinische Evidenzgewinnung