Clear Sky Science · de
Einzelnuklei und räumliche Profilierung von sakrokokzygealen Teratomen enthüllen die zelluläre Zusammensetzung und Heterogenität der X‑Inaktivierung
Warum Tumoren an der Wirbelsäule von Babys wichtig sind
Sakrokokzygeale Teratome sind seltene Tumoren, die an der Basis der Wirbelsäule eines Babys wachsen, manchmal bereits vor der Geburt. Sie können viele verschiedene Gewebe enthalten – Nervengewebe, Darm, Haut, Muskel – alle gemischt in einem Tumor. Ärzte können sie meist entfernen, doch manche wachsen gefährlich schnell, und sie treten bei Babys mit zwei X‑Chromosomen etwa dreimal so häufig auf wie bei denen mit nur einem. Diese Studie verwendet moderne genetische Werkzeuge, um eine detaillierte „zelluläre Landkarte" dieser Tumoren zu erstellen und zu untersuchen, ob ungewöhnliches Verhalten des X‑Chromosoms dazu beitragen könnte zu erklären, wie die Tumoren entstehen und warum sie so stark bei weiblichen Babys gehäuft auftreten.
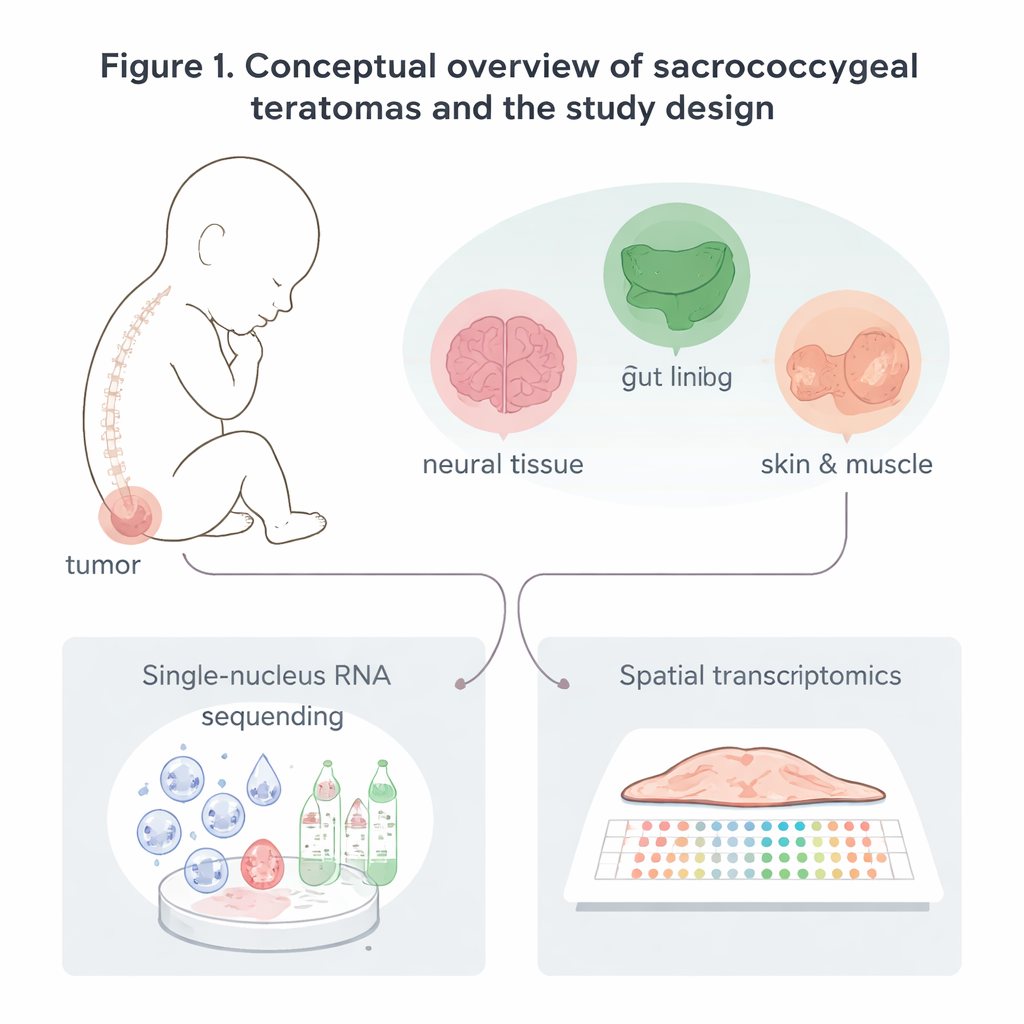
Erstellung einer detaillierten Karte der Tumorzellen
Die Forschenden sammelten acht sakrokokzygeale Teratome: sechs, die nach der Geburt entfernt wurden, und zwei, die vor der Geburt bei Hochrisikoschwangerschaften entfernt wurden. Statt die Tumoren nur unter dem Mikroskop zu betrachten, bestimmten sie, welche Gene in zehntausenden einzelner Zellkerne aktiv waren. Zusätzlich nutzten sie räumliche Transkriptomik, ein Verfahren, das Genaktivität in dünnen Gewebeschnitten misst und dabei erhält, woher jedes Signal im Tumor stammt. Aus diesen Daten identifizierten sie fünf große Zellfamilien: nervenbezogene Zellen, Epithelzellen (Auskleidung), unterstützende (stromale) Zellen wie Muskel und Knorpel, Gefäßzellen und Immunzellen wie Makrophagen und T‑Zellen. Jede dieser Familien enthielt mehrere Subtypen, was zeigt, dass diese Tumoren Mosaike vieler erkennbarer, körperähnlicher Gewebe sind und keine einheitliche Masse.
Verschiedene Tumoren, verschiedene Gewebemischungen
Obwohl jeder Tumor Zellen enthielt, die den drei großen embryonalen Keimblättern ähneln, variierten ihre Mischungen stark. Indem das Team alle Zellen eines Tumors als gemeinsame „Stimme" behandelte, verglichen sie die Gesamtausdrucksmuster der Gene und fanden drei breite Tumorgruppen. Eine Gruppe war reich an Epithelzellen, die stark ein Gen ausdrückten, das oft mit frühen embryonalen Zuständen verknüpft ist (POU5F1); eine andere Gruppe hatte weniger Epithelzellen, dafür mehr Blutgefäße und knorpelähnliches Gewebe; und eine dritte Gruppe kombinierte Epithel‑ und nervenbezogene Zellen. Diese Unterschiede korrelierten mit Genprogrammen, die mit Entzündung, Gefäßneubildung und Nervensystementwicklung zu tun haben. In schnell wachsenden Tumoren, die vor der Geburt entfernt wurden, zeigte die räumliche Kartierung, dass stromale und nervenähnliche Zellen große Bereiche dominierten, mit Clustern aktiv teilender Zellen verteilt, was nahelegt, dass diese schnell wachsenden Tumoren von Nischen sich teilender Stütz‑ und nervenbezogener Zellen angetrieben werden.
Die Idee einer verborgenen Stammzelle infrage stellen
Weil Teratome so verschiedene Gewebe enthalten, vermuteten viele Wissenschaftler, sie entstünden aus einer seltenen, mächtigen, stammzellähnlichen Zelle, ähnlich den frühen Vorläufern von Eizellen und Spermien. Das Team suchte gezielt nach Zellen, die gleichzeitig typische Gene pluripotenter Stammzellen und primordialer Keimzellen einschalten. Sie fanden verstreute Expression einiger dieser Gene, jedoch nie in einer Weise, die eine klare, einheitliche „Master“-Zellpopulation markierte. Stattdessen tauchten keimzell‑ und pluripotenzbezogene Gene in normalen Tumorzelltypen auf, etwa in Immunzellen oder bestimmten Epithelzellen. Das legt nahe, dass in zumindest den hier untersuchten Tumoren ein ursprünglicher stammzellähnlicher Gründer entweder verschwunden ist oder nur schwache Spuren in ausgereifteren Zellpopulationen hinterlassen hat.
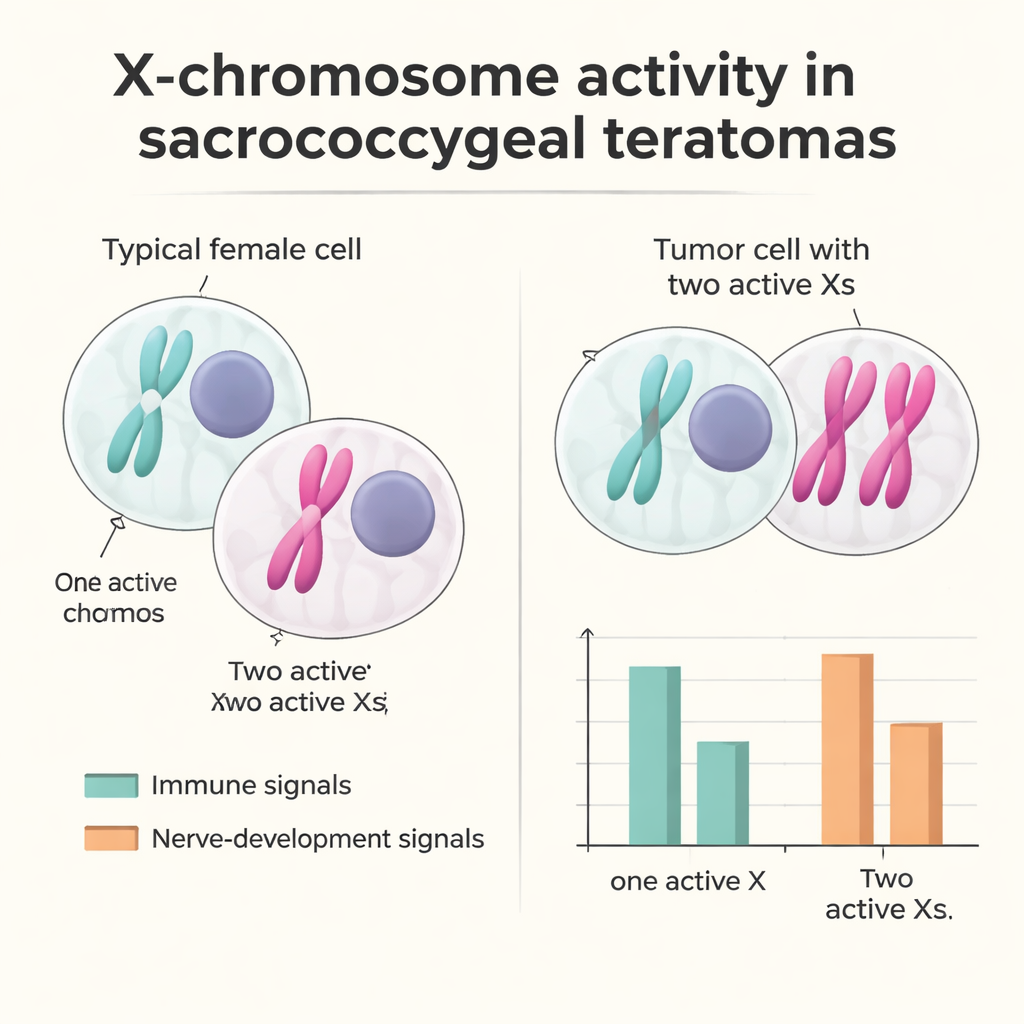
Zwei aktive X‑Chromosomen und eine abgeschwächte Immunantwort
Um zu untersuchen, warum diese Tumoren bei Babys mit zwei X‑Chromosomen deutlich häufiger sind, untersuchten die Forschenden, wie das X‑Chromosom in Tumorzellen reguliert wird. In typischen weiblichen Zellen wird ein X abgeschaltet, um die Genkopienzahl gegenüber Männern auszugleichen; diese Inaktivierung ist durch ein Molekül namens XIST gekennzeichnet. In einem weiblichen Tumor entdeckten sie eine erhebliche Gruppe von Zellen, die XIST nicht exprimierten und Genexpressionsmuster zeigten, die mit zwei aktiven X‑Chromosomen vereinbar sind. Diese „XaXa‑ähnlichen" Zellen traten am häufigsten in Epithel‑, nervenbezogenen und stromalen Populationen auf. Durch Verfolgung natürlicher genetischer Varianten zeigte das Team, dass viele X‑verknüpfte Gene, die auf dem inaktiven X still sein sollten, nun von beiden Kopien aktiv waren, was auf ein Versagen des üblichen Inaktivierungssystems hindeutet und nicht bloß auf eine Verdopplung eines bereits aktiven X. Zellen mit zwei aktiven X‑Chromosomen tendierten dazu, mehr Gene zu exprimieren, die an früher Entwicklung und Nervenausbildung beteiligt sind, während Zellen mit einem normalen einzigen aktiven X stärkere Immun‑ und Entzündungssignale zeigten. Das deutet darauf hin, dass Veränderungen der X‑Dosierung das Tumorumfeld subtil weg von einer Immunantwort kippen könnten.
Was das für Patientinnen, Patienten und Familien bedeutet
Für Familien mit der Diagnose sakrokokzygeales Teratom ändert diese Arbeit den Alltag in der Behandlung noch nicht: Die Versorgung beruht weiterhin auf Operation und sorgfältiger Nachsorge. Sie liefert jedoch ein klareres Bild davon, woraus diese Tumoren bestehen, und weist auf neue Erklärungsansätze dafür hin, warum sie entstehen und warum sie bei Babys mit zwei X‑Chromosomen häufiger sind. Die Studie zeigt, dass sich Tumoren nach den Gewebearten und Genprogrammen gruppieren lassen, die sie enthalten, und dass in mindestens einem Fall Zellen mit zwei aktiven X‑Chromosomen Entwicklungsvorteile gewinnen und gleichzeitig Immun‑Signale abschwächen. Solche detaillierten zellulären Karten könnten künftig helfen, besser vorherzusagen, welche Tumoren aggressiv wachsen, Tests zu inspirieren, die gefährliche Zellpopulationen überwachen, und die Forschung zu Therapien zu leiten, die das normale Gleichgewicht des X‑Chromosoms wiederherstellen oder die Anti‑Tumor‑Immunität stärken.
Zitation: Rojas, E.J., Giannikou, K., Huang, B.J. et al. Single nuclei and spatial profiling of sacrococcygeal teratomas reveals cellular composition and X inactivation heterogeneity. npj Precis. Onc. 10, 87 (2026). https://doi.org/10.1038/s41698-025-01262-4
Schlüsselwörter: sakrokokzygeales Teratom, Einzelzellsequenzierung, räumliche Transkriptomik, X‑Chromosomeninaktivierung, fetale Tumoren