Clear Sky Science · de
Neoadjuvantes Sintilimab, albumingebundenes Paclitaxel und Carboplatin bei lokal fortgeschrittenem, resektablem Plattenepithelkarzinom der Speiseröhre: klinische Studie und mechanistische Untersuchung
Den Wandel gegen einen tödlichen Rachenkrebs einleiten
Speiseröhrenkrebs zählt zu den tödlichsten Krebserkrankungen weltweit und wird häufig erst entdeckt, wenn er bereits tief in den Brustkorb vorgedrungen ist. Viele Patientinnen und Patienten kommen noch für eine Operation in Frage, doch selbst mit den besten Chemotherapie‑ und Strahlentherapie‑Protokollen bleibt das Rückfallrisiko hoch. Diese Studie prüft eine neue Strategie, die die körpereigene Abwehr vor der Operation stärkt, und untersucht mikroskopisch, wie sich Tumoren und ihr Umfeld daraufhin verändern. Die Ergebnisse deuten auf wirksamere Behandlungsansätze und einen Weg zu wirklich personalisierter Versorgung hin.
Ein neuer Drei‑Medikamenten‑Plan vor der Operation
Die Forschenden rekrutierten 24 Personen in China mit einer häufigen und aggressiven Form des Speiseröhrenkrebses, dem Plattenepithelkarzinom. Alle hatten Tumoren, die fortgeschritten, aber noch operativ entfernbar waren. Vor dem Eingriff erhielt jede Patientin/jeder Patient drei Zyklen einer Kombinationsbehandlung: Sintilimab, ein immunaktivierender Antikörper, der T‑Zellen hilft, Krebs zu erkennen; dazu zwei Standard‑Chemotherapeutika, albumingebundenes Paclitaxel und Carboplatin. Nach dieser neoadjuvanten Phase unterzogen sich die Patienten einer Operation zur Entfernung des Speiseröhrentumors, und die meisten setzten anschließend Sintilimab fort.
Stärkeres Tumor‑Schrumpfen und ermutigende Überlebensdaten
Bei der Untersuchung der entfernten Tumoren durch Chirurgen und Pathologen zeigte sich, dass das präoperative Regime bei vielen Patientinnen und Patienten zu einer deutlichen Verkleinerung geführt hatte. Etwa 42 % zeigten eine sogenannte major pathologische Response, das heißt, nur ein kleiner Bruchteil lebensfähiger Tumorzellen blieb übrig. Bei einem von drei Patienten waren im Haupttumorbereich überhaupt keine nachweisbaren Krebszellen mehr vorhanden. Auch in Bildgebung und klinischer Nachbeobachtung waren die Ergebnisse vielversprechend: drei Jahre nach der Behandlung waren etwa drei von vier Patienten ohne Anzeichen eines Rückfalls am Leben, und nahezu vier von fünf noch am Leben insgesamt. Wichtig ist, dass die Nebenwirkungen dieses intensivierten Plans beherrschbar waren, es keine behandlungsbedingten Todesfälle gab und die chirurgische Entfernung sicher und durchführbar blieb.
Wie die Nachbarschaft des Tumors die Antwort prägt
Nicht alle Patienten profitierten gleichermaßen, daher suchte das Team nach Erklärungen. Im Fokus stand das tumoröse Mikroumfeld — die komplexe Nachbarschaft aus Krebszellen, Immunzellen und Signalstoffen. Mittels gezielter Proteinmessungen an sorgfältig präparierten Tumorproben verglichen sie gute Responder mit Nicht‑Respondern. Vor der Behandlung fanden sie 14 Proteine, die zwischen den Gruppen unterschiedlich ausgeprägt waren. Ein Oberflächenprotein, CD44, fiel besonders auf: Tumoren mit höheren CD44‑Werten sprachen tendenziell besser auf die sintilimabbasierte Therapie an. Nach der Behandlung waren bei den Respondern viele Proteine, die an Immunaktivität und DNA‑Reparatur beteiligt sind, vermindert — ein Hinweis darauf, dass die Kombinationstherapie die Unterstützungsmechanismen des Tumors erfolgreich gestört und die lokale Immunlandschaft umgestaltet hat.
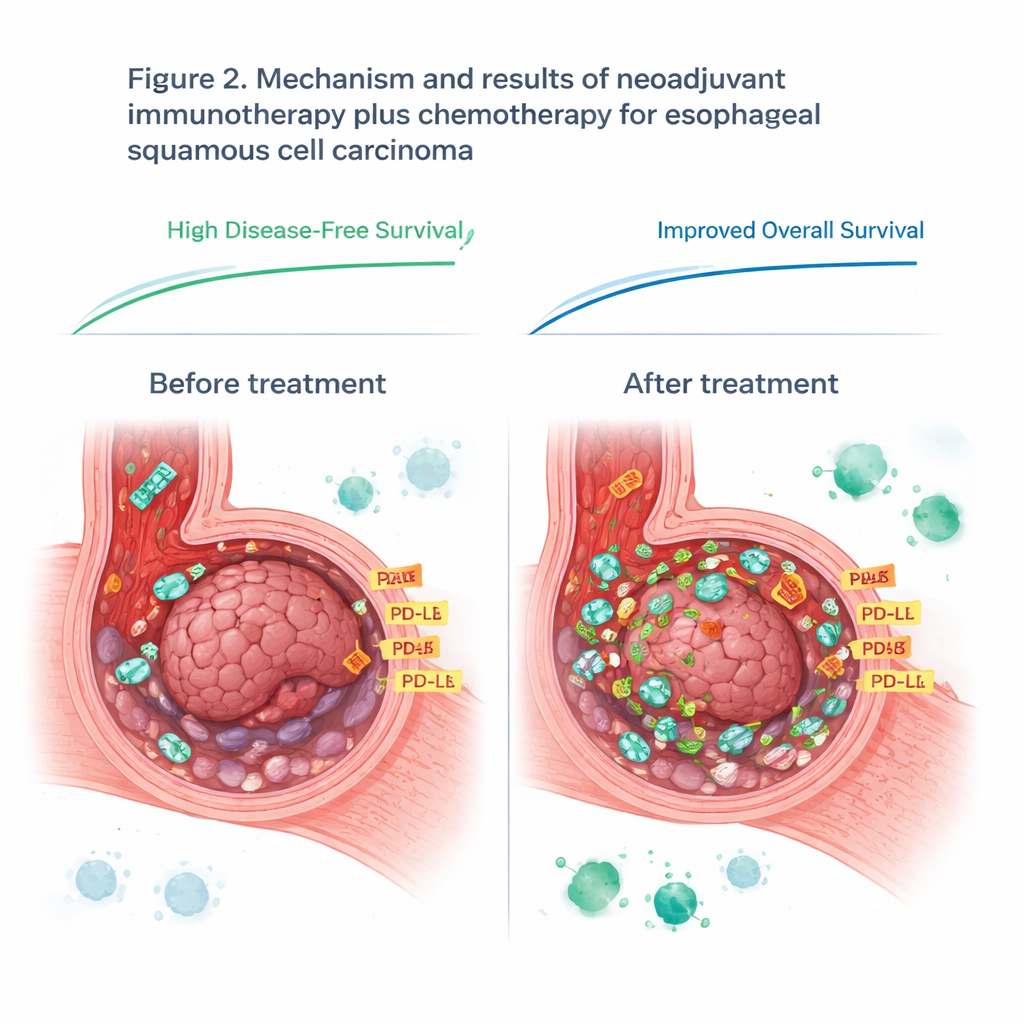
Ein Umdenken bei einem verbreiteten Immunmarker
Die Studie betrachtete außerdem PD‑L1, ein Protein, das oft als Orientierungsgröße dafür dient, wer von Immun-Checkpoint‑Medikamenten profitieren könnte. Vor der Behandlung sagten PD‑L1‑Werte auf den Tumorproben nicht voraus, wer gut ansprechen würde, was die derzeitige Praxis bei dieser Krebsart infrage stellt. Während der Behandlung stieg PD‑L1 jedoch bei allen Patientinnen und Patienten an, wahrscheinlich weil das aktivierte Immunsystem den Tumor mit Entzündungssignalen flutete. Nach der Therapie waren höhere PD‑L1‑Werte im verbliebenen Tumorgewebe enger mit dem Ansprechen auf die Immuntherapie verknüpft. Das legt nahe, dass das Timing eine Rolle spielt: Eine einzelne Messung von PD‑L1 vor der Behandlung kann entscheidende Veränderungen übersehen, die erst eintreten, wenn das Immunsystem in Aktion tritt.
Was das für Patienten und die Zukunft bedeutet
Für Menschen, die sich einer Operation wegen fortgeschrittenem Speiseröhrenkrebs gegenübersehen, enthält diese Studie zwei hoffnungsvolle Botschaften. Erstens scheint die Kombination von Sintilimab mit Chemotherapie vor der Operation Tumoren stärker zu verkleinern und möglicherweise die Chancen auf ein langfristiges Überleben zu erhöhen, ohne gefährliche Nebenwirkungen hinzuzufügen. Zweitens zeigt die Arbeit, dass Tumor und sein Mikroumfeld nicht statisch sind; sie werden durch die Behandlung in verfolg- und messbarem Maße umgestaltet, etwa durch Proteine wie PD‑L1 und CD44. Solche molekularen Fingerabdrücke könnten in Zukunft Ärzten helfen, Therapien in Echtzeit besser auszuwählen und anzupassen — und so mehr „kalte“ Tumoren, die das Immunsystem ignorieren, in „heiße“ Tumoren zu verwandeln, die eine starke, anhaltende Immunantwort zulassen.
Zitation: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Schlüsselwörter: Speiseröhrenkrebs, Immuntherapie, neoadjuvante Therapie, PD‑1‑Inhibitoren, tumoröses Mikroumfeld