Clear Sky Science · de
Algorithmusgestützte individualisierte Therapieplanung verbessert Überleben in einem Mausmodell des triple-negativen Brustkrebses
Warum klügere Chemotherapie wichtig ist
Chemotherapie rettet Leben, wird aber häufig noch nach dem Prinzip „One-Size-Fits-All“ verabreicht: Personen mit ähnlichen Tumoren erhalten oft dieselbe Wirkstoffdosis zum gleichen Zeitplan. Das kann für einige Patientinnen und Patienten starke Nebenwirkungen bedeuten und für andere unzureichenden Nutzen. Die hier beschriebene Studie stellt eine einfache, aber wirkungsvolle Frage: Was wäre, wenn wir Computeralgorithmen verwenden könnten, um die Chemotherapie in Echtzeit individuell anzupassen, ähnlich wie ein Thermostat die Heizung eines Hauses reguliert? Anhand eines fortgeschrittenen Mausmodells eines aggressiven Brustkrebses zeigen die Forschenden, dass solch maßgeschneiderte Dosierungen das Überleben verlängern und die Entwicklung von Arzneimittelresistenzen begrenzen können.
Das Problem mit routinemäßigen Krebsmedikamentenplänen
Heute erhalten viele Patientinnen und Patienten die höchste Dosis, die sie vertragen, in festen Intervallen. Dieses sogenannte Maximum-Tolerated-Dose-Protokoll berücksichtigt nicht, wie schnell ein bestimmter Tumor wächst, wie der Körper einer Patientin oder eines Patienten das Medikament verarbeitet oder wie der Tumor sich im Zeitverlauf verändert. Infolgedessen können Tumoren anfangs zurückgehen, später aber als stärker resistente Varianten wiederkehren, während die Betroffenen unter erheblichen Nebenwirkungen leiden. Frühere Versuche, dies zu verbessern, etwa die „metronomische“ Chemotherapie mit kleineren, häufigeren Dosen, lieferten in klinischen Studien gemischte Ergebnisse und haben nicht eindeutig gezeigt, wie Dosis und Zeitplan am besten gewählt werden sollten. Es besteht ein klarer Bedarf an einer rationaleren, individualisierten Art der Chemotherapieplanung.
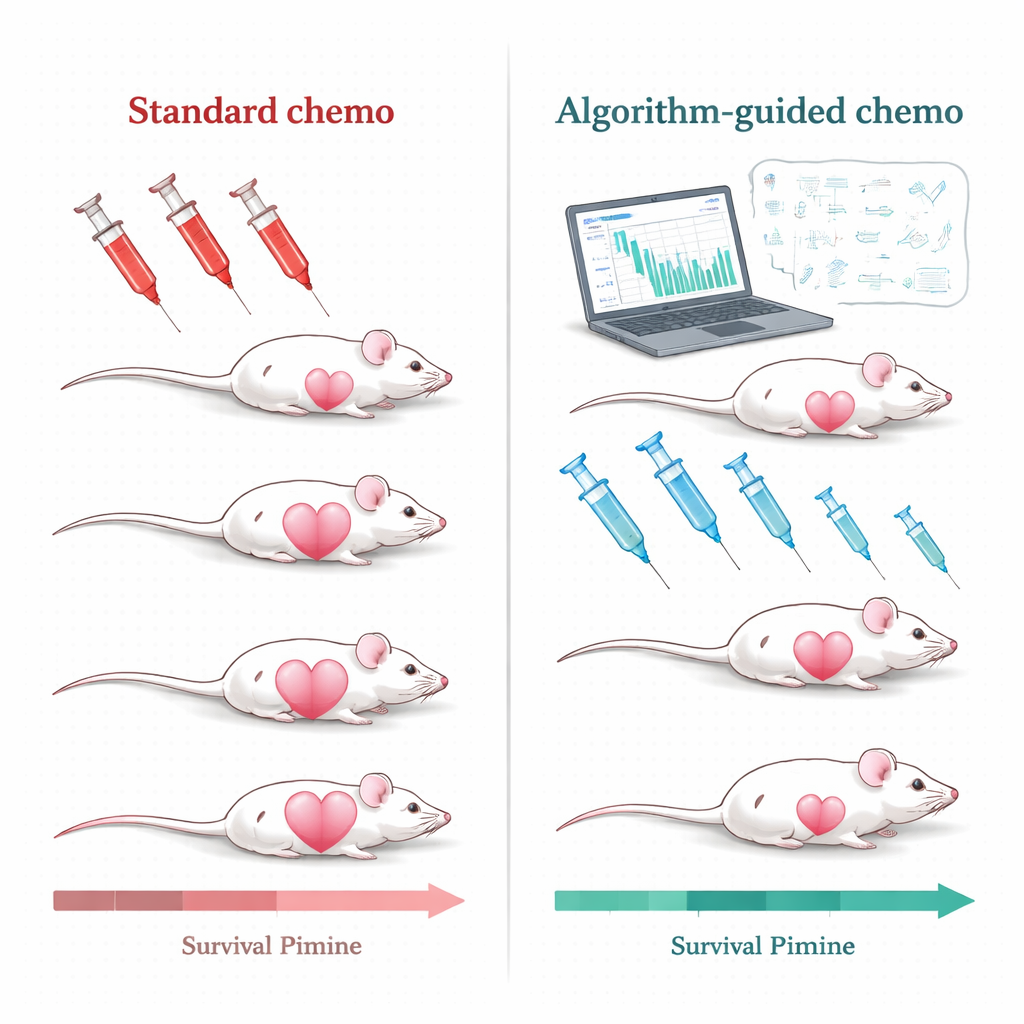
Algorithmen zur Therapieanpassung nutzen
Das Forschungsteam ging diese Herausforderung bei Mäusen mit triple-negativen Brusttumoren an, einer Form von Brustkrebs, die beim Menschen besonders schwer zu behandeln ist und noch weitgehend auf Chemotherapie angewiesen ist. Die Mäuse wurden mit einer häufig verwendeten Wirkstoffformulierung, pegyliertem liposomalem Doxorubicin, behandelt. Statt wiederholt hoch dosierte Behandlungen nur dann zu geben, wenn Tumoren zu einer bestimmten Größe nachwuchsen, entwickelten die Wissenschaftlerinnen und Wissenschaftler mathematische Modelle, die beschreiben, wie der Tumor wächst, unter Behandlung zurückgeht und wie sich das Medikament im Blut verteilt. Diese Modelle wurden mit einfachen, klinisch realistischen Messwerten gespeist: wiederholten Tumorgrößenmessungen und Blutspiegeln des Medikaments. Aus diesen Eingaben erzeugte ein Computeralgorithmus personalisierte Behandlungspläne für jede Maus.
Zwei Wege, wie der Computer helfen kann
Die Studie testete zwei Varianten der algorithmusgestützten Therapieplanung. In einem Ansatz, PDPK genannt, verwendete der Computer frühe Daten, um einen 30-tägigen Plan mit relativ kleinen, wiederholten Dosen zu entwerfen, der darauf abzielte, den Wirkstoffspiegel im Blut gleichmäßig, aber niedrig zu halten — hoch genug, um den Tumor zu kontrollieren, aber niedrig genug, um die Toxizität zu begrenzen. Im zweiten Ansatz, Model Predictive Control genannt, aktualisierte der Algorithmus den Plan täglich auf Basis der neuesten Tumormessung und passte die Dosisgrößen an, um den Tumor stetig nach unten zu drücken. Beide Methoden beruhen auf derselben Grundidee: Einen realistischen „digitalen Zwilling“ der tumorgefährdeten Maus zu verwenden, um viele mögliche Dosierungsmuster im Voraus zu simulieren und diejenigen auszuwählen, die unter Sicherheitsbedingungen am ehesten am besten funktionieren.
Längeres Überleben und weniger Arzneimittelresistenz
Im Vergleich mit dem standardmäßigen hochdosierten, tumorgetriggerten Protokoll waren die Unterschiede deutlich. Unter der konventionellen Therapie schrumpften Tumoren häufig zunächst stark, traten aber schließlich wieder auf, und wiederholte hohe Dosen begünstigten das Entstehen resistenter Erkrankungen. Dagegen hielten die meisten algorithmisch entworfenen Behandlungen die Tumoren deutlich besser unter Kontrolle, verlängerten die Zeit bis zum Rückfall und verhinderten in vielen Fällen während des Studienzeitraums klare Anzeichen von Resistenz. Über Dutzende von Mäusen hinweg lebten sowohl die PDPK- als auch die Model-Predictive-Control-Gruppen deutlich länger als die Tiere auf dem Standardprotokoll, wobei mehrere algorithmusbasierten Strategien starke, statistisch signifikante Überlebensvorteile zeigten.
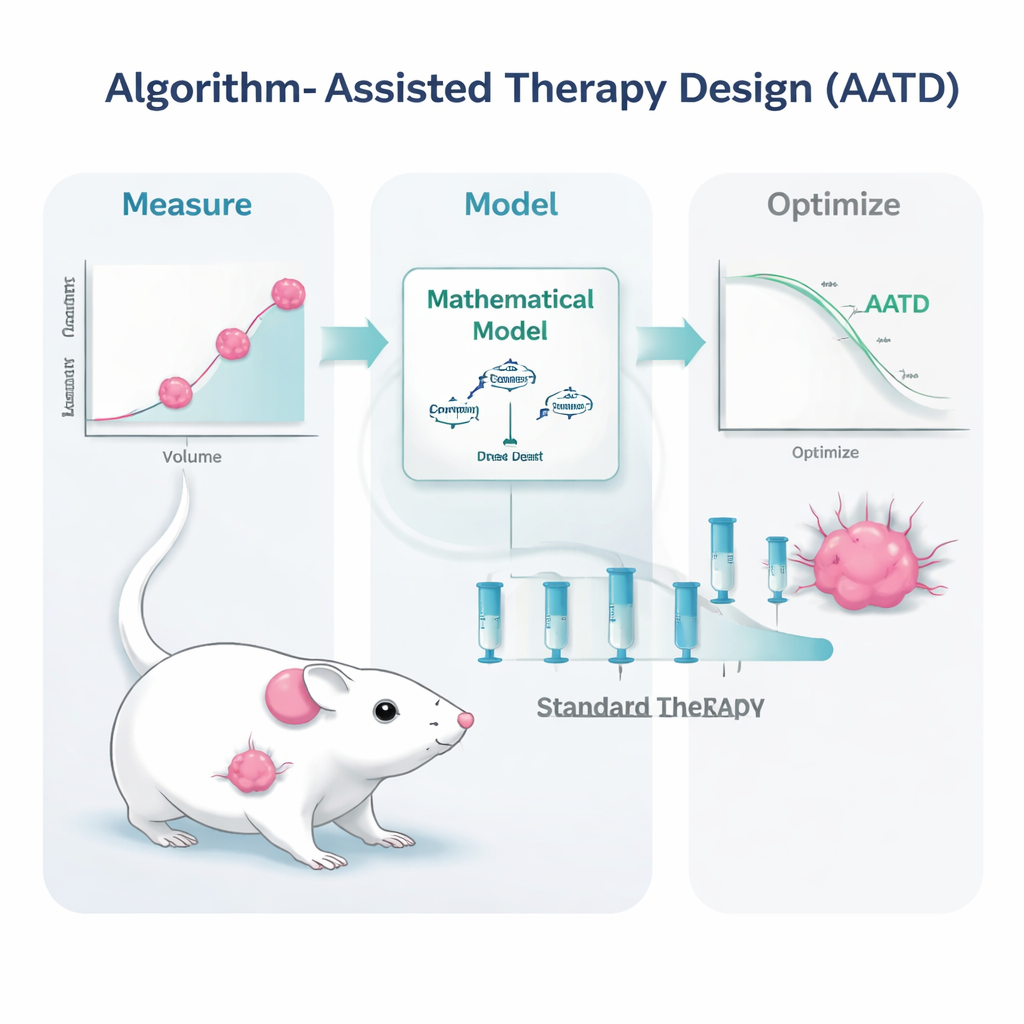
Was das für zukünftige Patientinnen und Patienten bedeuten könnte
Obwohl diese Arbeit an Mäusen durchgeführt wurde, sind ihre zentralen Bestandteile — Messung der Tumorgröße, Überwachung der Wirkstoffspiegel im Blut und Einsatz von Computermodellen — bei Menschengere bereits mit modernen Bildgebungs- und Labormethoden möglich. Die Studie legt nahe, dass Ärzten eines Tages statt der Frage „Was ist die Standarddosis?“ eher die Frage gestellt werden könnte: „Angesichts des individuellen Tumorverhaltens und der Medikamentenverarbeitung dieser Patientin / dieses Patienten, welche Dosis und welches Timing sind gerade jetzt am besten?“ Praktische Hürden bleiben, etwa der Bedarf an häufigeren Messungen und die Logistik flexibler Dosierung, doch die Botschaft ist klar: Chemotherapie muss nicht grob und einheitlich sein. Mit Hilfe von Algorithmen kann sie zu einem präziseren, anpassungsfähigeren Instrument werden, das Patientinnen und Patienten bessere Chancen auf eine langfristige Kontrolle aggressiver Krebserkrankungen bietet.
Zitation: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
Schlüsselwörter: personalisiert, triple-negativer Brustkrebs, algorithmusgestützte Therapie, mathematische Tumormodellierung, Doxorubicin-Dosierung