Clear Sky Science · de
Räumliche Transkriptomik enthüllt molekulare Heterogenität und subtypspezifische therapeutische Targets beim kleinzelligen Lungenkrebs
Warum diese Lungenkrebsstudie wichtig ist
Kleinzelliger Lungenkrebs zählt zu den tödlichsten Krebsformen, betrifft überwiegend Menschen mit Raucherbiografie und tritt nach Chemotherapie oft rasch wieder auf. Ärztinnen und Ärzte wissen, dass kleinzellige Lungenkarzinome sich nicht alle gleich verhalten, doch es fehlten die Mittel, um zu sehen, wie verschiedene Krebszellen und Immunzellen innerhalb jedes Tumors räumlich angeordnet sind. In dieser Studie wurde eine neue Technologie eingesetzt, die die Genaktivität in tausenden kleinen Flecken auf einem Tumorschnitt liest und so eine „molekulare Landkarte“ jeder Probe erstellt. In Kombination mit maßgeschneiderter Computeranalyse entdeckten die Forschenden verborgene Muster, die auf präzisere, subtypspezifische Behandlungsansätze hinweisen könnten.
Tumoren vor Ort kartieren
Das Team analysierte Tumorproben von 21 Patientinnen und Patienten mit begrenztem Stadium kleinzelligen Lungenkrebs, die operiert wurden, bevor sie Medikamente erhielten. Statt das Gewebe zu zerkleinern und damit räumliche Informationen zu verlieren, nutzten sie räumliche Transkriptomik: ein Verfahren, das misst, welche Gene an vielen genau definierten Stellen eines Gewebes aktiv sind. Jeder Messpunkt behält seine Originalposition bei, sodass die Wissenschaftler Genaktivität mit der physischen Lage von Krebszellen, normalen Zellen und Immunzellen verknüpfen konnten. Darauf setzten sie zwei zentrale Werkzeuge: einen neuen „Edgeindex“-Score, um zu quantifizieren, wie stark Tumorzellen ins umliegende Gewebe eindringen, und ein künstliches neuronales Netzwerk—eine Form des maschinellen Lernens—um automatisch zu kennzeichnen, welche Punkte Tumor und welche nicht sind.
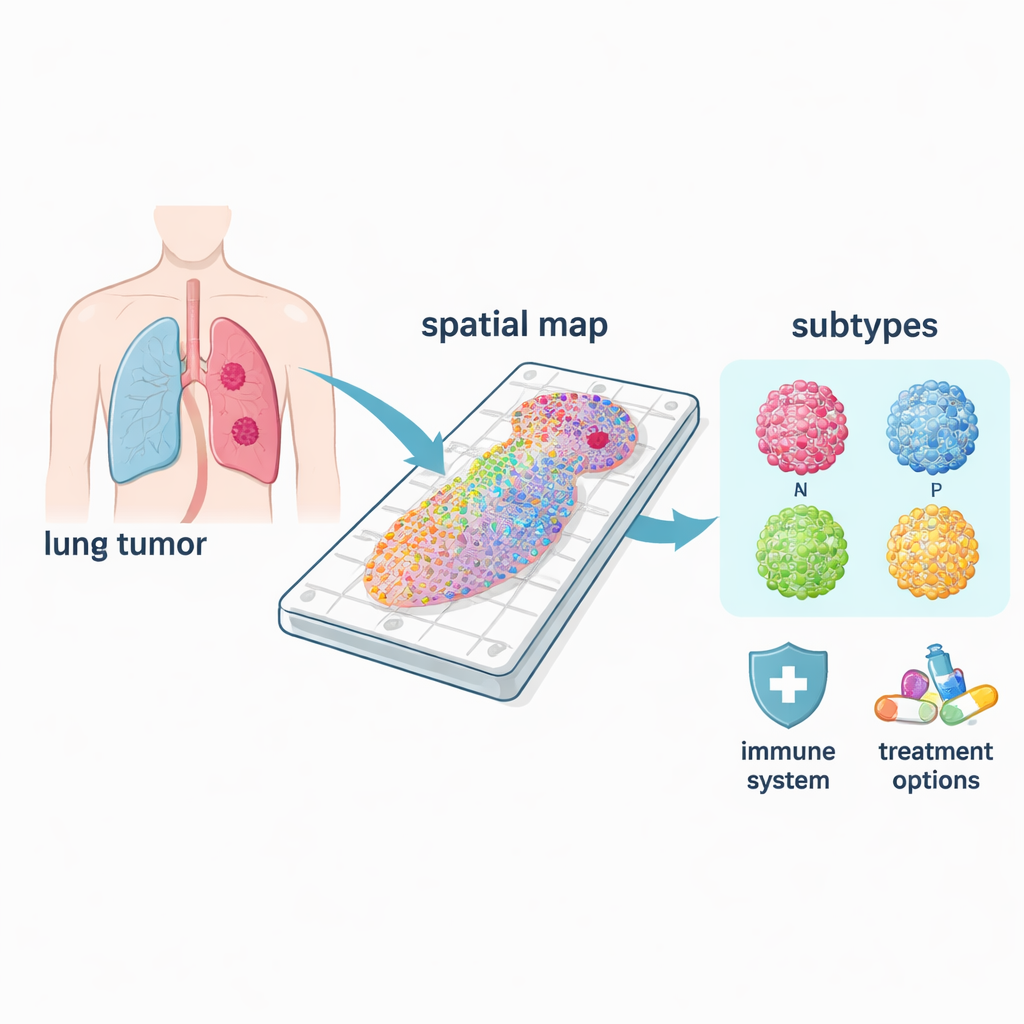
Verschiedene Krebsarten in einer Erkrankung
Kleinzelliger Lungenkrebs ist keine einheitliche Krankheit, sondern umfasst mindestens vier wichtige molekulare Subtypen, meist bezeichnet nach zentralen Kontrollgenen: ASCL1, NEUROD1, POU2F3 und YAP1. Mit ihren räumlichen Karten konnten die Forschenden sehen, wo jeder Subtyp innerhalb der Tumoren dominierte und wie sich ihre Biologie unterschied. Die häufigen ASCL1- und NEUROD1-Formen standen stark mit Zellteilungsprogrammen in Verbindung, was ihrem Ruf als hochproliferative Formen entspricht. Dagegen waren POU2F3-Regionen an Immunwege gebunden, während YAP1-Bereiche Signale für Stoffwechsel und Gewebeumbau zeigten—Merkmale, die mit Ausbreitung und Therapieresistenz zusammenhängen könnten. Weil diese Muster räumlich aufgelöst sind, kann die Methode den eigentlichen „treibenden“ Subtyp in einem gemischten Tumor identifizieren, was bei Bulk-Tests oft übersehen wird.
Die invasive Randzone und der Immunwandel
Eine der zentralen Neuerungen der Studie, der Edgeindex, erfasst, wie stark Tumorzellen mit dem umgebenden Nicht-Tumorgewebe durchmischt sind. Niedrige Werte stehen für kompakte, gut begrenzte Tumoren, hohe Werte für verstreute Inseln und zerklüftete, invasive Ränder. Tumoren mit hohem Edgeindex zeigten eine Anreicherung für Genprogramme in Verbindung mit extrazellulärer Matrix, Metastasen und Zelltod. Sie wiesen zudem eine auffällig veränderte Immunlandschaft auf: weniger Helfer-T-Zellen und andere adaptive Immunakteure, dagegen mehr angeborene Zellen wie bestimmte natürliche Killerzellen und Monozyten. Die Autorinnen und Autoren deuten dies als „immunologisches Nischen‑Remodelling“, in dem der Tumor gezielte, präzise Immunantworten verdrängt und eine weniger effektive, vorwiegend angeborene Abwehr hinterlässt, die den Krebs nicht vollständig kontrollieren kann.
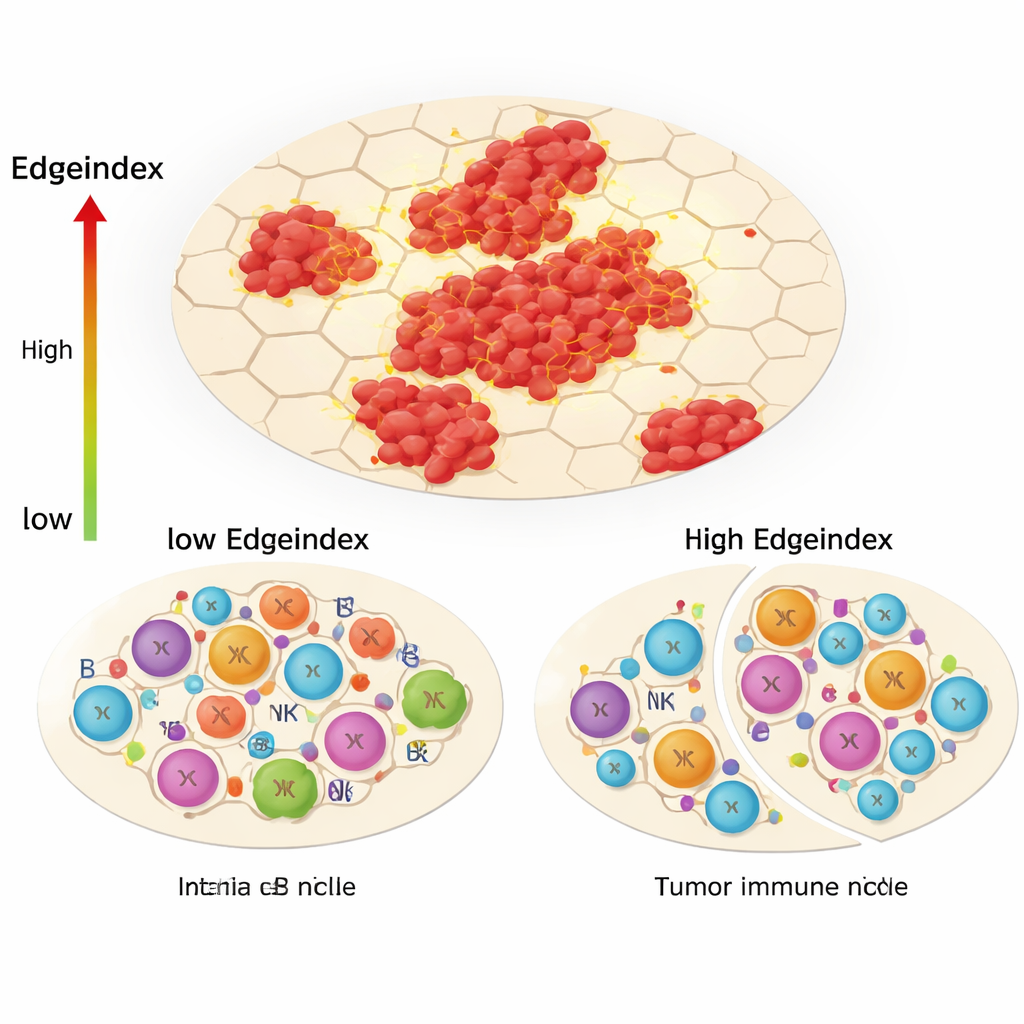
Verborgene Vielfalt in und um Tumoren
Über Subtyp- und Invasionsmuster hinaus zeigte die räumliche Datengrundlage, dass sowohl die Krebszellpopulationen als auch ihre umliegenden Mikroumgebungen intern vielfältig sind. Durch Clusterbildung der Messpunkte innerhalb jedes Tumors zählte das Team, wie viele unterschiedliche Genexpressions‑„Nachbarschaften“ in den Tumorregionen und im angrenzenden Nicht‑Tumorgewebe existierten. Eine höhere Diversität innerhalb des Tumors war mit immunbezogenen Wegen verknüpft, während bestimmte Muster im umgebenden Gewebe auf Zellzyklusaktivität und genetische Regulation hinwiesen. Die Forschenden untersuchten außerdem, wie stark verschiedene Regionen über bekannte Signalstoffe „kommunizieren“. Tumoren mit intensiverer Kommunikation zwischen Regionen zeigten tendenziell stärkere immunbezogene Signale, was die Vorstellung untermauert, dass Immunaktivität und Tumorwachstum räumlich eng verflochten sind.
Die Tumorentwicklung im Zeitverlauf verfolgen
Um abzuschätzen, wie sich Tumorzellen im Krankheitsverlauf verändern, führte das Team eine „Pseudotime“-Analyse durch, die Zellen entlang eines Entwicklungsweges basierend auf ihrer Genaktivität ordnet. In den Proben identifizierten sie wiederholt ein Gen, UCHL1, als zentrales Element dieser Verläufe. Hohe UCHL1-Spiegel fielen mit starker Zellzyklusaktivität in Tumorpunkten zusammen, während niedrigere Werte mit Immun- und Zelltodwegen assoziiert waren. Da UCHL1 ein neuralartiges Protein ist, das zuvor mit aggressiven Lungenkarzinomen in Verbindung gebracht wurde, stärken diese Befunde die Annahme, dass es ein nützliches Medikamentenziel sein könnte, insbesondere für neuroendokrin-ähnliche Zellen, die den kleinzelligen Lungenkrebs vorantreiben.
Was das für Patientinnen und Patienten bedeutet
Einfach gesagt verwandelt diese Studie flache Mikroskopschnitte kleinzelligen Lungenkrebses in reichhaltige, geschichtete Karten, die zeigen, wo sich unterschiedliche Krebs‑Subtypen befinden, wie aggressiv sie einwachsen, wie sie mit ihrer Umgebung kommunizieren und wie das Immunsystem reagiert oder versagt. Der neue Edgeindex‑Score und der Kartierungsansatz heben hervor, welche Tumoren besonders infiltrativ sind und welche Immunzellen an der Grenze vorhanden oder fehlend sind. Indem diese räumlichen Muster mit subtypspezifischen Schwachstellen verknüpft werden—etwa mit Wirkstoffen, die DLL3, BCL‑2, AURKA, IGF‑1R/PARP oder Immuncheckpoints ansprechen—bringt die Arbeit das Feld näher daran, jede Patientin und jeden Patienten einer maßgeschneiderten Behandlungsstrategie zuzuordnen. Zwar müssen diese Werkzeuge noch in größeren Studien validiert werden, doch sie bieten einen Plan für präzisere und potenziell wirksamere Therapien bei einer Krebserkrankung, die dringend bessere Optionen braucht.
Zitation: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Schlüsselwörter: kleinzelliger Lungenkrebs, räumliche Transkriptomik, Tumorheterogenität, tumorales Immunmikromilieu, Präzisionsonkologie