Clear Sky Science · de
Computationale Pathologiemerkmale der Immunarchitektur sagen klinisch relevante Ergebnisse beim kleinzelligen Lungenkrebs (SCLC) voraus
Warum die Verteidiger des Körpers bei Lungenkrebs zählen
Der kleinzellige Lungenkrebs ist eine der aggressivsten Formen von Lungenkrebs: Er breitet sich oft schnell aus und kommt nach der Behandlung zurück. Ärztinnen und Ärzte können Tumoren im Mikroskop sehen, doch die feinmaschigen Muster, wie Krebszellen und Immunzellen nebeneinanderliegen, sind mit bloßem Auge zu komplex, um sie zuverlässig zu beurteilen. Diese Studie stellt eine computergestützte Methode namens PhenopyCell vor, die diese verborgenen Muster aus routinemäßigen Biopsiepräparaten liest und sie nutzt, um vorherzusagen, wie lange Patientinnen und Patienten voraussichtlich leben und wie gut sie auf eine Chemotherapie ansprechen könnten. Für Betroffene und ihre Familien könnten solche Einblicke eines Tages helfen, die Behandlung zu individualisieren statt auf ein Einheitskonzept zu setzen.
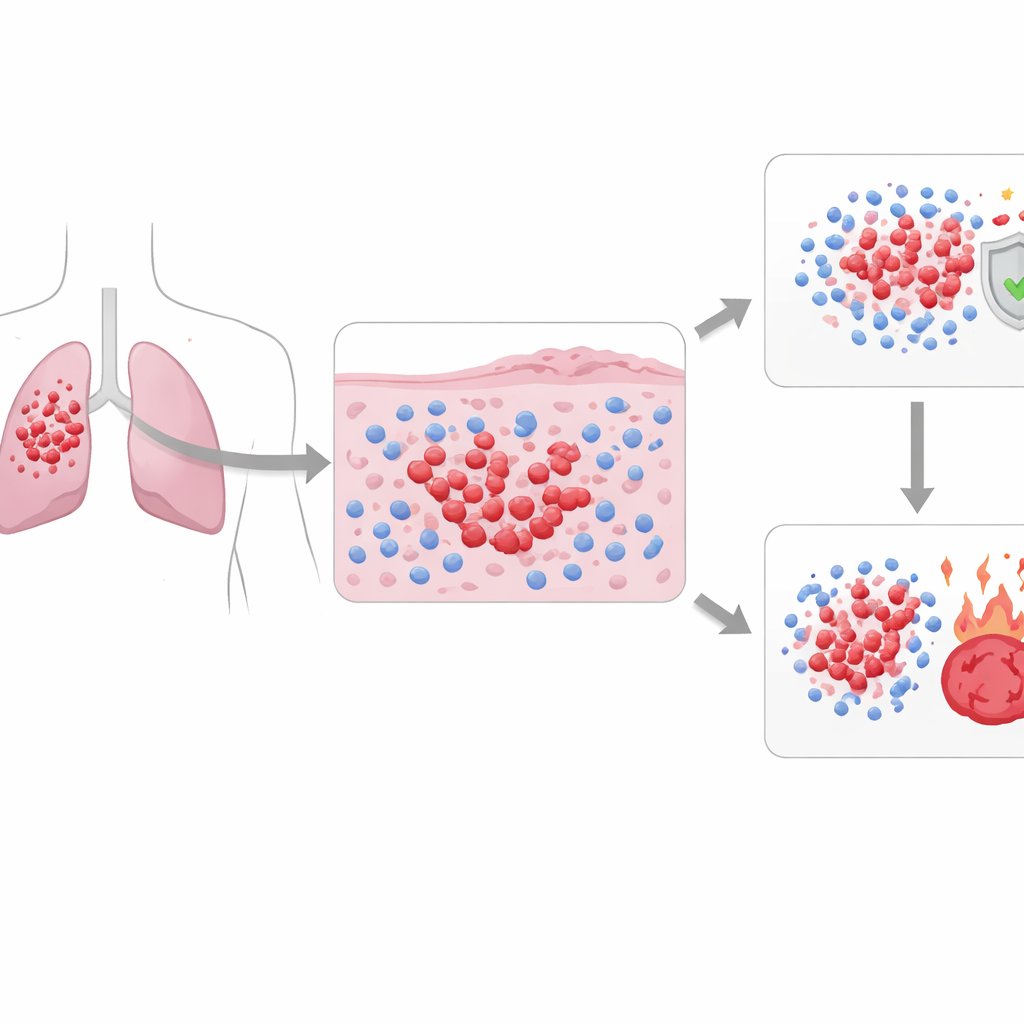
Genaueres Hinschauen bei einem tödlichen Lungenkrebs
Kleinzelliger Lungenkrebs macht etwa 15 % der Lungenkrebserkrankungen aus, verursacht jedoch einen großen Anteil der Todesfälle, weil er schnell wächst und metastasiert. Üblicherweise unterscheidet man eine „begrenzte“ Erkrankung, die in ein Strahlungsfeld passt, von einer „ausgedehnten“ Erkrankung mit weiter Verbreitung. Die Standard-Erstlinie ist eine potente platinhaltige Chemotherapie, manchmal in Kombination mit Immuntherapie. Viele Tumoren sprechen zunächst gut an, doch der Krebs kehrt oft innerhalb eines Jahres zurück, und weniger als einer von zehn Patientinnen und Patienten überlebt langfristig. Gegenwärtige Tests, die Tumorgröße, Ausbreitung und grundlegendes mikroskopisches Erscheinungsbild berücksichtigen, erklären nicht, warum einige Patientinnen und Patienten auf dieselben Medikamente besser reagieren als andere.
Computern beibringen, Tumornachbarschaften zu lesen
Die Forschenden entwickelten PhenopyCell, um standardmäßig gefärbte Gewebeschnitte in eine detaillierte Karte von Zell„nachbarschaften“ zu verwandeln. Mit bereits vorhandenen Deep‑Learning‑Werkzeugen brachten sie einem Computer zuerst bei, einzelne Tumorzellen und Immunzellen auf digitalen Bildern von Biopsien aus 281 Patientfällen aus drei US‑Zentren zu erkennen und zu markieren. Anschließend teilten sie jede Folie in Tumor-, nahes Gewebe‑ und entfernte Nicht‑Tumor‑Regionen und berechneten über hundert numerische Merkmale. Diese Merkmale beschreiben zum Beispiel, wie dicht Immunzellen um Tumorklumpen angeordnet sind, wie weit Immunzellen von Krebszellen entfernt sitzen, wie vielfältig die Zellmischung ist und wie regelmäßig die Zellen über das Präparat verteilt sind.
Verborgene Muster, die mit Überleben und Therapieansprechen verknüpft sind
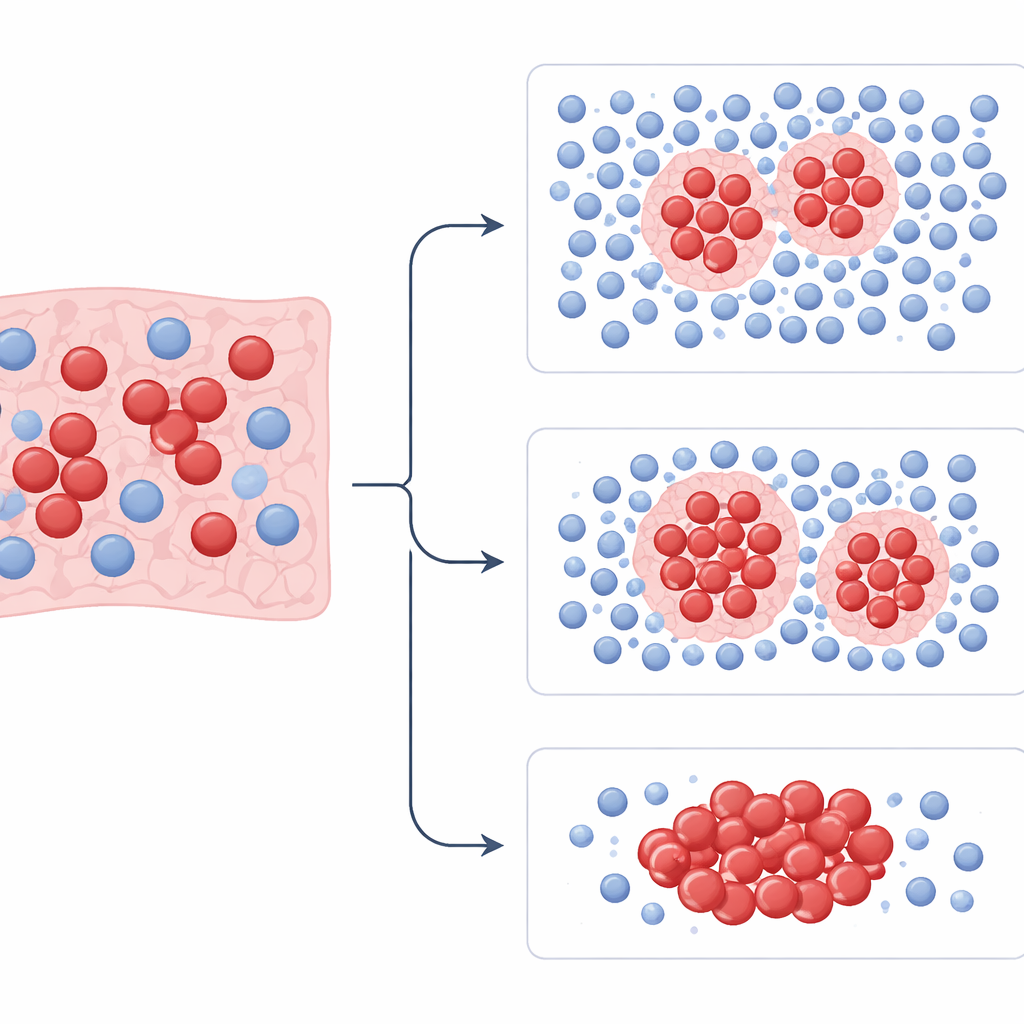
Mit diesen Messwerten trainierte das Team Modelle, um Patientinnen und Patienten in höher- und niedrigrisiko Gruppen zu trennen und vorherzusagen, wer auf eine Platin‑Chemotherapie ansprechen würde. Die Modelle wurden an Fällen eines Krankenhauses trainiert und dann an Patientengruppen der beiden anderen Krankenhäuser getestet. In allen Datensätzen zeigten die von PhenopyCell erfassten Muster starke Zusammenhänge mit dem Gesamtüberleben und mit dem Ansprechen auf Chemotherapie. Patientinnen und Patienten, deren Tumoren viele organisierte Areale mit dicht um Tumorklumpen sitzenden Immunzellen zeigten, lebten tendenziell länger. Bei verstreuten oder spärlichen Immunzellen und sehr ungleichmäßiger Verteilung der Tumorzellen bestanden häufiger aggressive Erkrankungsverläufe und schlechtere Outcomes. Diese Zusammenhänge blieben bestehen, selbst wenn Alter, Geschlecht und andere klinische Faktoren berücksichtigt wurden, und sie zeigten sich sowohl in begrenzten als auch in ausgedehnten Krankheitsstadien.
Jenseits von Black‑Boxen und routinemäßigen Mikroskopprüfungen
Die Studie verglich PhenopyCell außerdem mit neueren „foundation“ KI‑Modellen und mit traditionellen Messgrößen von Immunzellen, den tumorinfiltrierenden Lymphozyten. Einige große Deep‑Learning‑Modelle erzielten zwar hohe Genauigkeit in der ursprünglichen Trainingsgruppe, lieferten jedoch bei externen Testpatienten inkonsistente Ergebnisse, was Fragen zur Stabilität aufwarf. Einfache Zählungen von Immunzellen, ob computerbasiert oder von einer Pathologin bzw. einem Pathologen geschätzt, sagten das Überleben ebenfalls nicht zuverlässig voraus. Im Gegensatz dazu lieferte PhenopyCells Fokus darauf, wie Immun‑ und Tumorzellen räumlich angeordnet sind – nicht nur wie viele vorhanden sind – zuverlässigere und leichter interpretierbare Signale. Die verwendeten Merkmale lassen sich direkt mit biologischen Konzepten verknüpfen, etwa Immunexklusion, Nekrosearealen und variierenden Tumorformen.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht‑Spezialisten ist die Kernbotschaft, dass die „Architektur“ eines Tumors – also wie Krebszellen und die Verteidiger des Körpers das Schlachtfeld besetzen – wichtige Hinweise darauf enthält, wie sich die Erkrankung verhalten wird und wie sie auf Behandlung reagiert. PhenopyCell zeigt, dass sich diese Hinweise aus den bereits im Rahmen der Standardversorgung entnommenen routinemäßigen Biopsieschnitten gewinnen lassen, ohne zusätzliche Eingriffe. Da die Studie retrospektiv ist und überwiegend Patientinnen und Patienten umfasst, die nur Chemotherapie erhielten, sind größere, prospektive Studien, insbesondere bei Patientengruppen mit modernen Immuntherapien, nötig, bevor ein solches System in den klinischen Alltag einfließen kann. Dennoch weist diese Arbeit einen klaren Weg hin zu einer stärker personalisierten Versorgung beim kleinzelligen Lungenkrebs.
Zitation: Barrera, C., Jain, P., Corredor, G. et al. Computational pathology features of immune architecture predict clinically relevant outcomes in small-cell lung cancer (SCLC). npj Precis. Onc. 10, 119 (2026). https://doi.org/10.1038/s41698-025-01225-9
Schlüsselwörter: kleinzelliger Lungenkrebs, computationale Pathologie, Tumormikroumgebung, Architektur von Immunzellen, Vorhersage des Ansprechens auf Behandlung