Clear Sky Science · de
Entschlüsselung von Gehirnmetastasen beim epithelialen Eierstockkarzinom: multimodale Analyse und potenzielle Biomarker
Warum diese Forschung wichtig ist
Eierstockkrebs ist bereits eine lebensbedrohliche Erkrankung, doch bei einer kleinen Zahl von Frauen tritt er später an einem besonders fragilen Ort auf: im Gehirn. Diese Hirnmetastasen sind selten, aber oft tödlich, und Ärztinnen und Ärzte haben noch wenige Mittel, vorherzusagen, wer gefährdet ist oder wie man sie am besten behandelt. Die vorliegende Studie verfolgt diese Wanderung vom Becken ins Gehirn auf molekularer Ebene und nutzt moderne DNA- und RNA-Werkzeuge, um zu verstehen, wie sich Eierstocktumoren im Gehirn anpassen und welche frühen Warnzeichen eines Tages eine individuellere Versorgung ermöglichen könnten.
Von einem häufigen Krebs zu einer seltenen Bedrohung im Gehirn
Das epitheliale Eierstockkarzinom ist die tödlichste gynäkologische Krebserkrankung in Industrieländern. Die meisten Patientinnen sprechen zunächst auf Operation und Chemotherapie an, doch etwa 80 Prozent erleben schließlich ein Wiederauftreten der Erkrankung mit Resistenz gegenüber Medikamenten. Rezidive bleiben meist im Abdomen; nur ein kleiner Teil der Frauen entwickelt Fernmetastasen, etwa im Gehirn. Da sich die Behandlungen verbessern und die Patientinnen länger leben, haben verstreute Krebszellen jedoch mehr Zeit, das Gehirn zu besiedeln, sodass diese Metastasen zunehmend beobachtet werden. Sobald Gehirnmetastasen auftreten, sinkt das typische Überleben auf unter ein Jahr, was die Dringlichkeit unterstreicht, zu verstehen, wie und warum dies geschieht.
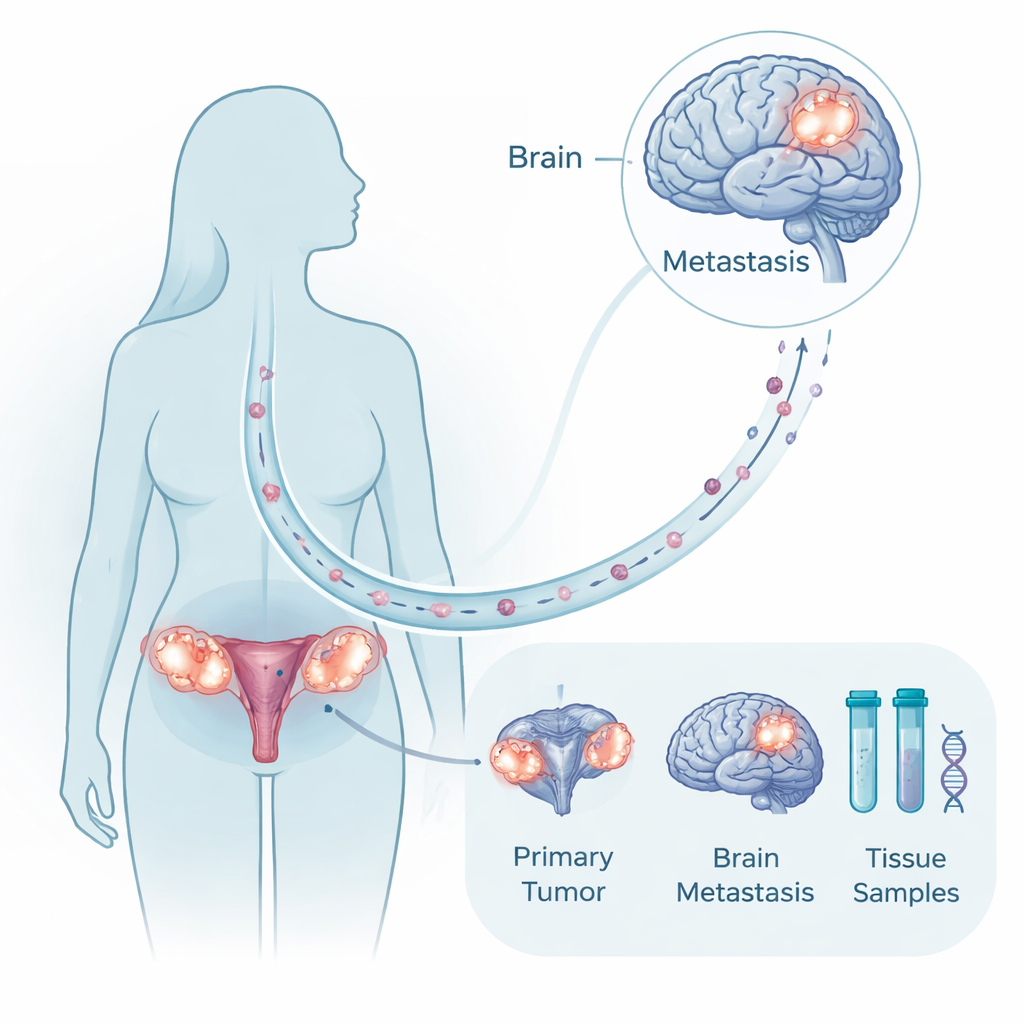
Eine seltene, aber wertvolle Gewebesammlung
Weil eine Hirnoperation für viele Patientinnen nicht möglich oder nicht angebracht ist, sind Tumorproben sowohl vom ursprünglichen Eierstocktumor als auch von der entsprechenden Hirnablagerung derselben Frau ungewöhnlich. Die Forschenden stellten genau dieses gepaarte Material von zehn Patientinnen zusammen, die über zwei Jahrzehnte behandelt wurden, ergänzt durch Vergleichsproben aus gesundem Gehirn und Eierstock sowie aus anderen, nicht zerebralen Metastasen. Sie analysierten Tumor-DNA auf Mutationen und große chromosomale Veränderungen und untersuchten RNA, um zu sehen, welche Gene an- oder abgeschaltet sind. Dieser multimodale Ansatz erlaubte es ihnen zu prüfen, ob Hirntumoren völlig neue Abzweigungen sind oder eng verwandte Nachkommen des Primärtumors, und welche molekularen Programme sich verändern, wenn Zellen im Gehirn Fuß fassen.
Genetische Stabilität, aber neues Verhalten
Die DNA-Analyse zeigte, dass die ursprünglichen Eierstocktumoren und ihre entsprechenden Hirnmetastasen bemerkenswert ähnlich waren. Beide trugen viele der gleichen krebsfördernden Mutationen, insbesondere im Gen TP53, und teilten einen insgesamt „monoklonalen“ Ursprung, was bedeutet, dass die Hirnherde offenbar aus derselben Stammkrebszelle hervorgingen. Große DNA-Gewinne und -Verluste kamen in den Hirnherden etwas häufiger vor, waren aber nicht überwältigend. Das legt nahe, dass die Ausbreitung ins Gehirn nicht durch den Erwerb eines völlig neuen Satzes von Mutationen ermöglicht wird. Stattdessen zeigt sich die entscheidende Veränderung auf der Ebene der Genaktivität: welche Anweisungen aus der DNA abgelesen und von den Krebszellen genutzt werden, während sie sich an die einzigartige Umgebung des Gehirns anpassen.
Wie Eierstocktumoren lernen, im Gehirn zu überleben
Beim Vergleich der Genaktivität über alle Gewebe hinweg trat ein charakteristisches Signaturmuster für Gehirnmetastasen zutage. Hirnherde zeigten Anzeichen aggressiven Wachstums mit Aktivierung von Zellzyklusprogrammen, die von bekannten Krebsregulatoren wie MYC und E2F gesteuert werden. Sie veränderten auch Proteine, die das Gewebsgerüst bilden und umgestalten, was den Zellen hilft, in Hirngewebe einzudringen und sich dort zu verankern. Auffallend war, dass einige Gene, die mit Nerven- und Gliazellen verbunden sind, hochreguliert waren, was darauf hindeutet, dass Eierstockkrebszellen zum Teil Gehirnzellen nachahmen, um sich anzupassen. Besonders bemerkenswert waren AFP, üblicherweise im Fetus und in bestimmten Tumoren aktiv, und GFAP, ein typisches Protein von Stützzellen im Gehirn. Die Autorinnen und Autoren identifizierten außerdem eine kleine Gruppe von Genen, die bereits im Primärtumor von Frauen erhöht waren, die später Gehirnmetastasen entwickelten, nicht jedoch bei Langzeitüberlebenden ohne Hirnbeteiligung. Dieses „prämétastatische“ Muster betraf Immunmodulation, Kommunikation über nervenähnliche Signale und Veränderungen im Stoffwechsel.
Frühe Warnsignale und molekularer Dialog
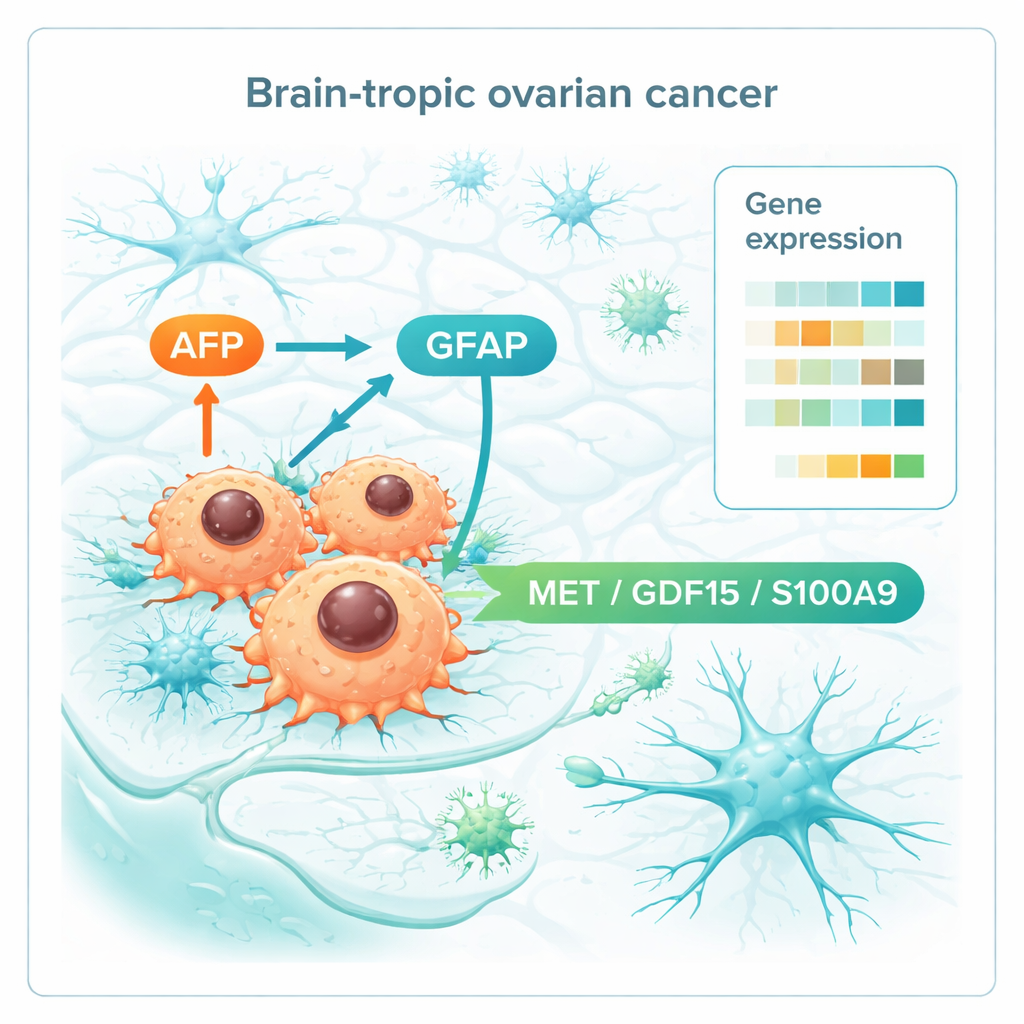
Die Forschenden gingen noch weiter und konzentrierten sich auf Moleküle, die an der Zelloberfläche sitzen oder ausgeschieden werden, da diese hervorragende Kandidaten für Bluttests oder Arzneimittelziele sind. Sie identifizierten drei Akteure — MET, GDF15 und S100A9 — die sowohl in Primärtumoren, die zum Gehirn metastasierten, als auch in den Hirnmetastasen selbst konsistent erhöht waren. Diese Moleküle sind an Zellbewegung, Stress- und Nährstoffwahrnehmung sowie an der Gestaltung des Immunmilieus beteiligt, was darauf hindeutet, dass sie Eierstockkrebszellen helfen, mit dem Gehirngewebe zu kommunizieren und es zu ihren Gunsten umzugestalten. Zusammen mit AFP und GFAP bilden sie eine kurze Liste potenzieller Biomarker, die eines Tages Hochrisikopatientinnen markieren oder auf Wirkstoffe hinweisen könnten, die die Tumor–Gehirn-Kommunikation stören.
Was das für Patientinnen bedeutet
Vorerst wird diese Arbeit die Behandlung nicht sofort verändern, und die Autorinnen und Autoren räumen ein, dass ihre Patientinnenkohorte klein ist. Indem sie jedoch zeigen, dass hirnmetastasierende Eierstockkrebse große Teile ihres ursprünglichen genetischen Profils bewahren, während sie die Nutzung ihrer Gene umprogrammieren, hebt die Studie neue Wege hervor, Probleme früh zu erkennen. Bestätigen künftige Forschungen, dass Marker wie AFP, GFAP, MET, GDF15 und S100A9 zuverlässig auf eine Neigung zum Befall des Gehirns hinweisen, könnten Ärztinnen und Ärzte bestimmte Patientinnen enger überwachen, Therapieentscheidungen anpassen oder Wirkstoffe testen, die diese Signalwege blockieren. Im Kern beginnt die Studie, eine angsteinflößende späte Komplikation in einen Prozess zu verwandeln, der messbar, verständlich und schließlich abwendbar ist.
Zitation: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
Schlüsselwörter: Eierstockkrebs, Gehirnmetastasen, Biomarker, Genexpression, präzisionsonkologie