Clear Sky Science · de
Adipozyten-gesteuerte STAT3-ANGPT2-PTGIS-Achse fördert kutane Metastasen beim Brustkrebs und stellt einen angreifbaren Signalweg dar
Warum die Ausbreitung auf die Haut bei Brustkrebs wichtig ist
Wenn Brustkrebs gestreut hat, denken die meisten Menschen an Knochen, Leber oder Lunge. Doch bei vielen Patientinnen und Patienten taucht der Krebs an einem unerwarteten Ort wieder auf: an der Haut der Brustwand, manchmal Jahre nachdem der ursprüngliche Tumor entfernt wurde. Diese hartnäckigen, schmerzhaften Hautknoten sind nicht nur ein kosmetisches Problem — sie sind ein Zeichen einer aggressiven Erkrankung, die schwer zu behandeln ist. Diese Studie untersucht, warum manche Brustkrebse zur Haut hingezogen werden, und zeigt eine überraschende Partnerschaft zwischen Krebszellen, dem umliegenden Fettgewebe sowie den Blut- und Lymphgefäßen, die Tumore versorgen.
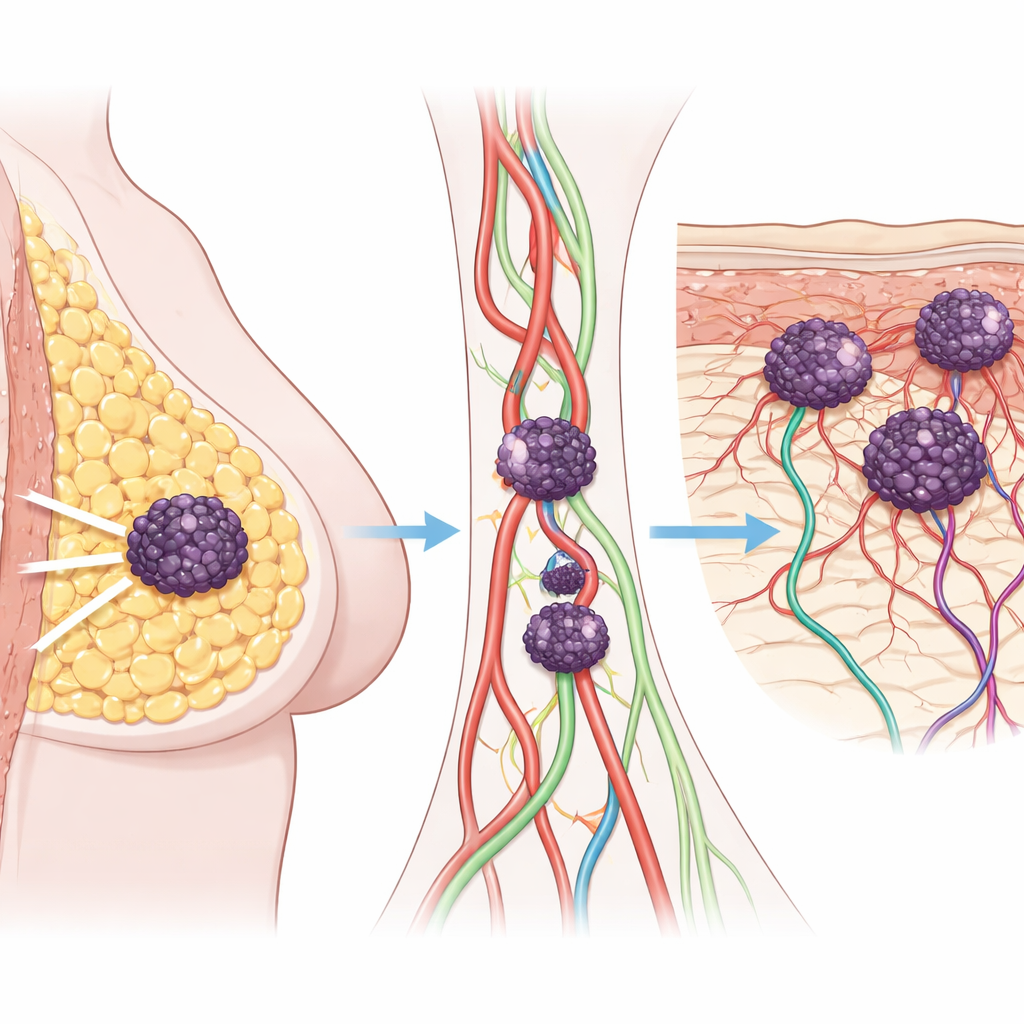
Hauttumoren als Warnsignal
Die Forschenden werteten zunächst Krankengeschichten von 126 Personen mit Brustkrebs aus und verglichen diejenigen, bei denen kein Rückfall auftrat, jene, deren Krebs in Organe wie Lunge oder Knochen gestreut hatte, und jene, die Hautmetastasen entwickelten. Patientinnen und Patienten, deren Erkrankung sich ausschließlich in der Haut wieder zeigte, hatten bereits zum Zeitpunkt der Diagnose fortgeschrittenere und schnell wachsende Tumoren. Ihre Tumore wiesen hohe Teilungsraten der Zellen und frühe Invasionen in Blut- und Lymphgefäße auf. Obwohl einige dieser Betroffenen keine sichtbaren Fernmetastasen hatten, waren ihre Gesamt- und krankheitsfreien Überlebensraten schlechter als bei Patientinnen und Patienten ohne Hautbeteiligung, was hervorhebt, dass Hautmetastasen eine besonders aggressive Form von Brustkrebs kennzeichnen.
Blutgefäße und Fett formen die Hautnische
Um zu verstehen, was die Haut zu einem so fruchtbaren Boden macht, verfolgte das Team eine Patientin über mehrere Jahre und sammelte Proben aus dem ursprünglichen Brusttumor und späteren Hautknoten. Unter dem Mikroskop waren sowohl Brust- als auch Hautläsionen reich an neu gebildeten Blut- und Lymphgefäßen — winzige Autobahnen, die Krebszellen helfen, zu wandern und sich festzusetzen. Die Genaktivitätsprofilierung zeigte, dass die Tumore mit fortschreitender Erkrankung ganze Netzwerke einschalteten, die mit Blutgefäßwachstum, Entzündung und der Verarbeitung von Fetten und Fettsäuren zusammenhängen. Insbesondere wurden Wege, die den Abbau üblicher Nahrungsfette wie Arachidonsäure und Linolsäure betreffen, stärker aktiv, was darauf hindeutet, dass Energie aus Fett und den eigenen Fettdepots der Haut die Tumorentwicklung fördert.
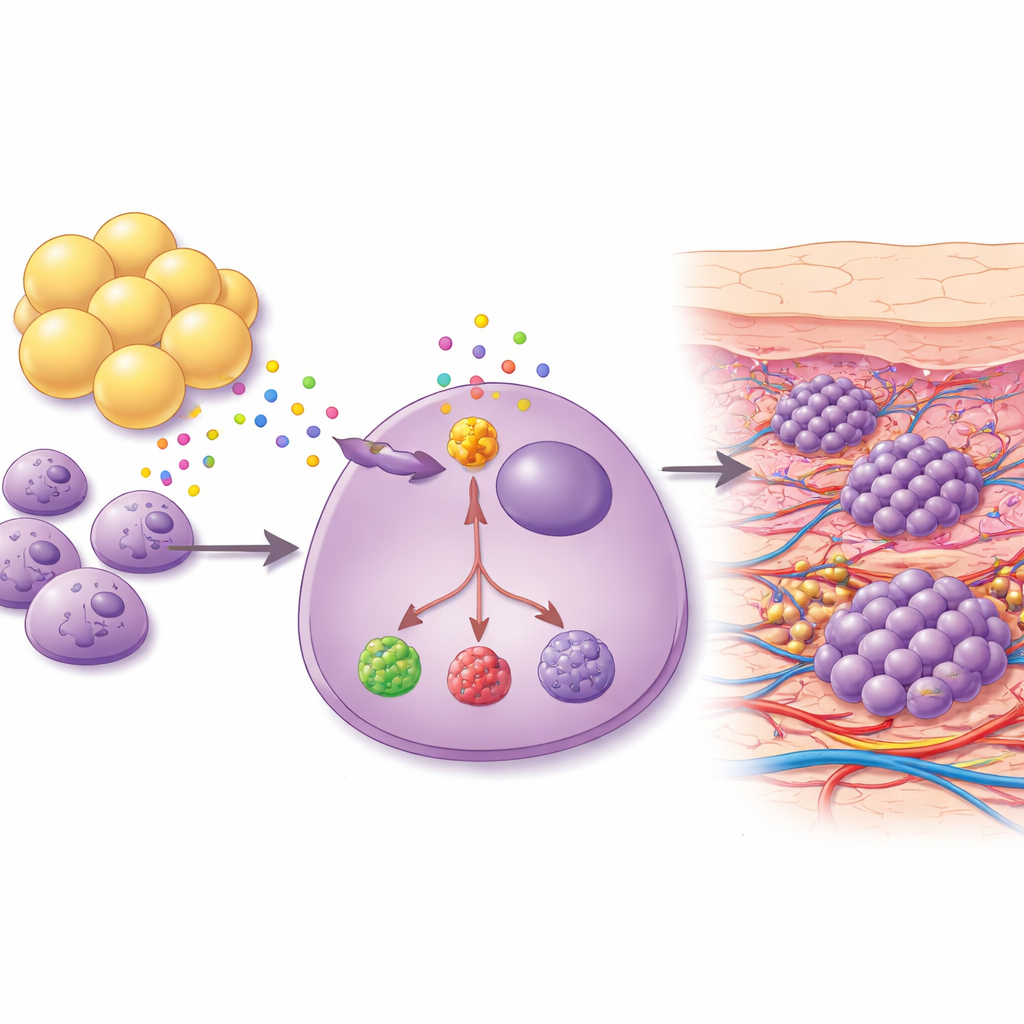
Fettzellen senden starke Wachstumssignale
Da Brust und darunterliegende Brustwand reich an Fett sind, fragten die Forschenden, ob Fettzellen selbst Krebszellen zur Haut locken könnten. Sie kultivierten Brustkrebszellen zusammen mit Adipozyten — reifen Fettzellen — aus derselben Patientin und sammelten das Gemisch der von den Fettzellen freigesetzten Moleküle. Dieser Cocktail verstärkte stark die Fähigkeit von Blutgefäßzellen, im Labor röhrenartige Strukturen zu bilden, ein Kennzeichen der Angiogenese. In Mäusemodellen führte die Exposition von Tumoren gegenüber dem von Fettzellen abgeleiteten Medium zu neuem Krebswachstum in haut- und fettreichen Bereichen wie Hals und Rücken. Aus diesen Hautläsionen gewonnene Krebszellen waren stammzellähnlicher, widerstandsfähiger gegen das Absterben und produzierten höhere Mengen an Wachstums- und Entzündungsfördernden Faktoren, darunter das Protein ANGPT2 und das Stoffwechselenzym PTGIS.
Ein Signalumschalter, der abgeschaltet werden kann
Bei tiefergehenden Untersuchungen verglich das Team gewöhnliche Tumorzellen mit ihren hautaffinen Gegenstücken und stellte fest, dass ein verbreiteter intrazellulärer Kommunikationsweg — der JAK–STAT-Signalweg — stark aktiviert war, insbesondere das Protein STAT3. Wenn STAT3 aktiviert ist, wirkt es wie eine Schaltzentrale und erhöht ANGPT2, VEGFC (ein Treiber des Lymphgefäßwachstums) und PTGIS, die alle Blutgefäßbildung und die Umgestaltung der Tumorumgebung fördern. Die Blockade von STAT3 mit dem Wirkstoff Stattic verringerte das Wachstum von Hauttumoren bei Mäusen und senkte die Konzentration dieser nachgeschalteten Faktoren. In Tumorproben von Patientinnen und Patienten war hohe Aktivität von STAT3, ANGPT2 und PTGIS mit einem schlechteren progressionsfreien und krankheitsfreien Überleben verknüpft, und diese Marker waren besonders erhöht bei Patientinnen und Patienten, deren Metastasen auf die Haut beschränkt waren.
Was das für Patientinnen und Patienten bedeutet
In der Summe zeichnet die Arbeit das kutane metastatische Mammakarzinom als einen eigenständigen und gefährlichen Subtyp, der von einer Dreiecksbeziehung zwischen Krebszellen, umliegendem Fett und den Gefäßen, die Tumore versorgen, angetrieben wird. Signale aus Adipozyten aktivieren STAT3 in Krebszellen, was wiederum ANGPT2 und PTGIS hochfährt und den Fettsäurestoffwechsel umgestaltet, sodass die Haut zu einer gastfreundlichen Nische wird, in der Tumore siedeln und wachsen können. Für Patientinnen und Patienten bedeutet das, dass Hautmetastasen nicht einfach „lokale“ Rückfälle sind, sondern Marker einer aggressiven Biologie. Ermutigend ist, dass derselbe Weg, der diesen Prozess antreibt, auch seine Schwachstelle sein könnte: Medikamente, die STAT3 oder Schlüssel-Enzyme des Stoffwechsels wie PTGIS hemmen, könnten zukünftig helfen, die Versorgungsleitungen zu kappen, die es Brustkrebs ermöglichen, die Haut zu kolonisieren.
Zitation: Luo, CW., Ou-Yang, F., Chang, SJ. et al. Adipocyte-driven STAT3-ANGPT2-PTGIS axis promotes cutaneous metastasis in breast cancer and represents a targetable pathway. npj Precis. Onc. 10, 111 (2026). https://doi.org/10.1038/s41698-025-01184-1
Schlüsselwörter: Hautmetastasen bei Brustkrebs, Tumormikroumgebung, Adipozyten-Signalgebung, STAT3-Signalweg, Angiogenese