Clear Sky Science · de
Methoden für randomisierte, verblindete, kontrollierte Bewertung vermeintlicher Krankheitsinterventionen in multilaboratorischen, präklinischen Bewertungsnetzwerken
Warum das für die tägliche Gesundheit wichtig ist
Viele vielversprechende medizinische Behandlungen wirken in Tierversuchen stark, scheitern dann aber in großen, teuren klinischen Studien. Dieser Artikel zeigt konkret, wie Wissenschaftler jene frühen Tierversuche so umgestalten können, dass ihre Ergebnisse vertrauenswürdiger sind und eher vorhersagen, was bei echten Patientinnen und Patienten passieren wird – als Fallbeispiel dient der Schlaganfall. 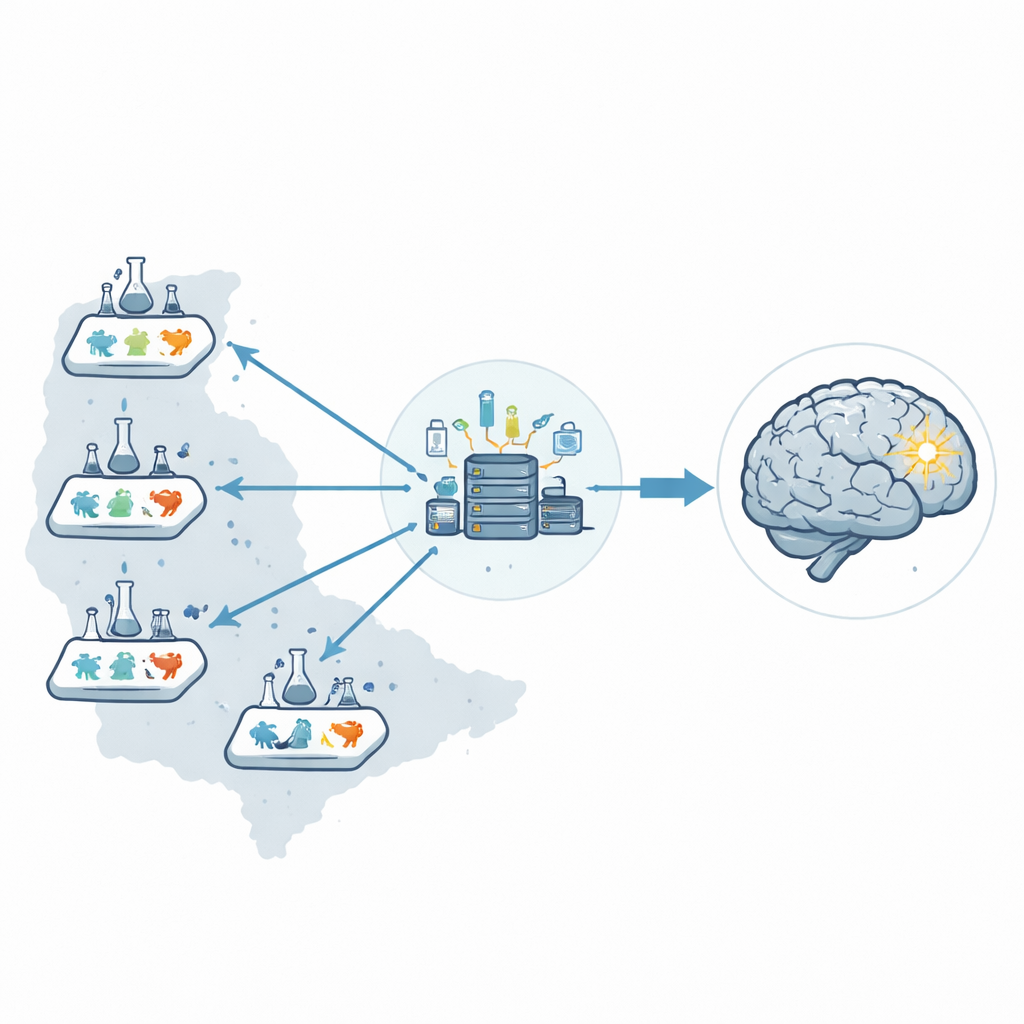
Ein Netzwerk statt eines einzelnen Labors aufbauen
Anstatt sich auf ein Labor zu stützen, errichteten die Forschenden ein sechslaboriges präklinisches Netzwerk in den Vereinigten Staaten, das Stroke Preclinical Assessment Network heißt. Ein zentrales Koordinationszentrum leitete den gesamten Ablauf: Versand kodierter Wirkstoffampullen, zufällige Zuweisung der Behandlungen, Entgegennahme aller Daten und Durchführung der Statistik. Indem diese Aufgaben von den Personen getrennt wurden, die Operationen durchführten oder Ergebnisse bewerteten, verringerten sie die Chance, dass menschliche Erwartungen die Resultate unmerklich beeinflussen.
Fairness und Verblindung in der Praxis
Um die Regeln einer guten klinischen Studie nachzuahmen, wurde jedes Tier bei Ankunft erfasst, gekennzeichnet und nachverfolgt. Behandlungen wurden in identischen Ampullen verpackt, sodass Chirurginnen und Chirurgen während der Schlaganfallinduktion und Therapie nicht zwischen Wirkstoff und Placebo unterscheiden konnten. Ein strukturiertes Randomisierungsprogramm sorgte dafür, dass Männchen und Weibchen, verschiedene Schlaganfallmodelle und alle sechs Standorte gleichmäßig zu jeder Behandlungsgruppe beitrugen. Selbst wenn ein Tier verstarb oder ein Eingriff scheiterte, blieb es im Protokoll, sodass Ausfälle nicht stillschweigend ausgeblendet werden konnten und versteckte Verzerrungen vermieden wurden.
Behandlungen in realistischen Schlaganfallmodellen testen
Das Netzwerk verwendete fünf verschiedene Nagetiermodelle, die zusammen wichtige Aspekte des menschlichen Schlaganfalls abbildeten, darunter Alter, Bluthochdruck und diätbedingt verursachte Fettleibigkeit. Der Schlaganfall wurde an allen Standorten auf dieselbe Weise erzeugt, indem kurzzeitig eine große Hirnarterie blockiert und dann der Blutfluss wiederhergestellt wurde – vergleichbar mit modernen Verfahren zur Gerinnselentfernung beim Menschen. Die Tiere erhielten eine von sechs Kandidatenbehandlungen mit potenziell schützender Wirkung oder eine passende Kontrollbehandlung. Das Team verfolgte die Tiere mit einfachen Bewegungstests, etwa wie sie in einer Ecke abdrehten oder auf einem Gitter liefen, sowie mit Hirnscans, um die Größe der Schädigung über 30 Tage zu messen.
Verblindete Bewertung, gemeinsame Daten und durchdachte Statistik
Um Bewertungen unvoreingenommen zu halten, wurden Verhaltenstests auf Video aufgezeichnet und in ein zentrales Archiv hochgeladen. Diese Videos, von identifizierenden Informationen bereinigt, wurden an geschulte Bewerter in anderen Laboren geschickt, die sie ohne Kenntnis der Behandlung oder des Testortes bewerteten. Magnetresonanztomographien wurden durch eine automatisierte Analysepipeline geleitet, die Gehirn und Schadensareal mit minimaler menschlicher Eingabe segmentierte. Alle Ergebnisse flossen in ein Multiarm‑, Mehrstufen‑Statistikdesign ein, das erlaubte, mehrere Behandlungen parallel zu prüfen: Schwache oder offensichtlich unwirksame Kandidaten konnten früh verworfen werden, während vielversprechende weiter in spätere Phasen vorrückten. 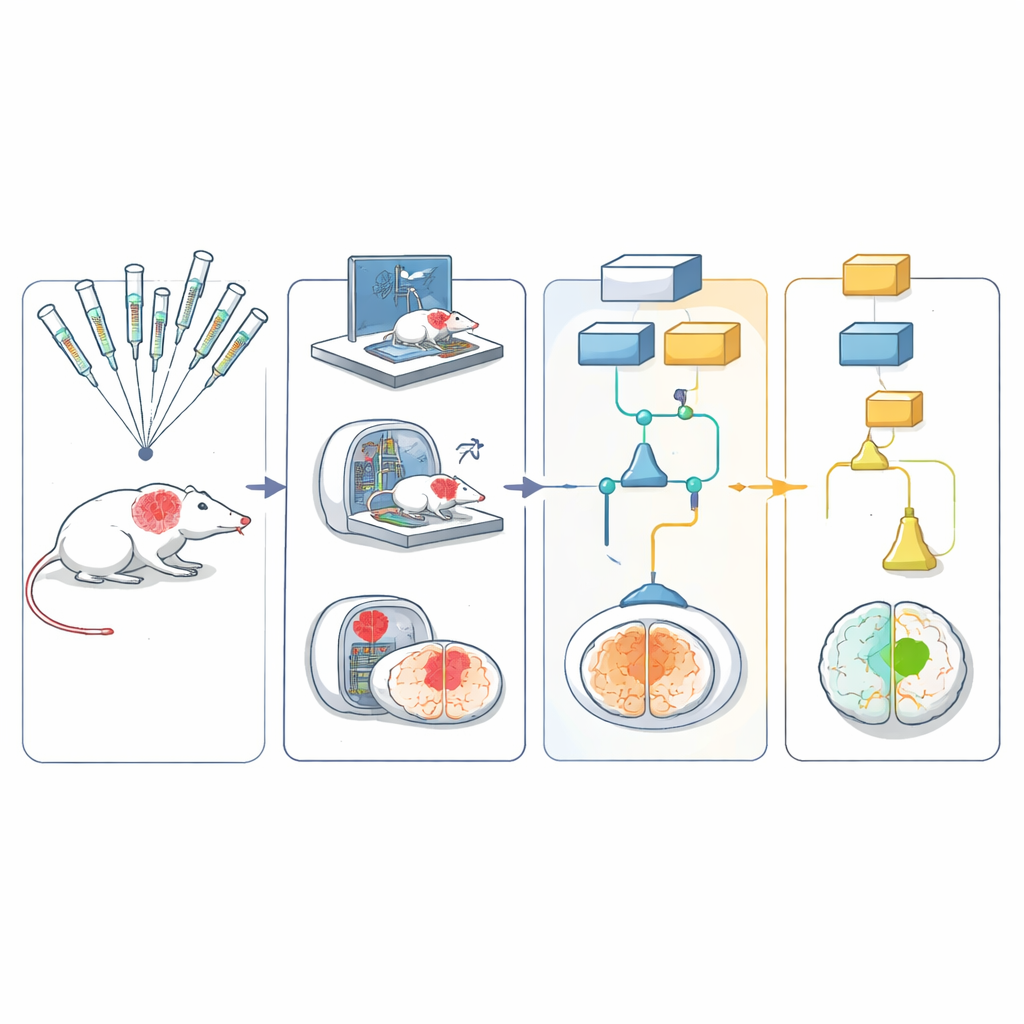
Was die Ergebnisse über Schlaganfalltherapien zeigten
Über vier Stufen und 2.615 Tiere erwies sich das System als praktikabel, selbst während der Störungen durch die COVID‑19‑Pandemie. Die Methoden hielten die Behandlungsgruppen beständig ausgeglichen, minimierten Fehler bei der Dosierung und zeigten eine Verbesserung der Datenqualität, als die Standorte die Lernkurve durchliefen. Am Ende wurden fünf von sechs Behandlungen ausgeschlossen, während eine — Harnsäure, ein Radikalfänger — die vorab festgelegte Schwelle für einen Nutzen erfüllte. Gleichzeitig zeigte die Arbeit Grenzen einiger populärer Modelle auf, etwa sehr hohe Sterblichkeitsraten bei alten Mäusen, was darauf hindeutet, dass sie für künftige Studien möglicherweise unpraktisch oder unrealistisch sind.
Großes Fazit: eine Vorlage für verlässlichere präklinische Wissenschaft
Für eine interessierte Leserin oder einen interessierten Leser ist die Kernbotschaft, dass die Art und Weise, wie wir Behandlungen an Tieren testen, genauso wichtig ist wie das, was wir testen. Indem die Schutzmaßnahmen moderner klinischer Studien — Randomisierung, Verblindung, lückenlose Erfassung jeder Versuchsperson und sorgfältige Statistik — in die Tierforschung übernommen werden, zeigt dieses Netzwerk, dass frühe Studien sowohl rigoroser als auch effizienter sein können. Das detaillierte Handbuch, das sie liefern, lässt sich auf andere Krankheiten übertragen und bietet einen Weg zu Laborbefunden, die Replikationen standhalten und Ärztinnen, Patienten sowie Förderern mehr Vertrauen geben, dass eine Therapie im klinischen Einsatz tatsächlich Aussicht auf Wirksamkeit hat.
Zitation: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Schlüsselwörter: Schlaganfall, präklinische Studien, Tiermodelle, Forschungs‑Rigorosität, multizentrische Studien