Clear Sky Science · de
PiggyBac-vermittelte Transgenese und CRISPR–Cas9-Knockout beim Großen Wachsraupenfalter, Galleria mellonella
Eine winzige Raupe mit großem medizinischen Potenzial
Stellen Sie sich vor, neue Antibiotika zu testen oder gefährliche Infektionen zu untersuchen, ohne Mäuse oder andere Säugetiere zu verwenden. Die Larven des Großen Wachsraupenfalters, Galleria mellonella, entwickeln sich zunehmend zu einem kostengünstigen, ethisch attraktiven Ersatz für solche Experimente. Diese Studie zeigt, wie Forschende einen wichtigen Schritt vorangekommen sind, indem sie diesen Raupen die gleichen genetischen Werkzeuge geben, die Fruchtfliegen und Zebrafische so leistungsfähig für die biomedizinische Forschung gemacht haben.
Warum dieses Insekt für die menschliche Gesundheit wichtig ist
Die Larven von Galleria mellonella ahmen überraschend gut nach, wie der menschliche Körper auf Keime reagiert. Sie können bei 37 °C – unserer Körpertemperatur – gehalten werden und lassen sich mit einer Vielzahl medizinisch relevanter Bakterien und Pilze infizieren. Wenn sie erkranken, verdunkelt sich ihr Körper durch einen Prozess namens Melanisierung, der Forschenden eine sichtbare Anzeige des Gesundheitszustands liefert. Da sie wirbellose Tiere sind, entfallen viele der rechtlichen und ethischen Hürden, die mit Wirbeltierexperimenten verbunden sind, und sie sind billig in großen Mengen zu züchten. Die Larven wurden sogar gefunden, als sie gängige Kunststoffe abbauen, was auf mögliche Anwendungen in der Umweltforschung hinweist.
Das fehlende genetische Werkzeug
Trotz dieser Vorteile fehlten den Wachsraupen bislang die ausgefeilten genetischen Techniken, die in klassischen Labortieren verfügbar sind. In den letzten zehn Jahren haben mehrere Teams das Genom des Falters entschlüsselt und seine aktiven Gene und Proteine katalogisiert, doch Forschende konnten Gene bislang nicht leicht an- oder abschalten oder nützliche Marker einfügen. Diese Lücke begrenzte, was mit dem Modell möglich war – etwa Tiere zu bauen, die bei einer Infektion aufleuchten, oder spezifische Gene zu löschen, um ihre Rolle in der Immunantwort zu testen. Die vorliegende Arbeit geht dieses Problem direkt an, indem sie zwei leistungsfähige Gentechniksysteme, bekannt als PiggyBac und CRISPR–Cas9, für die Anwendung in Galleria mellonella adaptiert.
Leuchtende Reporter-Larven erzeugen
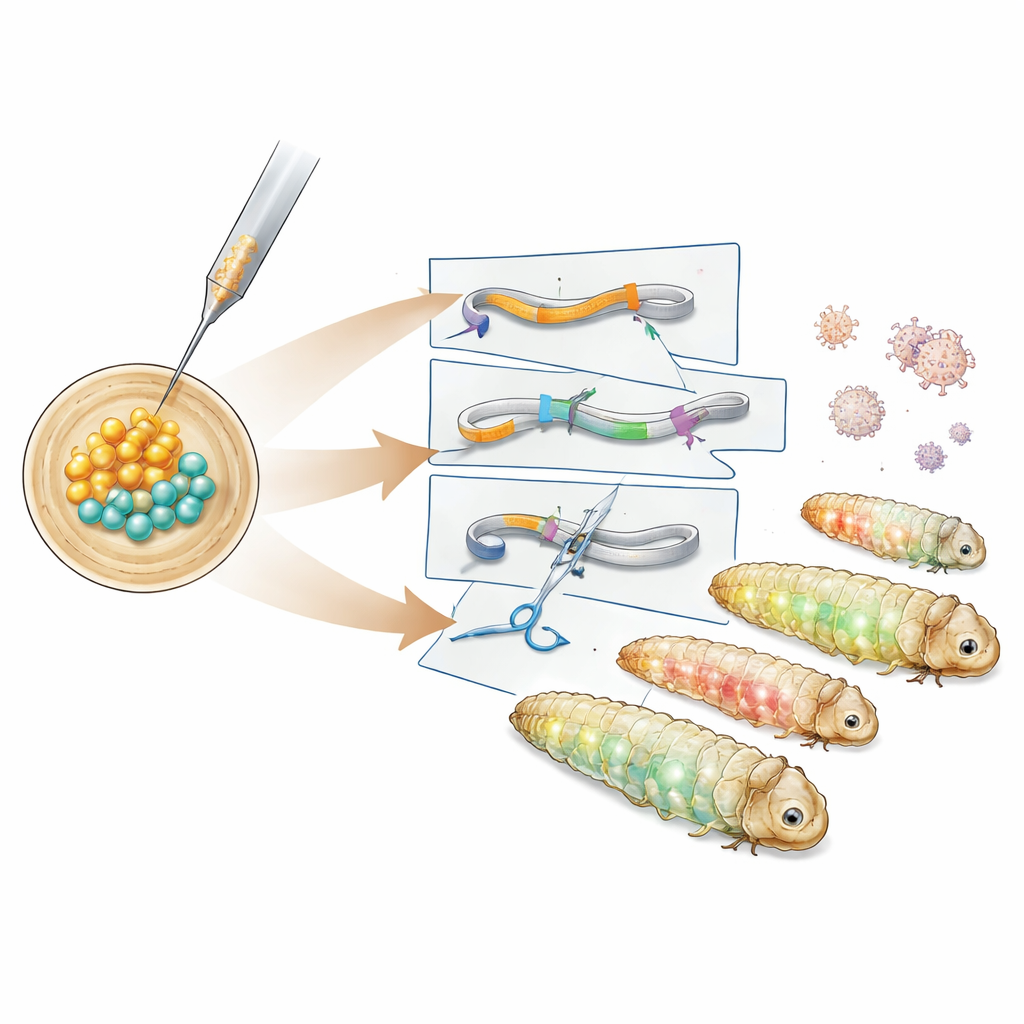
Das Team untersuchte zunächst den Zeitpunkt der frühen Embryonalentwicklung der Motte und fand ein etwa sechs Stunden langes Fenster nach der Eiablage, in dem sich alle teilenden Zellkerne noch ein gemeinsames Inneres teilen. Das Injizieren von DNA während dieses Zeitraums ermöglicht es, neues genetisches Material in alle späteren Gewebe zu übertragen, einschließlich zukünftiger Spermien und Eizellen. Unter Nutzung dieses Zeitfensters führten die Forschenden DNA-Konstrukte ein, die auf dem PiggyBac-Transposon basieren – einem "Ausschneide-und-Einfüge"-Element, das große DNA-Stücke in das Genom einfügt. Nach Tests verschiedener Helferplasmide identifizierten sie eine Version mit einer hyperaktiven PiggyBac-Enzymvariante, die erfolgreich transgene Linien erzeugte. Diese Larven exprimierten grüne und rote fluoreszierende Proteine in unterschiedlichen Geweben, und DNA-Analysen zeigten, dass die genetische Kassette in einem harmlosen Abschnitt zwischen natürlichen Genen eingelagert war.
Zellen beobachten und Gene ausschalten
Als Nächstes erzeugten die Autorinnen und Autoren spezialisiertere Reporter-Linien. Ein Konstrukt markierte ein Strukturprotein namens Tubulin mit grüner Fluoreszenz, um das zelluläre Innenskelett hervorzuheben, während ein anderes einen roten Marker an ein Histonprotein fusionierte, das die DNA im Zellkern umwickelt. Diese Linien leuchteten in charakteristischen Mustern im Darm, im Fettkörper, in den Seidendrüsen und anderen Geweben, sodass Forschende Zellstrukturen in lebenden oder fixierten Larven sichtbar machen konnten. Um über das Einfügen von Genen hinauszugehen und Gene tatsächlich zu deaktivieren, wandte das Team CRISPR–Cas9 an. Sie injizierten vorassemblierte CRISPR-Protein‑RNA-Komplexe, die auf den grünen Fluoreszenzmarker abzielten, in Embryonen, die die Reporter-Kassette bereits trugen. Viele Nachkommen zeigten teilweisen oder vollständigen Verlust des grünen Signals, behielten jedoch die rote Augenfluoreszenz, und DNA-Sequenzierung bestätigte kleine Insertionen und Deletionen an der beabsichtigten CRISPR-Schnittstelle.
Vom technischen Fortschritt zur praktischen Wirkung
Obwohl die Effizienz von PiggyBac und CRISPR in diesen Motten im Vergleich zu manchen anderen Insekten noch mäßig ist, skizzieren die Autorinnen und Autoren klare Wege zur Verbesserung durch Feinabstimmung von Promotoren, Enzymvarianten und Injektionsstrategien. Selbst in der aktuellen Form ist das Werkzeugset leistungsfähig genug, um stabile Linien zu erzeugen, die wichtige Zellkomponenten visualisieren oder gezielte Gen-Knockouts tragen. Für Nicht‑Spezialisten bedeutet das große Ganze: Galleria mellonella kann nun fast so flexibel genetisch manipuliert werden wie bekanntere Labortiere. Das erlaubt Forschenden, Raupen zu bauen, die über Infektionen berichten, Aspekte menschlicher Erkrankungen modellieren oder neue Medikamente testen — schneller, günstiger und humaner — und könnte so die Abhängigkeit von Säugetiermodellen in der Infektionsbiologie und verwandten Feldern reduzieren.
Zitation: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Schlüsselwörter: Galleria mellonella, Modell für Infektionen bei wirbellosen Tieren, Gentechnik, PiggyBac-Transgenese, CRISPR-Knockouts