Clear Sky Science · de
Erhöhte NO2-getriebene mehrphasige Bildung von partikulärem Nitrat und Sulfat unter Bedingungen hoher Luftfeuchte
Warum feuchte Luft trotzdem schmutzig sein kann
Viele Menschen gehen davon aus, dass feuchtes, nebliges Wetter die Luft reinigt und Schadstoffe aus der Atmosphäre wäscht. In Südchina passiert jedoch häufig das Gegenteil: Wenn warme, feuchte Meeresluft auf kühlere Landesluft trifft, baut sich dichter Dunst auf, obwohl die üblichen atmosphärischen Reinigungsprozesse schwach sind. Diese Studie erklärt, warum das so ist, und zeigt, wie ein verbreiteter Verkehrsschadstoff, Stickstoffdioxid, bei sehr hoher Luftfeuchte still und heimlich die schnelle Bildung schädlicher Feinstaubpartikel antreibt.
Klebende Luft über einer Küstenstadt
Die Forschenden konzentrierten sich auf Xiamen, eine Küstenstadt in Südchina, während zwei Wochen im frühen Frühjahr 2024. Zu dieser Jahreszeit kollidiert warme, feuchte Meeresluft häufig mit kühlerer, trockener Kontinentalluft und bleibt stationär, wodurch quasi-stationäre Wetterfronten entstehen. Während dieser Hochfeuchteereignisse wird die Luft stagnierend, die Windgeschwindigkeiten sinken und eine flache Luftschicht legt sich über die Stadt. Messungen von einer Dach-Überwachungsstation zeigten, dass die Feinstaubkonzentrationen (PM2,5) anstiegen, die Sicht abnahm und bei zunehmender Feuchte häufig Nebel auftrat. Innerhalb dieser dunstigen Phasen änderte sich die chemische Zusammensetzung der Partikel in zwei klaren Stufen: zunächst dominierte Nitrat, anschließend stieg Sulfat stark an.
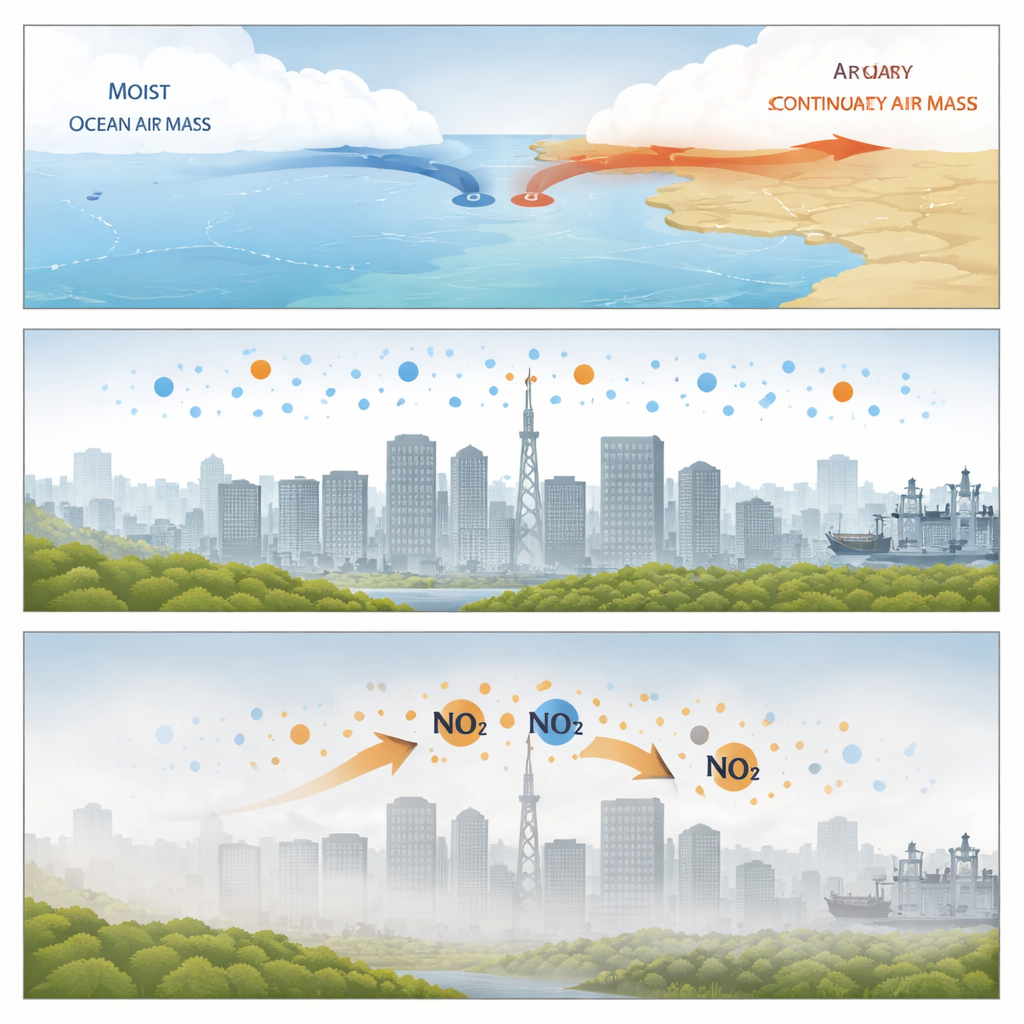
Zwei Phasen versteckter Chemie
In den frühen, sehr feuchten Stunden dieser Ereignisse reichern sich Partikel mit Nitrat an, obwohl die übliche sonnenlichtgetriebene Chemie schwach und die Ozonwerte gering waren. Die Gruppe fand, dass die beste Erklärung darin besteht, dass Stickstoffdioxid aus Verkehr und anderen Quellen direkt an nassen Partikeloberflächen und dünnen Wasserfilmen auf dem Boden aufgenommen wird. In diesen konzentrierten Tropfen reagiert Stickstoffdioxid schneller als in gewöhnlichem Wasser und bildet sowohl Nitrat als auch eine weitere reaktive Stickstoffform, die wieder in die Luft entweichen kann. Die enge Verbindung zwischen Stickstoffdioxid, Aerosolwasser, Partikeloberfläche und steigendem Nitrat deutet darauf hin, dass diese Oberflächenprozesse nachts die Nitratbildung dominierten.
Wenn Nebel Stickstoff in Schwefelpartikel verwandelt
Mit weiter steigender Luftfeuchte und der Bildung von Nebel verschob sich die Chemie. Sulfat, gebildet aus Schwefeldioxid, begann schnell zu wachsen und konnte Nitrat sogar überholen. Auch hier spielte Stickstoffdioxid eine zentrale Rolle, jedoch auf andere Weise. In Nebel- und größeren Tropfen oxidierten Stickstoffdioxid und seine Reaktionsprodukte gelösten Schwefel in einer Reihe wässriger Reaktionen. Ein wichtiges Zwischenprodukt, eine reaktive Stickstoffspezies, die sich mit Salpetriger Säure im Gleichgewicht befindet, zeigte sich in größeren, weniger sauren Tropfen beständiger als in winzigen, stärker sauren Partikeln. Diese längere Verweildauer ermöglichte wiederholte Angriffe auf gelösten Schwefel und trieb die rasche Sulfatproduktion genau dann an, wenn dichter Nebel und Dunst vorhanden waren.
Die Unsichtbaren quantifizieren
Um diese Ideen zu prüfen, bauten die Autorinnen und Autoren ein detailliertes Computer-»Boxmodell«, das Gasphasenchemie, Reaktionen in flüssigem Wasser und Austauschprozesse zwischen Luft und Partikeln kombinierte. Wenn sie die Aufnahme von Stickstoffdioxid durch nasse Partikel und Nebeltropfen zuließen, gab das Modell die beobachteten Anstiege von Nitrat und Sulfat gut wieder. Während der feuchten Ereignisse machte die direkte Aufnahme von Stickstoffdioxid nahezu die Hälfte aller gebildeten Nitratmengen aus, und stickstoffbasierte Oxidanten (Stickstoffdioxid plus seine wässrigen Produkte) erzeugten fast zwei Drittel des Sulfats. Nachts übertraf der Stickstoffdioxid-Weg deutlich die bekanntere Route über einen anderen nächtlichen Oxidanten, Dinitro-stoffpentoxid. Das Modell zeigte außerdem, dass Nebeltropfen mit ihrer größeren Größe und höheren pH-Werten besonders günstige Reaktionsräume für die Stickstoff–Schwefel-Chemie sind, die Sulfat bildet.
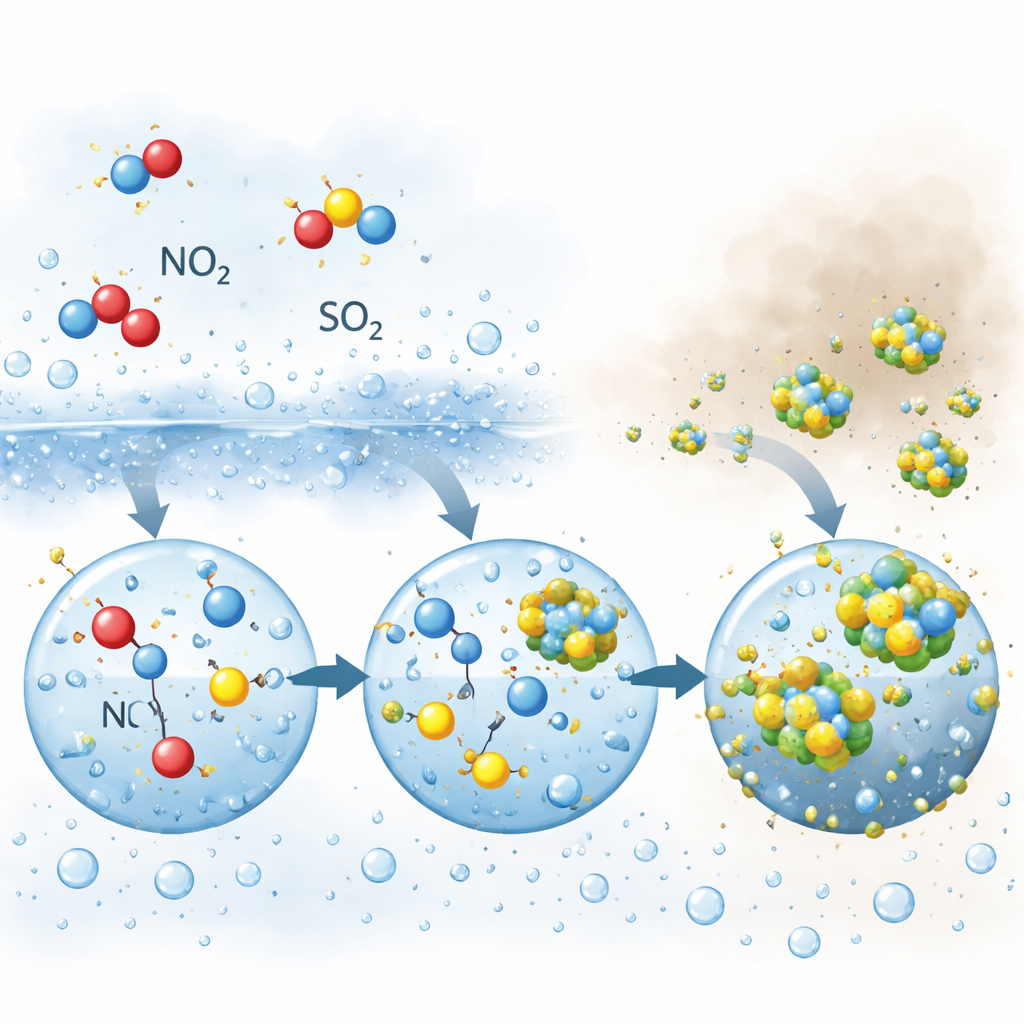
Was das für sauberere Luft bedeutet
Die Studie kommt zu dem Schluss, dass Stickstoffdioxid weit mehr tut, als nur als Warnsignal für Verkehrsemissionen zu dienen: Unter sehr feuchten, stagnierenden Bedingungen wird es zu einem starken Treiber der Feinstaubbildung. Indem es die Umwandlung gasförmiger Stickstoff- und Schwefelverbindungen in Nitrat- und Sulfatpartikel beschleunigt, helfen diese versteckten, wasserbasierten Reaktionen zu erklären, warum die Partikelwerte nicht so schnell gesunken sind wie die Emissionen von Stickstoff- und Schwefelgasen in China. Die Ergebnisse deuten darauf hin, dass wirksame Smogbekämpfung in Küsten- und feuchten Regionen nicht nur berücksichtigt, wie viel Stickstoffdioxid emittiert wird, sondern auch wie oft die Atmosphäre in diese klebrigen, nebeligen Zustände gerät, die sie in eine mikroskopische chemische Fabrik verwandeln.
Zitation: Lin, Z., Ji, X., Xu, L. et al. Enhanced NO2-driven multiphase formation of particulate nitrate and sulfate under high-humidity conditions. npj Clim Atmos Sci 9, 76 (2026). https://doi.org/10.1038/s41612-026-01352-5
Schlüsselwörter: Luftverschmutzung, Stickstoffdioxid, Feinstaub, hohe Luftfeuchte, Nebelchemie