Clear Sky Science · de
Richtung Krebs exprimiertes EGFR mit einem humanisierten monoklonalen Antikörper anvisieren
Krebs’ versteckte Kennzeichen finden
Krebsbehandlungen haben häufig Schwierigkeiten, ein Gleichgewicht zwischen dem gezielten Angriff auf Tumorzellen und dem Schutz gesunden Gewebes zu finden. Diese Arbeit beschreibt einen neu im Labor entwickelten Antikörper, genannt A10, der krebsartige Zellen mit einer bestimmten Form eines Wachstumsrezeptors von normalen Zellen unterscheiden kann. Indem er sich auf eine Struktur konzentriert, die vor allem dann sichtbar wird, wenn dieser Rezeptor verändert oder auf Tumorzellen übermäßig vorhanden ist, eröffnet A10 die Möglichkeit für Therapien, die sowohl wirksam als auch selektiver sind als viele derzeitige Optionen.
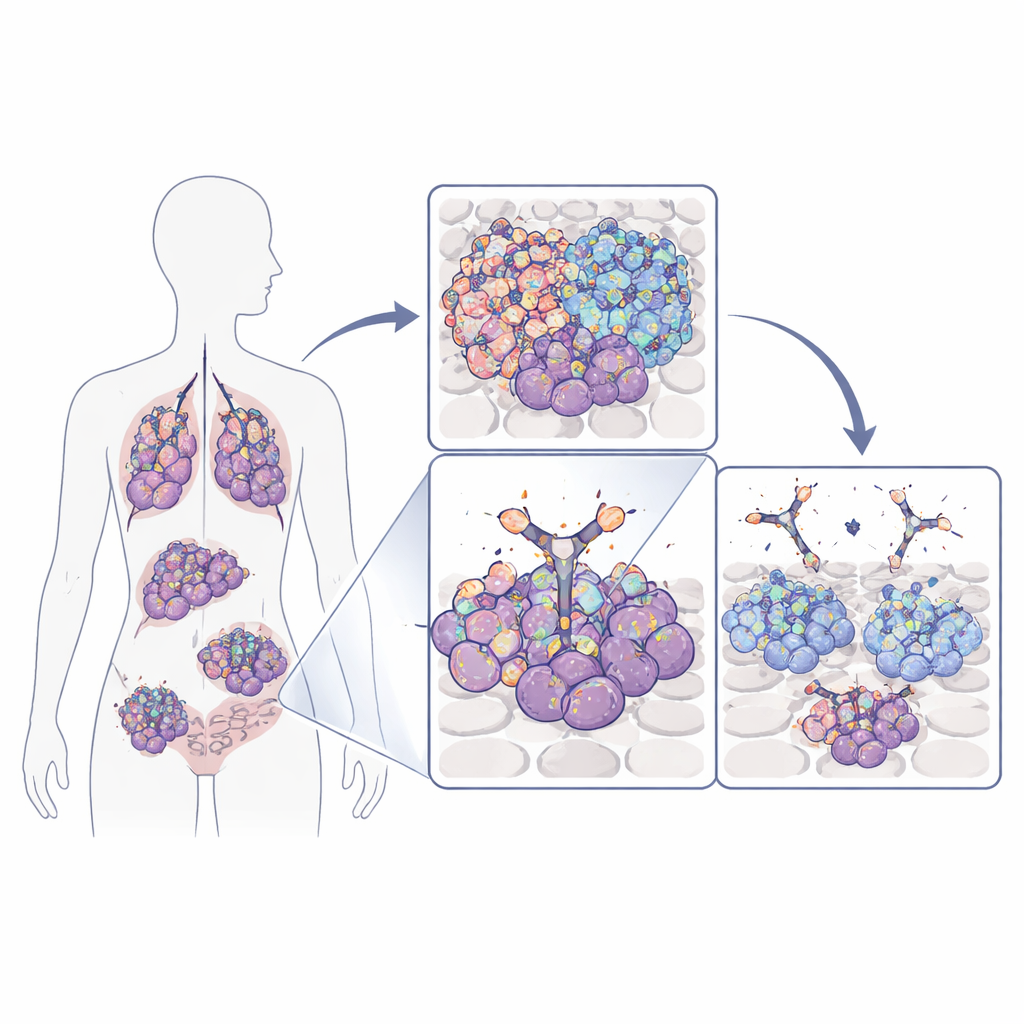
Warum dieser Wachstums-Schalter wichtig ist
Viele Tumore, einschließlich aggressiver Gehirn-, Lungen-, Brust- und Darmkrebse, sind auf ein Oberflächenprotein angewiesen, das epidermale Wachstumsfaktor-Rezeptor (EGFR) genannt wird, um zu wachsen und zu überleben. Tumorzellen können diesen Rezeptor erhöhen, indem sie entweder sein Gen amplifizieren, es mutieren oder eine verkürzte, ständig aktive Version produzieren, bekannt als EGFRvIII. Standardmedikamente, die EGFR blockieren, treffen oft sowohl Krebszellen als auch normales Gewebe, weil sie Teile des Rezeptors erkennen, die überall vorkommen. Das Team dieser Studie konzentrierte sich stattdessen auf eine kleine Schleife des EGFR, die hauptsächlich auf Krebszellen deutlich exponiert ist—entweder weil EGFR in abnormal hoher Anzahl vorhanden ist oder weil der Rezeptor in EGFRvIII verkürzt ist. Diese Schleife wirkt wie eine krebsspezifische „Flagge“, die prinzipiell deutlich sicherer anvisiert werden kann.
Einen Maus-Antikörper in ein Humanpräparat verwandeln
Die Forschenden hatten zuvor einen Maus-Antikörper, 40H3, entdeckt, der diese exponierte Schleife auf krebsexprimiertem EGFR erkannte. Maus-Antikörper können jedoch bei wiederholter Gabe beim Menschen Immunreaktionen auslösen. Um dies zu vermeiden, nutzte das Team Protein-Engineering-Methoden, um die entscheidenden Bindungssegmente von 40H3 auf menschliche Antikörperrahmen zu übertragen und so vierzehn „humanisierte“ Kandidaten sowie ein chimäres Referenzmolekül zu erzeugen. Als sie diese Varianten an Krebszellen testeten, die EGFR überexprimieren, banden drei Versionen besonders stark, und eine—A10—stach als stärkster Binder hervor, während sie normale Zellen mit moderatem EGFR-Spiegel weiterhin ignorierte. Über ein breites Panel von Tumorzelllinien mit unterschiedlichen EGFR-Mutationen und Kopienzahlen zeigte A10 durchweg höhere Bindung als der ursprüngliche Maus-Antikörper und behielt eine starke Präferenz für maligne Zellen bei.
Sehen, wie der Antikörper sein Ziel ergreift
Um zu verstehen, warum A10 so selektiv ist, löste das Team eine hochauflösende 3D-Struktur des aktiven Teils des Antikörpers im gebundenen Zustand an der EGFR-Schleife. Die Schleife faltet sich zu einer engen Haarnadelstruktur, die durch eine Disulfidbindung stabilisiert wird, und A10 umfasst diese Form in einer Rinne zwischen seinen beiden Armen, wobei zahlreiche geladene Kontakte sie fixieren. Der Vergleich dieser Struktur mit bekannten Formen des gesamten EGFR-Moleküls ergab eine wichtige Einsicht: Sowohl in der inaktiven „verankerten“ als auch in der aktiven Dimerform des normalen EGFR ist die Schleife größtenteils verborgen oder teilweise durch benachbarte Domänen abgeschirmt. Das bedeutet, dass A10 seine Bindungsstelle bei typischen, mäßig exprimierten Rezeptoren nicht leicht erreichen kann. Im Gegensatz dazu fehlt bei der krebsspezifischen EGFRvIII-Variante der vordere Teil des Rezeptors, wodurch die Schleife stark exponiert und zugänglich bleibt. Die Daten deuten darauf hin, dass A10 hauptsächlich EGFR in bestimmten Übergangsformen sowie in überfüllten oder verkürzten Konfigurationen erkennt, die bevorzugt auf Tumorzellen auftreten.
Den Antikörper bewaffnen, um Tumorzellen zu töten
Eine tumorspezifische Flagge zu erkennen ist an sich schon nützlich, aber die Forschenden gingen weiter und verwandten A10 in ein Antikörper-Wirkstoff-Konjugat (ADC). Sie banden chemisch eine potente zelltötende Verbindung, Monomethylauristatin E (MMAE), an A10 mithilfe eines Linkers, der innerhalb von Zellen aufgespalten werden kann. Dieses A10-MMAE-ADC band Krebszellen genauso gut wie der unkonjugierte Antikörper. In Labortests über viele Zelllinien hinweg war das ADC am effektivsten gegen Tumore mit sehr hohen EGFR-Spiegeln oder EGFRvIII, wo A10 viele Bindungsstellen vorfand. In diesen Zellen reichten winzige Mengen des Konjugats aus, um den Zelltod auszulösen. Tumorlinien mit weniger A10-Zielen oder angeborener Resistenz gegen MMAE waren weniger betroffen, und normale Fibroblasten mit wildtypischem EGFR blieben trotz Empfindlichkeit gegenüber freiem MMAE unversehrt. Die Ergebnisse zeigen, dass die Kombination aus selektiver Bindung und intrazellulärer Wirkstofffreisetzung die Toxizität scharf auf Krebszellen fokussieren kann.
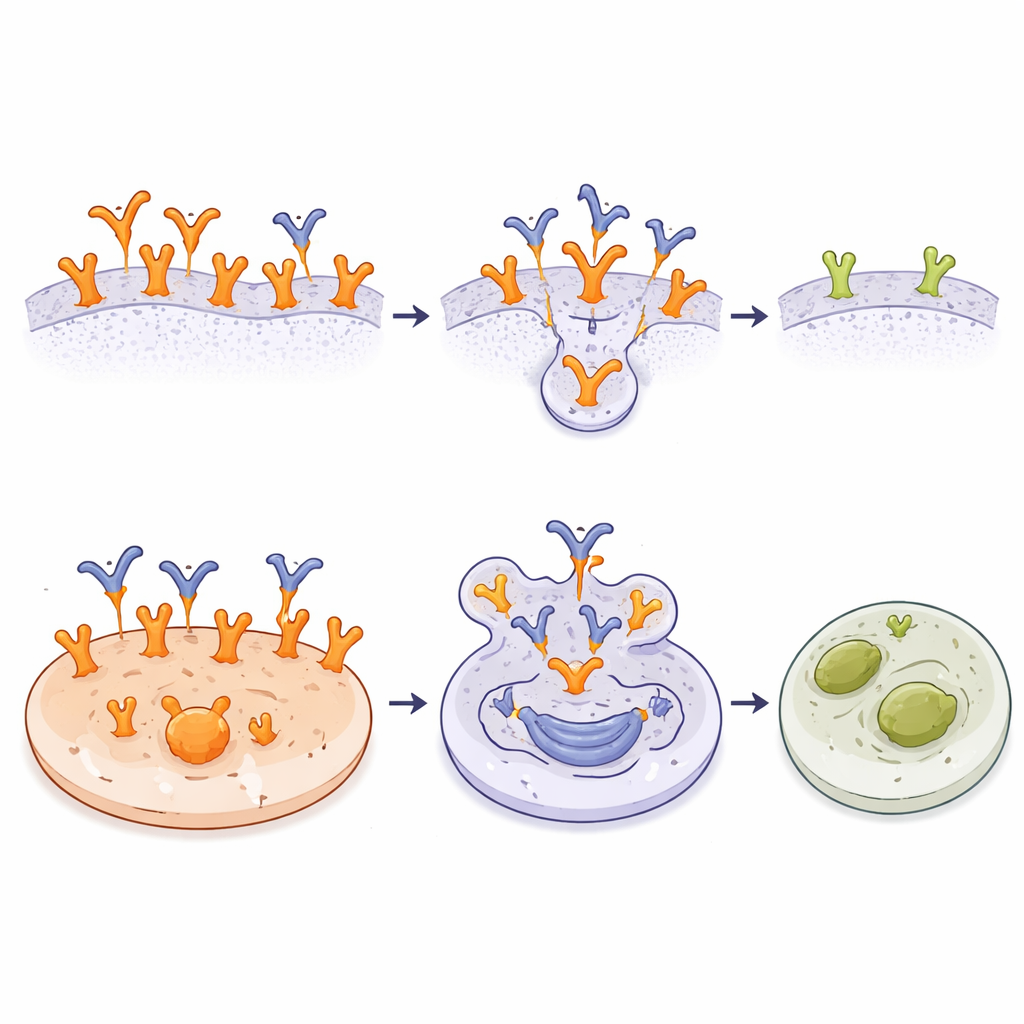
Was das für die künftige Krebsbehandlung bedeuten könnte
Vereinfacht gesagt zeigt diese Arbeit, dass es möglich ist, einen Antikörper zu konstruieren, der EGFR nur dann „sieht“, wenn er wie ein krebsfördernder Rezeptor aussieht und sich so verhält, und dabei die alltägliche Form auf gesundem Gewebe weitgehend ignoriert. Indem genau kartiert wird, wie A10 eine verborgene Schleife am EGFR ergreift, und gezeigt wird, dass ein auf A10 basierendes Wirkstoff-Konjugat rezeptorreiche Tumorzellen effizient töten kann, während normale Zellen verschont bleiben, liefert die Studie eine solide Grundlage für die Entwicklung sicherer, hochgradig zielgerichteter Therapien. Wenn sich diese Befunde auf Patientinnen und Patienten übertragen lassen, könnten zukünftige Behandlungen auf A10-Basis starke Wirkstoffe direkt an EGFR‑abhängige Tumore bringen und den Rest des Körpers größtenteils unberührt lassen.
Zitation: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Schlüsselwörter: EGFR, Antikörper-Wirkstoff-Konjugat, zielgerichtete Krebstherapie, Glioblastom, EGFRvIII