Clear Sky Science · de
Strukturelle und mechanistische Einblicke in die Zielsteuerung von α2β1- und α5β1-Integrinen durch bioengineerte extrazelluläre Vesikel aus Lungenkrebszellen
Die verborgenen Boten des Krebses
Lungenkrebs wird häufig spät entdeckt, wenn die Behandlungsmöglichkeiten eingeschränkt sind. Eine vielversprechende Strategie ist, Medikamente gezielt nur an Krebszellen zu liefern und gesundes Gewebe zu schonen. Diese Studie untersucht ein winziges, natürliches Transportsystem – extrazelluläre Vesikel (EVs), die Krebszellen bereits zur Kommunikation nutzen. Durch die Umgestaltung dieser Vesikel mit einem kurzen Zielmolekül zeigen die Forscher, wie sie an spezifische Andockstellen auf Tumorzellen binden können, und legen damit die Grundlage für präzisere und weniger toxische Krebstherapien.
Natürliche Pakete als intelligente Kuriere
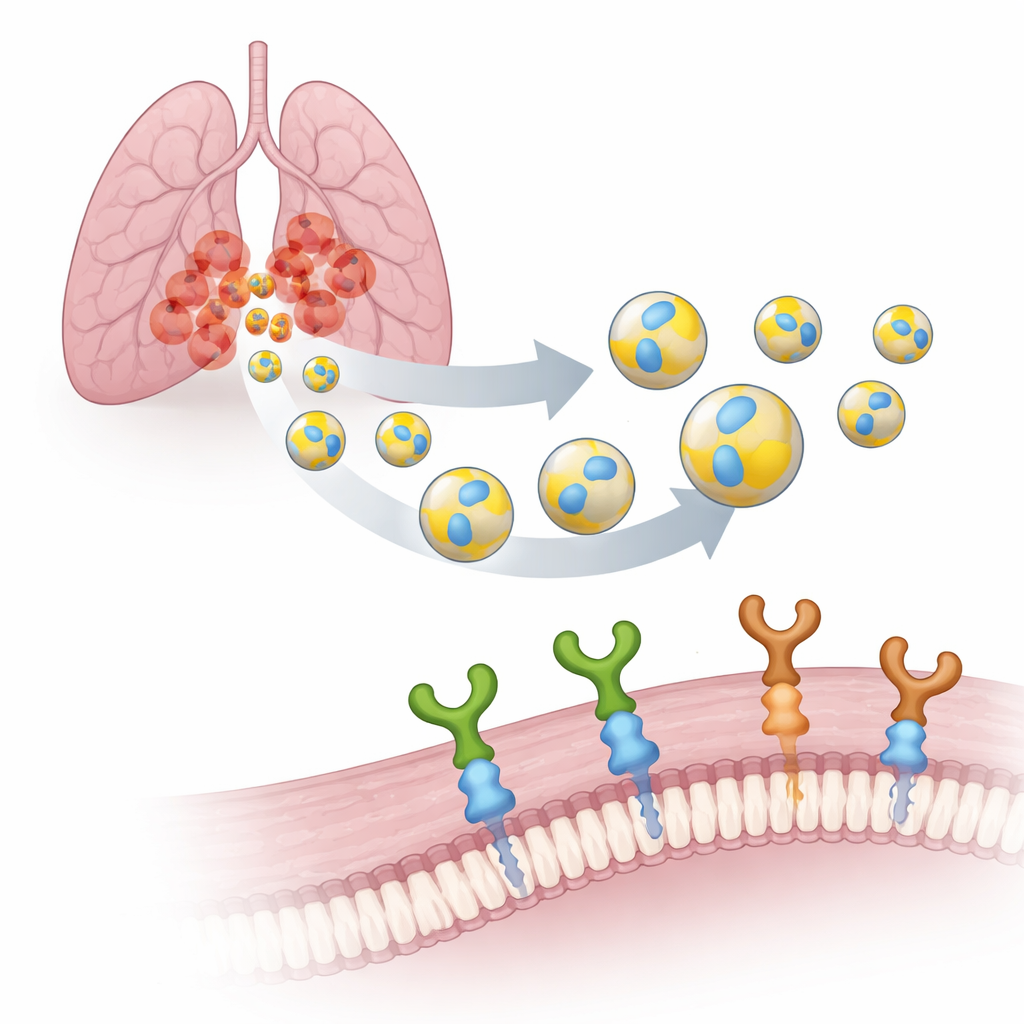
Jede Zelle in unserem Körper setzt EVs frei: nanoskalige Bläschen, umgeben von einer Membran – ein wenig wie mikroskopische Seifenblasen. Da sie von unseren eigenen Zellen stammen, sind EVs biologisch abbaubar, durchdringen biologische Barrieren leicht und lösen weniger Nebenwirkungen aus als synthetische Träger. Das Team konzentrierte sich auf EVs, die von menschlichen Lungenkrebszellen (A549) produziert werden, und stattete ihre Oberfläche mit einem kleinen sieben Bausteine langen Tag namens PTHTRWA aus. Frühere Experimente hatten gezeigt, dass dieses Tag EVs dazu bringt, in Mäusen gezielt Lungenkrebszellen anzusteuern und viel stärker an Tumorzellen zu binden als an normale Lungenzellen, bei nur geringer Toxizität.
Die richtigen Andockstellen an Tumorzellen finden
Um diese markierten Vesikel wirklich zielgerichtet einsetzen zu können, mussten die Forscher herausfinden, welche „Häfen“ auf Krebszellen sie erkennen. Sie untersuchten zwei verwandte Oberflächenrezeptoren, α2β1- und α5β1-Integrine. Das sind molekulare Greifhaken, die Zellen helfen, an ihrer Umgebung zu haften und Signale zu empfangen. In Lungentumoren steht α5β1 in starkem Zusammenhang mit aggressivem Verhalten, Metastasierung und schlechter Prognose, während α2β1 mit Chemoresistenz verknüpft wurde. Mit einer sensitiven Methode namens Oberflächenplasmonresonanz verglich das Team, wie stark PTHTRWA-dekorierte EVs an beide Integrine binden. Sie fanden heraus, dass Vesikel ohne Tag kaum wechselwirkten, während markierte EVs unter nahezu physiologischen Bedingungen feste, stabile Komplexe mit beiden Rezeptoren bildeten.
Das molekulare Umschlingen im Detail
Um auf atomarer Ebene nachzuvollziehen, was geschieht, wenn das Tag auf die Integrine trifft, wandten sich die Forscher Computersimulationen zu. Sie bauten dreidimensionale Modelle des Tags, gebunden an Schlüsselbereiche der Integrine, und ließen diese Systeme hunderte von Nanosekunden in virtuellem Wasser evolvieren. Die Berechnungen zeigten, dass sich PTHTRWA passgenau in eine flache Rinne des α2β1-Rezeptors einfügt und dort ein Netzwerk aus Wasserstoffbrücken und hydrophoben Kontakten bildet, das den Komplex stabilisiert. Entscheidend war, dass die Bindung eine offenere Konformation des Rezeptors – die hochaffine, signalbereite Form – gegenüber dem geschlossenen Ruhezustand begünstigte. Tests mit leicht modifizierten Versionen des Tags zeigten, dass kleine chemische Änderungen an einem Ende die Lage des Peptids in der Rinne und seine Präferenz für das eine oder andere Integrin subtil verändern können.
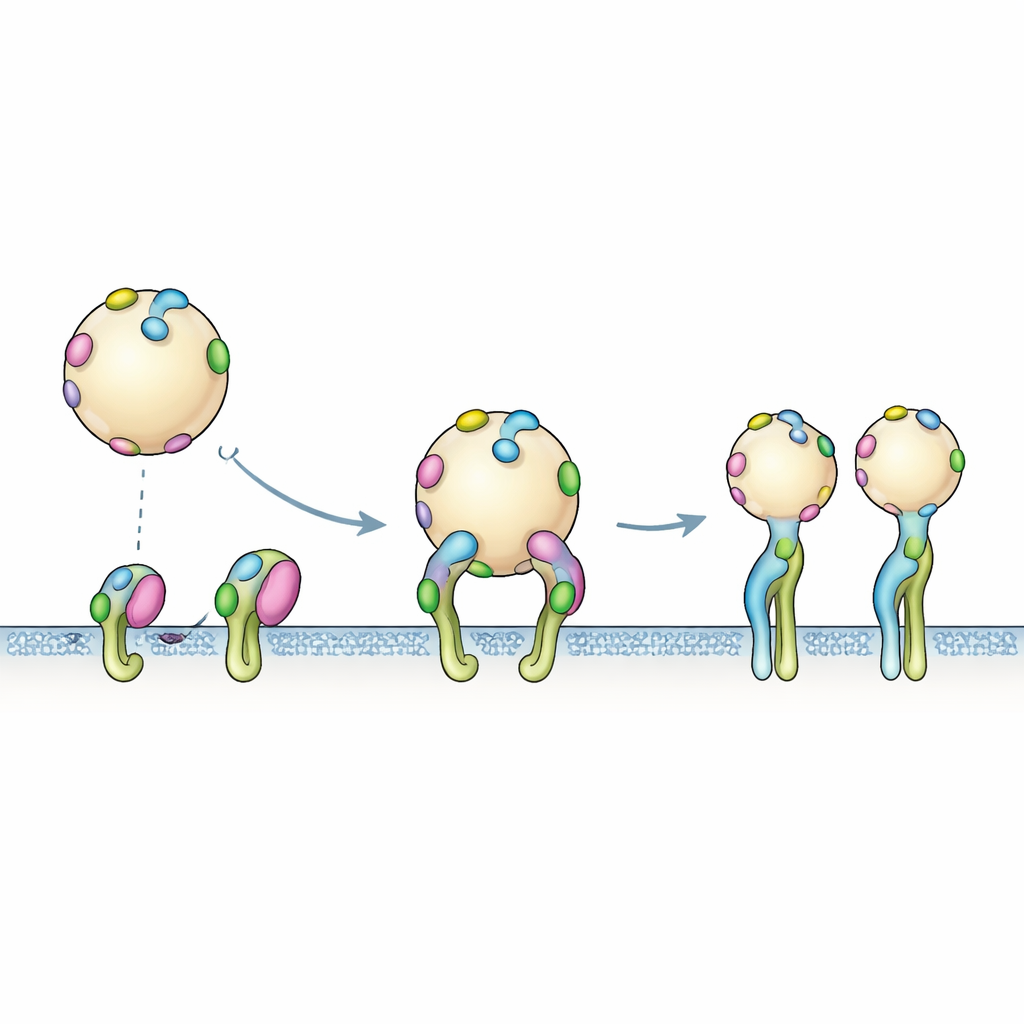
Von einzelnen Tags zu multivalenten Griffen
Computermodelle erfassen jeweils ein Tag, das an einen Rezeptor bindet, doch die reale EV-Oberfläche ist mit vielen Kopien von PTHTRWA übersät. Die Bindungsversuche spiegelten diese multivalente Realität wider: Sobald ein markiertes Vesikel ein Integrin-Cluster erreicht, können mehrere Tags gleichzeitig binden. Die Sensordaten passten am besten zu einem zweistufigen Prozess. Zuerst dockt das Vesikel kurz über schnelle, reversible Kontakte an. Dann folgt eine langsamere Umordnung, bei der die Integrine in ihre offene Form wechseln und der Gesamthalt verstärkt wird. Diese kooperative, vielhändige Fassung erklärt, warum die scheinbare Bindungsstärke ganzer Vesikel höher ist als aus den Eigenschaften eines einzelnen Tags vorhergesagt würde.
Was das für zukünftige Therapien bedeuten könnte
Kurz gesagt zeigt die Studie, dass EVs, die mit dem PTHTRWA-Tag ausgestattet sind, Integrine erkennen können, die in Lungenkrebs überaktiv sind, und dies dadurch tun, dass sie diese Rezeptoren in eine offen gebundene Form drücken. Durch die detaillierte Kartierung dieser Wechselwirkungen liefern die Forscher Gestaltungsprinzipien für die nächste Generation von vesikelbasierten Trägern, die Medikamente, Bildgebungsagentien oder andere Nutzlasten gezielt an maligne Zellen liefern könnten, während sie gesundes Gewebe größtenteils ignorieren. Zwar sind weitere Studien in Tieren und Menschen nötig, doch diese Integrin-Targeting-Strategie bringt die Vision einer personalisierten, EV-basierten Krebstherapie einen Schritt näher zur Realität.
Zitation: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Schlüsselwörter: Lungenkrebs, extrazelluläre Vesikel, Integrine, gezielte Wirkstoffabgabe, molekulare Simulationen